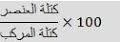1.1ماهي تجربة رذرفورد؟
قام رذرفورد بـتجربته الشهيرة أو ما تسمى بـ(تجربة رقاقة الذهب) وهي تجربة تعتمد على تسليط أشعة من جسيمات ألفا الموجبةعلى رقاقة ذهب ، فوجد أن بعض الأشعة تنعكس، والبعض ينحرف، ومعظمها ينفذ خلال صفيحة الذهب، ويدل ذلك على وجود بعض مساحات فارغة في الذرة، وأيضًا وجود جسيمات لها نفسشحنة الأشعة، وهناك جسيمات لها شحنة مختلفة عن شحنة الأشعة.
1.2كيف قام بالتجربة؟
قام رذرفورد بتركيب جهاز خاص للقيام بالتجربة. ومكونات الجهاز كانت :
1.مكعب من الرصاص يحتوي على مصدر يشع جسيمات ألفا.
2.لوحة معدنية على هيئة دائرة غير مكتملة مغطاة بطبعة من (كبريتيد الخارصين) الذي يعطي وميضاً عند اصطدام (جسيمات ألفا) به.
3.صحيفة رقيقة جداً من الذهب .
1.3ماهي خطوات التجربة؟
1-جعل رذرفورد جسيمات ألفا تصطدم بـاللوحة المعدنية المغطاة بـ(كبريتيد الخارصين)
2- وضع صحيفة ذهب رقيقة جداً بحيث تعترض مسار الأشعة قبل الاصطدام باللوحة المعدنية
1.4المشاهدة والاستنتاجات:
لاحظ رذرفورد عدة ملاحظات على هذه التجربة وبناء عليها استخرج استنتاجات ،وأهمها:
1-لاحظ أن معظم جسيمات ألفا الموجبة نفذت دون أن تعاني من دون انحراف واستنتج من ذلك أن معظم حجم الذرة فراغ.
2-لاحظ أيضا أن نسبة قليلة جدا من جسيمات ألفا لم تنفذ من صفيحة الذهب وارتدت عكس مسارها واستنتج عدة استنتاجات:
-نفاذ الأشعة يعني أن معظم حجم الذرة فراغ
-وانحراف الأشعة يعني أنها اقتربت من جسم مشحون بشحنة مشابهة (موجبة) لذلك تنافرت معها, أي أن شحنة النواة موجبة. ووجد ان الذرة فيها فراغ كبير.
1.5نموذج رذرفورد لتركيب الذرة:
استنتج رذرفورد أن نموذج طومسون لم يكن صحيحا لأنه لم يستطع أن يفسر نتائج تجربة (رقاقة الذهب).
واستنتج أيضاً أن الذرة تتكون غالباً من فراغ تتحرك فيه الإلكترونات. كما استنتج أن معظم الشحنة الموجبة للذرة ومعظم كتلتها تتركز في مكان صغير وكثيف في مركز الذرة ،وسماه (النواة)،وترتبط الإلكترونات السالبة الشحنة بالذرة من خلال التجاذب مع النواة الموجبة الشحنة
1.6لماذا اختار رذرفورد الذهب في تجربته؟
اختار رذرفورد الذهب في تجربته لان الذهب من أكثر العناصر قابلية للطرق ، فيمكن تقطيعه لشرائح رقيقة جدا، وهذا يفي بغرض التجربة لأنه أراد شريحة رقيقة كفاية لدراسة اختراق جسيمات ألفا من عدمها.
raneem noor
قام رذرفورد بـتجربته الشهيرة أو ما تسمى بـ(تجربة رقاقة الذهب) وهي تجربة تعتمد على تسليط أشعة من جسيمات ألفا الموجبةعلى رقاقة ذهب ، فوجد أن بعض الأشعة تنعكس، والبعض ينحرف، ومعظمها ينفذ خلال صفيحة الذهب، ويدل ذلك على وجود بعض مساحات فارغة في الذرة، وأيضًا وجود جسيمات لها نفسشحنة الأشعة، وهناك جسيمات لها شحنة مختلفة عن شحنة الأشعة.
1.2كيف قام بالتجربة؟
قام رذرفورد بتركيب جهاز خاص للقيام بالتجربة. ومكونات الجهاز كانت :
1.مكعب من الرصاص يحتوي على مصدر يشع جسيمات ألفا.
2.لوحة معدنية على هيئة دائرة غير مكتملة مغطاة بطبعة من (كبريتيد الخارصين) الذي يعطي وميضاً عند اصطدام (جسيمات ألفا) به.
3.صحيفة رقيقة جداً من الذهب .
1.3ماهي خطوات التجربة؟
1-جعل رذرفورد جسيمات ألفا تصطدم بـاللوحة المعدنية المغطاة بـ(كبريتيد الخارصين)
2- وضع صحيفة ذهب رقيقة جداً بحيث تعترض مسار الأشعة قبل الاصطدام باللوحة المعدنية
1.4المشاهدة والاستنتاجات:
لاحظ رذرفورد عدة ملاحظات على هذه التجربة وبناء عليها استخرج استنتاجات ،وأهمها:
1-لاحظ أن معظم جسيمات ألفا الموجبة نفذت دون أن تعاني من دون انحراف واستنتج من ذلك أن معظم حجم الذرة فراغ.
2-لاحظ أيضا أن نسبة قليلة جدا من جسيمات ألفا لم تنفذ من صفيحة الذهب وارتدت عكس مسارها واستنتج عدة استنتاجات:
-نفاذ الأشعة يعني أن معظم حجم الذرة فراغ
-وانحراف الأشعة يعني أنها اقتربت من جسم مشحون بشحنة مشابهة (موجبة) لذلك تنافرت معها, أي أن شحنة النواة موجبة. ووجد ان الذرة فيها فراغ كبير.
1.5نموذج رذرفورد لتركيب الذرة:
استنتج رذرفورد أن نموذج طومسون لم يكن صحيحا لأنه لم يستطع أن يفسر نتائج تجربة (رقاقة الذهب).
واستنتج أيضاً أن الذرة تتكون غالباً من فراغ تتحرك فيه الإلكترونات. كما استنتج أن معظم الشحنة الموجبة للذرة ومعظم كتلتها تتركز في مكان صغير وكثيف في مركز الذرة ،وسماه (النواة)،وترتبط الإلكترونات السالبة الشحنة بالذرة من خلال التجاذب مع النواة الموجبة الشحنة
1.6لماذا اختار رذرفورد الذهب في تجربته؟
اختار رذرفورد الذهب في تجربته لان الذهب من أكثر العناصر قابلية للطرق ، فيمكن تقطيعه لشرائح رقيقة جدا، وهذا يفي بغرض التجربة لأنه أراد شريحة رقيقة كفاية لدراسة اختراق جسيمات ألفا من عدمها.
raneem noor
التفاعلات النووية
اذا حدث تفاعل لذرة عنصر معين ، ولم تلعب الالكترونات دوراً فيه ، وأدى هذا التفاعل إلى تغيير عدد
نيوكليونات النواة ، فإن هذا التفاعل يسمى تفاعلاً نووياً واذا تغيّر العدد الذري للعنصر خلال هذاالتفاعل ينتج عنصراً جديداً ، أما اذا تغيّر العدد الكتلي للعنصر فينتج نظيراً للعنصر الداخل في التفاعل وبذلك يكون التفاعل النووي : " هو التفاعل الذي يغيّر النواة " .
وقد يتم التفاعل النووي لعنصر معين بدون مؤثر خارجي وقد تحدثنا عن هذا النوع في الفصل السابق
والذي يسّمى "النشاط الاشعاعي الطبيعي " .
وقد نقوم نحن باستحداث مؤثرات خارجية وفي هذه الحالة يسمّى التفاعل باسم " التفاعل النووي الاصطناعي " .
حاجز الجهد النووي : Nuclear Potential Barrier
لاحداث تفاعل نووي بين نواتين ، لابد من تقريبهما من بعضهما غلى مسافة يبدأ عندها تأثير النوى النووية ، ولذلك يتم تسريع احداهما لاكسابها طاقة حركية كافية تمكّنها من الاقتراب من النواة الأخرى والتغلب على قوى التنافر الكهرسكونية بينهما . فاذا قذف جسيم موجب الشحنة شحنة (القذفية) (ش1) باتجاه نواة ثقيلة (ش2) ، فان طاقة حركة الجسيم (ط ح) تتناقص تدريجياً نتيجة قوة التنافر بينه وبين النواة ، ولذلك تزداد طاقة الوضع (ط و) .
طو اذا ما أريد لهذا الجسيم أن يصل إلى جدار النواة ، فإنه ينبغي أن يمتلك طاقة
raneem noor
اذا حدث تفاعل لذرة عنصر معين ، ولم تلعب الالكترونات دوراً فيه ، وأدى هذا التفاعل إلى تغيير عدد
نيوكليونات النواة ، فإن هذا التفاعل يسمى تفاعلاً نووياً واذا تغيّر العدد الذري للعنصر خلال هذاالتفاعل ينتج عنصراً جديداً ، أما اذا تغيّر العدد الكتلي للعنصر فينتج نظيراً للعنصر الداخل في التفاعل وبذلك يكون التفاعل النووي : " هو التفاعل الذي يغيّر النواة " .
وقد يتم التفاعل النووي لعنصر معين بدون مؤثر خارجي وقد تحدثنا عن هذا النوع في الفصل السابق
والذي يسّمى "النشاط الاشعاعي الطبيعي " .
وقد نقوم نحن باستحداث مؤثرات خارجية وفي هذه الحالة يسمّى التفاعل باسم " التفاعل النووي الاصطناعي " .
حاجز الجهد النووي : Nuclear Potential Barrier
لاحداث تفاعل نووي بين نواتين ، لابد من تقريبهما من بعضهما غلى مسافة يبدأ عندها تأثير النوى النووية ، ولذلك يتم تسريع احداهما لاكسابها طاقة حركية كافية تمكّنها من الاقتراب من النواة الأخرى والتغلب على قوى التنافر الكهرسكونية بينهما . فاذا قذف جسيم موجب الشحنة شحنة (القذفية) (ش1) باتجاه نواة ثقيلة (ش2) ، فان طاقة حركة الجسيم (ط ح) تتناقص تدريجياً نتيجة قوة التنافر بينه وبين النواة ، ولذلك تزداد طاقة الوضع (ط و) .
طو اذا ما أريد لهذا الجسيم أن يصل إلى جدار النواة ، فإنه ينبغي أن يمتلك طاقة
raneem noor
كيف اكتشف الإلكترون ؟
ولد العالم J.J. Thomson عام 1856 في بريطانيا، وبدأ دراسته الهندسية وهو في ال 14 من العمر في كلية أوينز العلمية، وبنى فيها دعامة رياضية وهندسية أهلته لاقتحام عالم الفيزياء التجريبي، فانضم إلى مخبر كافينديش Cavendish التابع لجامعة كامبريدج عام 1884، وبعد 13 عاماً من البحث في ذلك المختبر ... اكتشف الإلكترون.
لقد اكتشفت الأشعة المهبطية بواسطة العالم الألماني يوليوس بلاكر Julius Plucker ولم يكن لدى العلماء حينها أي تصور حول ماهية هذا الأشعة وما تتكون منه، وبدأت التجارب والجدالات حولها، فهل هي أمواج ؟ أم جسيمات ؟
في عام 1896، قرر تومسون أن يصمم بعض التجارب التي ستضع بدورها حدا لتلك الجدالات، فصمم أنبوب الأشعة المهبطية Cathode Ray Tube، وبدأ باكتشافاته واحداً تلو آخر، حيث استنتج من تجاربه بدايةً أنها أشعة ذات شحنة سالبة، ومن ثم توصل إلى أنها تتأثر بالحقل المغناطيسي الذي يحرفها عن مسارها المستقيم، وأخيراً، توصل إلى أنها تتأثر بالحقل الكهربائي الذي حرفها عن مسارها عند وصل بطارية على طرفي الأنبوب.
قام تومسون ببعض القياسات المتعلقة بزاوية انحراف الأشعة وعلاقتها بقوة الحقل المطبق، واستنتج منها كتلة الجسيمات التي تشكل الأشعة التي ذهل لصغر قيمتها لأنها كانت أصغر كتلة تعرف حينها على الإطلاق، وأعاد تجاربه مرات ومرات ومئات المرات ليتحقق من النتائج التي أظهرت جميعها أن نسبة كتلة تلك الجسيمات إلى كتلة ذرة الهيدروجين تساوي 1/1000، وبالتالي، هي أصغر من أصغر جسم مكتشف آنذاك (ذرة الهيدروجين) بألف مرة.
جاءت تسمية إلكترون electron بواسطة العالم الفيزيائي جورج ستوني عام 1891 كأصغر جسيم كهربائي، واستمرت بعد ذلك تسمية الجسيمات باللاحقة on، فمثلاً، جسيم الضوء سُمي فوتون، وجسيم الصوت سُمي فونون ... وهكذا.
raneem noor
ولد العالم J.J. Thomson عام 1856 في بريطانيا، وبدأ دراسته الهندسية وهو في ال 14 من العمر في كلية أوينز العلمية، وبنى فيها دعامة رياضية وهندسية أهلته لاقتحام عالم الفيزياء التجريبي، فانضم إلى مخبر كافينديش Cavendish التابع لجامعة كامبريدج عام 1884، وبعد 13 عاماً من البحث في ذلك المختبر ... اكتشف الإلكترون.
لقد اكتشفت الأشعة المهبطية بواسطة العالم الألماني يوليوس بلاكر Julius Plucker ولم يكن لدى العلماء حينها أي تصور حول ماهية هذا الأشعة وما تتكون منه، وبدأت التجارب والجدالات حولها، فهل هي أمواج ؟ أم جسيمات ؟
في عام 1896، قرر تومسون أن يصمم بعض التجارب التي ستضع بدورها حدا لتلك الجدالات، فصمم أنبوب الأشعة المهبطية Cathode Ray Tube، وبدأ باكتشافاته واحداً تلو آخر، حيث استنتج من تجاربه بدايةً أنها أشعة ذات شحنة سالبة، ومن ثم توصل إلى أنها تتأثر بالحقل المغناطيسي الذي يحرفها عن مسارها المستقيم، وأخيراً، توصل إلى أنها تتأثر بالحقل الكهربائي الذي حرفها عن مسارها عند وصل بطارية على طرفي الأنبوب.
قام تومسون ببعض القياسات المتعلقة بزاوية انحراف الأشعة وعلاقتها بقوة الحقل المطبق، واستنتج منها كتلة الجسيمات التي تشكل الأشعة التي ذهل لصغر قيمتها لأنها كانت أصغر كتلة تعرف حينها على الإطلاق، وأعاد تجاربه مرات ومرات ومئات المرات ليتحقق من النتائج التي أظهرت جميعها أن نسبة كتلة تلك الجسيمات إلى كتلة ذرة الهيدروجين تساوي 1/1000، وبالتالي، هي أصغر من أصغر جسم مكتشف آنذاك (ذرة الهيدروجين) بألف مرة.
جاءت تسمية إلكترون electron بواسطة العالم الفيزيائي جورج ستوني عام 1891 كأصغر جسيم كهربائي، واستمرت بعد ذلك تسمية الجسيمات باللاحقة on، فمثلاً، جسيم الضوء سُمي فوتون، وجسيم الصوت سُمي فونون ... وهكذا.
raneem noor
الميكروسكوب النفقي الماسح Scanning tunneling microscope STM
عندما نتحدث عن الميكروسكوب فان اول ما نفكر به هو جهاز الميكروسكوب الذي نعرفه في مختبرات المدراس والذي يعمل بتكوين صورة ضوئية عن العينة المراد النظر لها بشكل مكبر، ومع تقدم العلم وتطوره اصبح بالإمكان ان نحصل على تكبير يفوق أي توقع. في بدايات القرن العشرين مع اكتشاف الفيزياء الحديثة والخاصية المزدوجة للإشعاع الكهرومغناطيسي والجسيمات المادية ونظرية ميكانيكا الكم التي تدرس الاجسام على المستوى الذري الدقيق اصبح بالإمكان تصميم ميكروسكوب يعمل على التكبير بدرجة عالية جدا تصل الى مئات الاف المرات وهي تعتمد على استخدام موجة الالكترون وقد تحدثنا عن الميكروسكوب الالكتروني الماسح SEM والميكروسكوب الالكتروني النافذ TEM وتوالت الاكتشافات ليظهر لنا في العام 1981 ميكروسكوب جديد من حيث فكرة عمله ومن حيث امكانياته وقدراته واستخداماته المتنوعة هذا الميكروسكوب يعرف باسم الميكروسكوب النفقي الماسح scanning tunneling microscope او STM.
يعتبر جهاز الميكروسكوب النفقي من الاجهزة الاساسية في علم النانوتكنولوجي والذي ساعد في دراسة المواد على المستوى الذري وفي بناء وفحص التراكيب النانوية. وتعتمد فكرة عمله على مبدأ النفق الكمي quantum tunneling.
فعندما يقترب طرف المجس الموصل للكهرباء والذي يعرف باسم tip من السطح المراد فحصه يطبق فرق جهد بين السطح وطرف المجس tip يسمح بمرور الالكترونات من خلال نفق في الفراغ بينهما.
تيار الالكترونات هذا تعرف باسم التيار النفقي tunneling current. يعتمد التيار النفقي على موضع المجس بالنسبة للسطح وعلى فرق الجهد المطبق وعلى الكثافة الموضعية للعينة.
في هذا المقال من كيف تعمل الاشياء سوف نقوم بشرح فكرة عمل جهاز الميكروسكوب النفقي STM وانماط تشغيله كما سوف نتعرف على الاجهزة التي تعمل على نفس فكرة عمله.
raneem noor
عندما نتحدث عن الميكروسكوب فان اول ما نفكر به هو جهاز الميكروسكوب الذي نعرفه في مختبرات المدراس والذي يعمل بتكوين صورة ضوئية عن العينة المراد النظر لها بشكل مكبر، ومع تقدم العلم وتطوره اصبح بالإمكان ان نحصل على تكبير يفوق أي توقع. في بدايات القرن العشرين مع اكتشاف الفيزياء الحديثة والخاصية المزدوجة للإشعاع الكهرومغناطيسي والجسيمات المادية ونظرية ميكانيكا الكم التي تدرس الاجسام على المستوى الذري الدقيق اصبح بالإمكان تصميم ميكروسكوب يعمل على التكبير بدرجة عالية جدا تصل الى مئات الاف المرات وهي تعتمد على استخدام موجة الالكترون وقد تحدثنا عن الميكروسكوب الالكتروني الماسح SEM والميكروسكوب الالكتروني النافذ TEM وتوالت الاكتشافات ليظهر لنا في العام 1981 ميكروسكوب جديد من حيث فكرة عمله ومن حيث امكانياته وقدراته واستخداماته المتنوعة هذا الميكروسكوب يعرف باسم الميكروسكوب النفقي الماسح scanning tunneling microscope او STM.
يعتبر جهاز الميكروسكوب النفقي من الاجهزة الاساسية في علم النانوتكنولوجي والذي ساعد في دراسة المواد على المستوى الذري وفي بناء وفحص التراكيب النانوية. وتعتمد فكرة عمله على مبدأ النفق الكمي quantum tunneling.
فعندما يقترب طرف المجس الموصل للكهرباء والذي يعرف باسم tip من السطح المراد فحصه يطبق فرق جهد بين السطح وطرف المجس tip يسمح بمرور الالكترونات من خلال نفق في الفراغ بينهما.
تيار الالكترونات هذا تعرف باسم التيار النفقي tunneling current. يعتمد التيار النفقي على موضع المجس بالنسبة للسطح وعلى فرق الجهد المطبق وعلى الكثافة الموضعية للعينة.
في هذا المقال من كيف تعمل الاشياء سوف نقوم بشرح فكرة عمل جهاز الميكروسكوب النفقي STM وانماط تشغيله كما سوف نتعرف على الاجهزة التي تعمل على نفس فكرة عمله.
raneem noor
نظرية دالتون الذرية
يعتبر الانجليزي جون دالتون أباً للكيمياء الحديثة وذلك بعد أن أقترح نظرية الذرية للمادة في حوالى عام 1803م. أن مفهوم الذرة (غير قابلة للتجزئة) لم يبدأ مع دالتون ولكن مع علماء الاغريق قبل الميلاد والذين أوضحوا عدم امكانية تقسيم المادة إلى الابد إلى اجزاء اصغر فاصغر وانه في نهاية المطاف يجب ان تكون هنالك جسيمات غير قابلة للتجزئة. لم تكن هذه الاقتراحات القديمة مبنية على نتائج تجارب علمية وإنما كانت ثمار تفكير عميق . تختلف نظرية دالتون عن ذلك كونها تعتمد على قوانين بقاء الكتلة والنسب الثابتة والتي اشتقت من العديد من الاستنتاجات المباشرة . يمكن التعبير عن النظرية التي اقترحها بالاتي :
1- تتكون المادة من العديد من الجسيمات الغير قابلة للتجزئة تسمى الذرات. يعتبر الانجليزي جون دالتونأباً للكيمياء الحديثة وذلك بعد أن أقترح نظرية الذرية للمادة في حوالى عام 1803م. أن مفهوم الذرة (غير قابلة للتجزئة) لم يبدأ مع دالتون ولكن مع علماء الاغريق قبل الميلاد والذين أوضحوا عدم امكانية تقسيم المادة إلى الابد إلى اجزاء اصغر فاصغر وانه في نهاية المطاف يجب ان تكون هنالك جسيمات غير قابلة للتجزئة. لم تكن هذه الاقتراحات القديمة مبنية على نتائج تجارب علمية وإنما كانت ثمار تفكير عميق . تختلف نظرية دالتون عن ذلك كونها تعتمد على قوانين بقاء الكتلة والنسب الثابتة والتي اشتقت من العديد من الاستنتاجات المباشرة . يمكن التعبير عن النظرية التي اقترحها بالاتي :
1- تتكون المادة من العديد من الجسيمات الغير قابلة للتجزئة تسمى الذرات.
2- تتميز كل ذرات العنصر بنفس الخواص ( الحجم ، الشكل ، الكتلة ) والتي تختلف باختلاف العناصر .
3- يحدث التفاعل الكيميائي عند تبديل وضعية الذرات وتحويلها من منظومة لاخري.
لقد أثبتت نظرية دالتون نجاحها من خلال تفسيرها لبعض الحقائق القائمة في ذلك الزمان كما انها استطاعت ايضا التنبؤ ببعض القوانين الغير مكتشفة :
اولا : تتضمن هذه النظرية قانون حفظ الكتلة حيث ان التفاعل الكيميائى لايفعل شيئا سوى اعادة توزيع الذرات ولم تفقد اي ذرة في هذة المنظومة وبالتالي تظل الكتلة ثابتة عند حدوث التفاعل الكيميائى .
ثانيا : تفسر هذه النظرية قانون النسب الثابتة . افترض ان مادة ما تتكون من عنصرين a و b. وان اي جزيئي من هذه المادة يتكون من ذرة واحدة منa وذرة واحدة من b يعرف الجزيئى بانة مجموعه ذرات مترابطة مع بعضها بقوة تسمح لها بالتصرف او اعادة التنظيم كجسيم واحد. افترض ايضا ان كتلة الذرة a تكون ضعف كتلة الذرة b وبالتالى فان الذرة a تساهم بضعف الكتلة التي تساهم بها الذرة b في تكوين جزيئى واحد من هذه المادة الامر الذي يعني ان نسبة كتلة الذرة aالى الذرة b هي 2/1 .
اما اذا اخذنا مجموعة كبيرة من جزيئات هذة المادة فاننا نجد دائما ان عدد ذرات aمتساويا لعدد ذرات b الامر الذي يعني انة بغض النظر عن حجم العينة فاننا دائما نحصل على نسبة كتلة aالى b تساوي 2/1 . بالمثل اذا فاعلنا a مع b لنحصل على هذا الجزيئى فنجد ان اي ذرة من a تتحد مع ذرة واحدة منb اما اذا خلطنا 100 ذرة من a مع 110 ذرة من b فنجد انة قد تبقت 10 ذرات من bغير متفاعلة بعد اكتمال التفاعل.
ثالثا : لقد تنبأت نظرية دالتون بقانون النسب المتضاعفة الذي يقول : عند تكوين مركبين مختلفين من نفس العنصرين فان كتلتي احد العنصرين اللتان تتفاعلان مع كتلة ثابتة من العنصر الاخر تكونان في شكل نسبة عددين بسيطين وصحيحين . قد يظهر هذا القانون وكانة اكثر تعقيدا من حقيقتة . دعنا نتحدث عن مركبين يتكونان من عنصري الأكسجين والكربون . اذا وجدنا في احدهما ( أول اكسيد الكربون ) ان 1.33 جم من الاكسجين متحدة مع 1.00 جم من الكربون بينما وجدنا في الاخر ( ثاني اكسيد الكربون ) ان 2.66 جم من الاكسجين متحدة مع 1.00 جم من الكربون فان نسبة كتلتي الاكسجين 2.66جم/1.33جم اللتان تتحدان مع كتلة ثابتة من الكربون 1.00 جم تكون في شكل عددين صحيحين :
تتفق هذه النسبة مع النظرية الذرية حيث ان أول أكسيد الكربون يحتوي على ذرة واحدة كربون تكون متحدة مع ذرة واحدة من الاكسجين بينما نجد ان ثاني اكسيد الكربون يحتوي ذرة كربون واحدة تكون متحدة مع ذرتين من الأكسجين . نسبة لان ثاني اكسيد الكربون ضعف ذرات الاكسجين المتحدة مع ذرة الكربون مثلما لأول أكسيد الكربون فان وزن الاكسجين في جزيئى ثاني اكسيد الكربون يجب ان يكون ضعف وزن الاكسجين في جزيئى أول اكسيد الكربون
raneem noor
يعتبر الانجليزي جون دالتون أباً للكيمياء الحديثة وذلك بعد أن أقترح نظرية الذرية للمادة في حوالى عام 1803م. أن مفهوم الذرة (غير قابلة للتجزئة) لم يبدأ مع دالتون ولكن مع علماء الاغريق قبل الميلاد والذين أوضحوا عدم امكانية تقسيم المادة إلى الابد إلى اجزاء اصغر فاصغر وانه في نهاية المطاف يجب ان تكون هنالك جسيمات غير قابلة للتجزئة. لم تكن هذه الاقتراحات القديمة مبنية على نتائج تجارب علمية وإنما كانت ثمار تفكير عميق . تختلف نظرية دالتون عن ذلك كونها تعتمد على قوانين بقاء الكتلة والنسب الثابتة والتي اشتقت من العديد من الاستنتاجات المباشرة . يمكن التعبير عن النظرية التي اقترحها بالاتي :
1- تتكون المادة من العديد من الجسيمات الغير قابلة للتجزئة تسمى الذرات. يعتبر الانجليزي جون دالتونأباً للكيمياء الحديثة وذلك بعد أن أقترح نظرية الذرية للمادة في حوالى عام 1803م. أن مفهوم الذرة (غير قابلة للتجزئة) لم يبدأ مع دالتون ولكن مع علماء الاغريق قبل الميلاد والذين أوضحوا عدم امكانية تقسيم المادة إلى الابد إلى اجزاء اصغر فاصغر وانه في نهاية المطاف يجب ان تكون هنالك جسيمات غير قابلة للتجزئة. لم تكن هذه الاقتراحات القديمة مبنية على نتائج تجارب علمية وإنما كانت ثمار تفكير عميق . تختلف نظرية دالتون عن ذلك كونها تعتمد على قوانين بقاء الكتلة والنسب الثابتة والتي اشتقت من العديد من الاستنتاجات المباشرة . يمكن التعبير عن النظرية التي اقترحها بالاتي :
1- تتكون المادة من العديد من الجسيمات الغير قابلة للتجزئة تسمى الذرات.
2- تتميز كل ذرات العنصر بنفس الخواص ( الحجم ، الشكل ، الكتلة ) والتي تختلف باختلاف العناصر .
3- يحدث التفاعل الكيميائي عند تبديل وضعية الذرات وتحويلها من منظومة لاخري.
لقد أثبتت نظرية دالتون نجاحها من خلال تفسيرها لبعض الحقائق القائمة في ذلك الزمان كما انها استطاعت ايضا التنبؤ ببعض القوانين الغير مكتشفة :
اولا : تتضمن هذه النظرية قانون حفظ الكتلة حيث ان التفاعل الكيميائى لايفعل شيئا سوى اعادة توزيع الذرات ولم تفقد اي ذرة في هذة المنظومة وبالتالي تظل الكتلة ثابتة عند حدوث التفاعل الكيميائى .
ثانيا : تفسر هذه النظرية قانون النسب الثابتة . افترض ان مادة ما تتكون من عنصرين a و b. وان اي جزيئي من هذه المادة يتكون من ذرة واحدة منa وذرة واحدة من b يعرف الجزيئى بانة مجموعه ذرات مترابطة مع بعضها بقوة تسمح لها بالتصرف او اعادة التنظيم كجسيم واحد. افترض ايضا ان كتلة الذرة a تكون ضعف كتلة الذرة b وبالتالى فان الذرة a تساهم بضعف الكتلة التي تساهم بها الذرة b في تكوين جزيئى واحد من هذه المادة الامر الذي يعني ان نسبة كتلة الذرة aالى الذرة b هي 2/1 .
اما اذا اخذنا مجموعة كبيرة من جزيئات هذة المادة فاننا نجد دائما ان عدد ذرات aمتساويا لعدد ذرات b الامر الذي يعني انة بغض النظر عن حجم العينة فاننا دائما نحصل على نسبة كتلة aالى b تساوي 2/1 . بالمثل اذا فاعلنا a مع b لنحصل على هذا الجزيئى فنجد ان اي ذرة من a تتحد مع ذرة واحدة منb اما اذا خلطنا 100 ذرة من a مع 110 ذرة من b فنجد انة قد تبقت 10 ذرات من bغير متفاعلة بعد اكتمال التفاعل.
ثالثا : لقد تنبأت نظرية دالتون بقانون النسب المتضاعفة الذي يقول : عند تكوين مركبين مختلفين من نفس العنصرين فان كتلتي احد العنصرين اللتان تتفاعلان مع كتلة ثابتة من العنصر الاخر تكونان في شكل نسبة عددين بسيطين وصحيحين . قد يظهر هذا القانون وكانة اكثر تعقيدا من حقيقتة . دعنا نتحدث عن مركبين يتكونان من عنصري الأكسجين والكربون . اذا وجدنا في احدهما ( أول اكسيد الكربون ) ان 1.33 جم من الاكسجين متحدة مع 1.00 جم من الكربون بينما وجدنا في الاخر ( ثاني اكسيد الكربون ) ان 2.66 جم من الاكسجين متحدة مع 1.00 جم من الكربون فان نسبة كتلتي الاكسجين 2.66جم/1.33جم اللتان تتحدان مع كتلة ثابتة من الكربون 1.00 جم تكون في شكل عددين صحيحين :
تتفق هذه النسبة مع النظرية الذرية حيث ان أول أكسيد الكربون يحتوي على ذرة واحدة كربون تكون متحدة مع ذرة واحدة من الاكسجين بينما نجد ان ثاني اكسيد الكربون يحتوي ذرة كربون واحدة تكون متحدة مع ذرتين من الأكسجين . نسبة لان ثاني اكسيد الكربون ضعف ذرات الاكسجين المتحدة مع ذرة الكربون مثلما لأول أكسيد الكربون فان وزن الاكسجين في جزيئى ثاني اكسيد الكربون يجب ان يكون ضعف وزن الاكسجين في جزيئى أول اكسيد الكربون
raneem noor
الفروع الرئيسية للكيمياء
و تنقسم الكيمياء إلى فرعين عامين هما :-
1 – الكيمياء غير العضوية :
و تختص بالمواد ذات الطبيعة الحجرية مثل الصخور , الخامات, المعادن ..................الخ.
2 – الكيمياء العضوية :
و تختص بمركبات عنصر الكربون دون المركبات البسيطة منها مثل أكاسيد الكربون و الكربونات و الكربيدات ...............الخ .
و يرجع تقسيم علم الكيمياء إلى هذين القسمين إلى أصل تاريخي ففي عام 1838 نجح فردرش وولر في تخليق
مادة عضوية ( يوريا ) و كان يظن قبل ذلك عدم إمكان تكوين هذه المواد صناعياً .
و قد أدت معرفة الصفات الخاصة لكثير من المواد العضوية بعد ذلك إلى هذا التقسيم و العمل به .
و قد أدى تداخل علوم الكيمياء و الطبيعة و الرياضة إلى نمو فروع آخرى من فروع الكيمياء في أواخر القرن الماضي فمنها ما سمي
بالكيمياء الطبيعية
و يشمل النواحي الطبيعية و الرياضية للتفاعلات العضوية و غير العضوية .
و يوجد فرع
آخر للكيمياء ظهر نتيجة لتطبيق التفاعلات الكيميائية علي نطاق تجاري كبير سمي
بالكيمياء التكنولوجية
و هو يعالج العمليات الإنتاجية للمواد باستخدام الكيمياء الصناعية علي نطاق كبير بالإضافة إلي دراسة المواد المنتجة و استخداماتها .
و فيما يلي تفصيل شامل لفروع الكيمياء :-
1 - الكيمياء التحليلية :
تختص بتعيين خواص المواد الكيميائية والصيغ الكيميائية للمركبات و المخاليط وتركيبها.
والتحليل الكمي يقدر كميات المواد الكيميائية المختلفة التي تتكون منها تلك المواد .
والتحليل النوعي يكشف عن نوع العناصر والمركبات التي تتكون منها المواد.
2 - الكيمياء الراديوية :
تختص بتعيين وإنتاج العناصر المشعة واستخداماتها في دراسة العمليات الكيميائية .
3 - الكيمياء التطبيقية :
تعنى بالتطبيق العملي بالمواد والعمليات الكيميائية.
4 - الكيمياء الزراعية :
تهتم بتطوير الأسمدة والمبيدات وتدرس العمليات الكيميائية التي تحدث داخل التربة والعمليات التي تتعلق بنمو المحاصيل .
5 - كيمياء البيئة:
تدرس وتراقب وتحاول ضبط العمليات الكيميائية والعوامل البيئية الأخرى وعلاقتها بالكائنات الحية .
6- الكيمياء الصناعية:
تختص بإنتاج المواد الخام كيميائياً وتطوير العمليات والمنتجات الكيميائية الصناعية ودراستها ومراقبتها.
7 - الكيمياء الحيوية:
تتعامل مع التراكيب والعمليات الكيميائية التي تحدث داخل الكائنات الحية .
8 - الكيمياء الغير عضوية:
تتعامل مع العمليات الكيميائية التي لا تحتوي على روابط بين ذرتي كربون (كربون – كربون) .
9 - الكيمياء العضوية :
تعنى بدراسة المواد الكيميائية التي تحتوي على روابط بين ذرات الكربون .
10 - الكيمياء الفيزيائية :
تترجم وتفسر العمليات الكيميائية اعتماداً على الخواص الفيزيائية للمادة, مثل الكتلة والحركة والحرارة والكهرباء والإشعاع .
11 - الحركية الكيميائية :
تدرس الخطوات في التفاعلات الكيميائية, والعوامل التي تؤثر على معدل سرعة التفاعلات الكيميائية .
12 - الديناميكا الحرارية الكيميائية:
تتعامل مع تغير الطاقة الذي يحدث أثناء التفاعلات الكيميائية وكيف يؤثر اختلاف الضغط والحرارة على التفاعلات .
13 - الكيمياء النووية:
تستخدم الطرق الكيميائية في دراسة التفاعلات النووية .
14 - كيمياء الكم :
تحلل توزيع الإلكترونات في الجزيئات وتفسر السلوك الكيميائي للجزيئات اعتماداً على البناء الإلكتروني .
15 - الكيمياء الإشعاعية :
تهتم بالآثار الكيميائية للأشعة العالية الطاقة على المواد .
16 - كيمياء حالة الصلابة :
تتعامل مع التركيب الكيميائي للمواد الصلبة, والتغير الذي يحدث داخل هذه المواد و فيما بينها.
17 - الكيمياء الفراغية :
تدرس ترتيب الذرات في الجزيئات والخواص التي تنتج عن هذا الترتيب .
18 - كيمياء السطوح :
تهتم باختبار الخواص السطحية للمواد الكيميائية .
19 - كيمياء البوليمرات :
تهتم بالبلاستيك والجزيئات السلسلية الأخرى المتشابكة التي تتكون بتشابك الجزيئات الصغيرة بعضها ببعض .
20 - الكيمياء الاصطناعية :
تختص باتحاد العناصر الكيميائية والمركبات لإنتاج مواد مماثلة لمواد موجودة في الطبيعة, أو تشكيل مواد .
raneem noor
و تنقسم الكيمياء إلى فرعين عامين هما :-
1 – الكيمياء غير العضوية :
و تختص بالمواد ذات الطبيعة الحجرية مثل الصخور , الخامات, المعادن ..................الخ.
2 – الكيمياء العضوية :
و تختص بمركبات عنصر الكربون دون المركبات البسيطة منها مثل أكاسيد الكربون و الكربونات و الكربيدات ...............الخ .
و يرجع تقسيم علم الكيمياء إلى هذين القسمين إلى أصل تاريخي ففي عام 1838 نجح فردرش وولر في تخليق
مادة عضوية ( يوريا ) و كان يظن قبل ذلك عدم إمكان تكوين هذه المواد صناعياً .
و قد أدت معرفة الصفات الخاصة لكثير من المواد العضوية بعد ذلك إلى هذا التقسيم و العمل به .
و قد أدى تداخل علوم الكيمياء و الطبيعة و الرياضة إلى نمو فروع آخرى من فروع الكيمياء في أواخر القرن الماضي فمنها ما سمي
بالكيمياء الطبيعية
و يشمل النواحي الطبيعية و الرياضية للتفاعلات العضوية و غير العضوية .
و يوجد فرع
آخر للكيمياء ظهر نتيجة لتطبيق التفاعلات الكيميائية علي نطاق تجاري كبير سمي
بالكيمياء التكنولوجية
و هو يعالج العمليات الإنتاجية للمواد باستخدام الكيمياء الصناعية علي نطاق كبير بالإضافة إلي دراسة المواد المنتجة و استخداماتها .
و فيما يلي تفصيل شامل لفروع الكيمياء :-
1 - الكيمياء التحليلية :
تختص بتعيين خواص المواد الكيميائية والصيغ الكيميائية للمركبات و المخاليط وتركيبها.
والتحليل الكمي يقدر كميات المواد الكيميائية المختلفة التي تتكون منها تلك المواد .
والتحليل النوعي يكشف عن نوع العناصر والمركبات التي تتكون منها المواد.
2 - الكيمياء الراديوية :
تختص بتعيين وإنتاج العناصر المشعة واستخداماتها في دراسة العمليات الكيميائية .
3 - الكيمياء التطبيقية :
تعنى بالتطبيق العملي بالمواد والعمليات الكيميائية.
4 - الكيمياء الزراعية :
تهتم بتطوير الأسمدة والمبيدات وتدرس العمليات الكيميائية التي تحدث داخل التربة والعمليات التي تتعلق بنمو المحاصيل .
5 - كيمياء البيئة:
تدرس وتراقب وتحاول ضبط العمليات الكيميائية والعوامل البيئية الأخرى وعلاقتها بالكائنات الحية .
6- الكيمياء الصناعية:
تختص بإنتاج المواد الخام كيميائياً وتطوير العمليات والمنتجات الكيميائية الصناعية ودراستها ومراقبتها.
7 - الكيمياء الحيوية:
تتعامل مع التراكيب والعمليات الكيميائية التي تحدث داخل الكائنات الحية .
8 - الكيمياء الغير عضوية:
تتعامل مع العمليات الكيميائية التي لا تحتوي على روابط بين ذرتي كربون (كربون – كربون) .
9 - الكيمياء العضوية :
تعنى بدراسة المواد الكيميائية التي تحتوي على روابط بين ذرات الكربون .
10 - الكيمياء الفيزيائية :
تترجم وتفسر العمليات الكيميائية اعتماداً على الخواص الفيزيائية للمادة, مثل الكتلة والحركة والحرارة والكهرباء والإشعاع .
11 - الحركية الكيميائية :
تدرس الخطوات في التفاعلات الكيميائية, والعوامل التي تؤثر على معدل سرعة التفاعلات الكيميائية .
12 - الديناميكا الحرارية الكيميائية:
تتعامل مع تغير الطاقة الذي يحدث أثناء التفاعلات الكيميائية وكيف يؤثر اختلاف الضغط والحرارة على التفاعلات .
13 - الكيمياء النووية:
تستخدم الطرق الكيميائية في دراسة التفاعلات النووية .
14 - كيمياء الكم :
تحلل توزيع الإلكترونات في الجزيئات وتفسر السلوك الكيميائي للجزيئات اعتماداً على البناء الإلكتروني .
15 - الكيمياء الإشعاعية :
تهتم بالآثار الكيميائية للأشعة العالية الطاقة على المواد .
16 - كيمياء حالة الصلابة :
تتعامل مع التركيب الكيميائي للمواد الصلبة, والتغير الذي يحدث داخل هذه المواد و فيما بينها.
17 - الكيمياء الفراغية :
تدرس ترتيب الذرات في الجزيئات والخواص التي تنتج عن هذا الترتيب .
18 - كيمياء السطوح :
تهتم باختبار الخواص السطحية للمواد الكيميائية .
19 - كيمياء البوليمرات :
تهتم بالبلاستيك والجزيئات السلسلية الأخرى المتشابكة التي تتكون بتشابك الجزيئات الصغيرة بعضها ببعض .
20 - الكيمياء الاصطناعية :
تختص باتحاد العناصر الكيميائية والمركبات لإنتاج مواد مماثلة لمواد موجودة في الطبيعة, أو تشكيل مواد .
raneem noor
طبقة الأوزون وأهميتها
إن طبقة الأوزون هي الطبقة التي تحتوي علي غاز الأوزون في طبقات الجو العليا من الغلاف الجوي والتي تقع في الغلاف الاستراتوسفيري للغلاف الجوي، وطبقة الأوزون تحيط بالغلاف الجوي إحاطة كامـلة علي ارتفاع يتراوح مابين 20 و 30 كيلـو متر من سطـح الأرض ويتراوح سمكها من 2-8 كيلو متر.
وتقوم طبقة الأوزون بدور المرشح الطبيعى والدرع الواقى الذى يحيط بالأرض ليحميها من الجزء الضار من الأشعة فوق البنفسجية (Ultra Violet - B) ذات الأضرار الجسيمة بصحة الإنسان والحيوان على حد سواء، كما تقلل من نمو النبات وإنتاج المحاصيل الزراعية، وتؤثر على نظم البيئة المائية.
إن النشاط البشري وما استحدثه الإنسان من تكنولوجيا في تخليق المواد الكيميائية قد أدي بعض منها إلي تدمير طبقة الأوزون ومن أهم المواد الكيميائية التي تستنفد طبقة الأوزون:
أ- الكلوروفلوروكربونات والهيدروكلوروفلوروكربونات المستخدمة بكثرة في أجهزة التبريد والتكييف المنزلية والتجارية والصناعية.
ب- الهالونات المستخدمة في أنظمة مكافحة الحرائق.
ج- مادة بروميد الميثيل المستخدمة كمبيد حشري في تخزين المحاصيل الزراعية وتعقيم التربة الزراعية.
د- بعض المذيبات المستخدمة فى تنظيف الأجزاء الميكانيكية و المعدنية والدوائر الالكترونية مثل مادة رابع كلوريد الكربون.
وتحتوى هذه الغازات عادة على ذرات من الكلور أو البروم تنفصل نتيجة لتأثرها بالأشعة فوق البنفسجية فتتجه إلى أقرب وحدة من غاز الأوزون الذى يتكون من ثلاث ذرات أوكسجين وتضم إليها إحداها تاركة ذرتين (وحدة لا تقاوم الأشعة فوق البنفسجية) وتمضى ذرة الكلور ومعها ذرة الأوكسجين إلى أن تلتقى بذرة أوكسجين أخرى منفردة، فتلتحم ذرتا الأوكسجين مع بعضهما مكونة وحدة أوكسجين (وحدة لا تقاوم الأشعة فوق البنفسجية) وتنفصل ذرة الكلور وتمضى إلى وحدة أوزون أخرى لتفعل معها نفس الشىء – وهكذا تتكرر عملية الهدم هذه ملايين المرات وذلك فى الطبقات العليا (الاستراتوسفيرية).
شوق المرشدي
إن طبقة الأوزون هي الطبقة التي تحتوي علي غاز الأوزون في طبقات الجو العليا من الغلاف الجوي والتي تقع في الغلاف الاستراتوسفيري للغلاف الجوي، وطبقة الأوزون تحيط بالغلاف الجوي إحاطة كامـلة علي ارتفاع يتراوح مابين 20 و 30 كيلـو متر من سطـح الأرض ويتراوح سمكها من 2-8 كيلو متر.
وتقوم طبقة الأوزون بدور المرشح الطبيعى والدرع الواقى الذى يحيط بالأرض ليحميها من الجزء الضار من الأشعة فوق البنفسجية (Ultra Violet - B) ذات الأضرار الجسيمة بصحة الإنسان والحيوان على حد سواء، كما تقلل من نمو النبات وإنتاج المحاصيل الزراعية، وتؤثر على نظم البيئة المائية.
إن النشاط البشري وما استحدثه الإنسان من تكنولوجيا في تخليق المواد الكيميائية قد أدي بعض منها إلي تدمير طبقة الأوزون ومن أهم المواد الكيميائية التي تستنفد طبقة الأوزون:
أ- الكلوروفلوروكربونات والهيدروكلوروفلوروكربونات المستخدمة بكثرة في أجهزة التبريد والتكييف المنزلية والتجارية والصناعية.
ب- الهالونات المستخدمة في أنظمة مكافحة الحرائق.
ج- مادة بروميد الميثيل المستخدمة كمبيد حشري في تخزين المحاصيل الزراعية وتعقيم التربة الزراعية.
د- بعض المذيبات المستخدمة فى تنظيف الأجزاء الميكانيكية و المعدنية والدوائر الالكترونية مثل مادة رابع كلوريد الكربون.
وتحتوى هذه الغازات عادة على ذرات من الكلور أو البروم تنفصل نتيجة لتأثرها بالأشعة فوق البنفسجية فتتجه إلى أقرب وحدة من غاز الأوزون الذى يتكون من ثلاث ذرات أوكسجين وتضم إليها إحداها تاركة ذرتين (وحدة لا تقاوم الأشعة فوق البنفسجية) وتمضى ذرة الكلور ومعها ذرة الأوكسجين إلى أن تلتقى بذرة أوكسجين أخرى منفردة، فتلتحم ذرتا الأوكسجين مع بعضهما مكونة وحدة أوكسجين (وحدة لا تقاوم الأشعة فوق البنفسجية) وتنفصل ذرة الكلور وتمضى إلى وحدة أوزون أخرى لتفعل معها نفس الشىء – وهكذا تتكرر عملية الهدم هذه ملايين المرات وذلك فى الطبقات العليا (الاستراتوسفيرية).
شوق المرشدي
قانون حفظ المادة وقانون النسب الثابتة:
تمهيد:
تنطبق النتائج التي توصلنا إليها عند دراسة الماء وكبريتيد الكالسيوم ينطبق على كل المركبات المعروفة, فهي كلها تنتج عن اتحاد العناصر مع بعضها بنسب وزنية ثابتة, وهذا ما وجده العلماء نتيجة للأبحاث والدراسات. ولو حصلنا الآن على عينات نقية من ملح الطعام سواء من تبخير ماء البحر الميت. أو تبخير ماء البحر المتوسط, أو من التفاعل:
NaOH + HCl
NaCl + H2O
وحللناها لوجدنا أنها تتكون من اتحاد i23i غم صوديوم مع i35.5i غم من الكلور تقريباً وينتج عن ذلك i58.5iغم من الملح تقريباً. وهذه النسبة أو أحد أجزائها أو مضاعفاتها هي التي نحصل عليها دائماً وذلك حسب كمية عينة الملح المدروسة صغيرة أم كبيرة.
اكتشف العلماء هذه الحقيقة في مطلع القرن التاسع عشر وتوصلوا نتيجة هذا الاكتشاف إلى قانونين هامين أصبحا الآن في عداد المسلمات وهما:
أولاً: قانون حفظ الكتلة Law of Conservation of mass
ثانياً: قانون النسب الثابتة Law of Definite Proportions
أولاً: قانون حفظ الكتلة Law of Conservation of mass
عند حدوث التغيرات الكيميائية فإن مجموع كتل المواد المتفاعلة يساوي مجموع كتل المواد بعد نهاية التفاعل.
مثال: عند تفاعل i3i غرامات من الكربون معi8i غرامات من الأوكسجين ينتج i11i غم من ثاني أوكسيد الكربون.
ولو تفاعل i3i غرامات من C مع i15i غرامات من O2 فإنه ينتج عن ذلك i11i غم CO2 وبقي i7i غرامات من O2 كما هي دون تغيير , أي أن كمية الأوكسجين الزائد بقيت كما هي من حيث الكتلة والنوع.
سؤال: اكتب جملة بلغتك الخاصة تعبر عن فهمك لقانون حفظ الكتلة
الإجابة:
" عند حدوث التغيرات الكيميائية يبقى مجموع كتل المواد قبل التفاعل وبعده ثابتاً دون تغيير
raneem noor
تمهيد:
تنطبق النتائج التي توصلنا إليها عند دراسة الماء وكبريتيد الكالسيوم ينطبق على كل المركبات المعروفة, فهي كلها تنتج عن اتحاد العناصر مع بعضها بنسب وزنية ثابتة, وهذا ما وجده العلماء نتيجة للأبحاث والدراسات. ولو حصلنا الآن على عينات نقية من ملح الطعام سواء من تبخير ماء البحر الميت. أو تبخير ماء البحر المتوسط, أو من التفاعل:
NaOH + HCl
NaCl + H2O
وحللناها لوجدنا أنها تتكون من اتحاد i23i غم صوديوم مع i35.5i غم من الكلور تقريباً وينتج عن ذلك i58.5iغم من الملح تقريباً. وهذه النسبة أو أحد أجزائها أو مضاعفاتها هي التي نحصل عليها دائماً وذلك حسب كمية عينة الملح المدروسة صغيرة أم كبيرة.
اكتشف العلماء هذه الحقيقة في مطلع القرن التاسع عشر وتوصلوا نتيجة هذا الاكتشاف إلى قانونين هامين أصبحا الآن في عداد المسلمات وهما:
أولاً: قانون حفظ الكتلة Law of Conservation of mass
ثانياً: قانون النسب الثابتة Law of Definite Proportions
أولاً: قانون حفظ الكتلة Law of Conservation of mass
عند حدوث التغيرات الكيميائية فإن مجموع كتل المواد المتفاعلة يساوي مجموع كتل المواد بعد نهاية التفاعل.
مثال: عند تفاعل i3i غرامات من الكربون معi8i غرامات من الأوكسجين ينتج i11i غم من ثاني أوكسيد الكربون.
ولو تفاعل i3i غرامات من C مع i15i غرامات من O2 فإنه ينتج عن ذلك i11i غم CO2 وبقي i7i غرامات من O2 كما هي دون تغيير , أي أن كمية الأوكسجين الزائد بقيت كما هي من حيث الكتلة والنوع.
سؤال: اكتب جملة بلغتك الخاصة تعبر عن فهمك لقانون حفظ الكتلة
الإجابة:
" عند حدوث التغيرات الكيميائية يبقى مجموع كتل المواد قبل التفاعل وبعده ثابتاً دون تغيير
raneem noor
أنواع الإشعاع
توجد ثلاثة أنواع من الإشعاع النشط: جسيمات ألفا، وكان بكويريل أول من تعرف عليها؛ وجسيمات بيتا التي تعرف عليها النيوزيلندي إرنست رذرفورد؛ وأشعة جاما التي تعرف عليها الزوجان الفرنسيان ماري وبيير كوري.
جسيمات ألفا. تحمل شحنات كهربائية موجبة. ويتركب جسيم ألفا من بروتونين ونيوترونين، أي أنه يماثل نواة ذرة الهيليوم. تنطلق جسيمات ألفا بطاقات عالية، ولكنها سرعان ما تفقدها عند مرورها في المادة. وبمقدور ورقتين من أوراق هذه الموسوعة إيقافها.
جُسَيّم ألفا
جسيم ذو شحنة موجبة، وطاقة عالية تطلقه نواة ذرة مشعة، عندما تخضع لتحوُّل نووي. ويُعد جسيم ألفا مطابقًا لنواة ذرة الهيليوم. ويتألف من بروتونين وإلكترونين يرتبطان معًا ارتباطًا وثيقًا. ويزن جُسيم ألفا أكثر من جسيم بيتا بـ 7,000 مرة. وينتقل جسيم ألفا لمسافة قصيرة بسبب كتلته الضخمة. فعلى سبيل المثال، ينتقل جسيم ألفا النموذجي إلى مسافة لا تزيد عن 5سم في الهواء.
جسيمات بيتا.
وهي إلكترونات. تطلق بعض النوي المشعة إلكترونات عادية تحمل شحنات كهربائية سالبة. لكن البعض الآخر يطلق بوزيترونات وهي إلكترونات ذات شحنة موجبة. وتنتقل جسيمات بيتا بسرعة تقارب سرعة الضوء ويستطيع بعضها أن ينفذ خلال 13ملم من الخشب.
جُسَيّم بَيْتا إلكترون يتولد عن نواة ذرة إشعاعية أثناء تعرضها لعملية تحوّل نووي. ومعظم جسيمات بيتا ذات شحنات سالبة تتكون عندما يتحول نيوترون إلى بروتون. وبعضها بوزيترونات وهي إلكترونات ذات شحنة موجبة تنتج عن تحول البروتون. وجسيمات بيتا بالغة الصغر، إذ تعادل فقط 1/1,840 من جسم البروتون. وتمكنها طاقتها العالية من الانطلاق في الجو لمسافات بعيدة واختراق المواد الصلبة التي يعادل سمكها عدة مليمترات. ويقيس العلماء طاقة جسيمات بيتا بحساب المدى الذي تأخذه في اختراق مواد معينة.
أشعة جاما.
أشعة غير مشحونة كهربائيًا. وتشبه هذه الأشعة الأشعة السينية، إلا أنها تكون في الغالب ذات طولٍ موجي أصغر. وهذه الأشعة هي فوتونات (جسيمات الإشعاع الكهرومغنطيسي)، وتنتقل بسرعة الضوء. تخترق أشعة جاما الأجسام بدرجةٍ أكبر من جسيمات ألفا أو بيتا.
أشعة جاما شكل من أشكال الإشعاع الكهرومغنطيسي يشبه الأشعة السينية. ولأشعة جاما طول موجي أقصر من الطول الموجي للأشعة السينية،كما أنهما يختلفان في أصلهما أيضًا. تنتج الأشعة السينية خلال عدة عمليات مختلفة مرتبطة بالإلكترونات التي تدور حول نواة الذرة بينما تنبعث أشعة جاما من النواة نفسها.
تنبعث من نوى اليورانيوم وعناصر إشعاعية طبيعية أخرى جسيمات ألفا أو بيتا مع انبعاث أشعة جاما في الوقت نفسه، وتتحول العناصر بذلك إلى عناصر جديدة. ويمكن أن تنبعث أشعة جاما بمفردها من خلال ما يعرف باسم التحولات التماكبية. ولا يغير بث أشعة جاما تركيب النواة. وبدلاً من ذلك، تفقد جزءًا محدودًا من الطاقة.
ربما تحمل أشعة جاما ملايين الإلكترون فولت من الطاقة وباستطاعتها اختراق أنواع عديدة من المواد. ولكن باستطاعة بعض المواد امتصاص أشعة جاما. على سبيل المثال، تستطيع شريحة من الحديد سمكها 1,3سم امتصاص 50% من أشعة جاما ذات مليون إلكترون فولت. وتعادل هذه القدرة الامتصاصية قدرة 10سم من المياه أو 0,65سم من الرصاص.
تفقد أشعة جاما الطاقة عندما تصطدم مع الذرات خلال مرورها عبر المادة. وخلال هذه الاصطدامات، ربما تفصل أشعة جاما الإلكترونات من الذرات الأم. تُدعى هذه العملية التأين (التحويل إلى أيونات)، لأنها تحول الذرة المتعادلة إلى ذرة مشحونة تدعى الأيون. يُدعى الإلكترون الحر والذرة المشحونة الموجبة الأيون المزدوج. وقد تنبعث أشعة جاما ذات الطاقة العالية من المادة الموجودة بقرب النواة، وذلك بتكوين زوج من الإلكترونات يسميان البوزيترون (جسم موجب ذو كتلة تعادل كتلة الإلكترون) والنقترون (إلكترون عادي ذو شحنة سالبة). وفي هذه العملية يتم امتصاص أشعة جاما. وعملية إيجاد زوج الإلكترونات هذه بوساطة أشعة جاما هي عكس ما يحدث عندما يتحد النيوترون والبوزيترون.فعندما يتحد هذان الجسيمان فإنهما يتلاشيان وينتج عن ذلك شعاعان من أشعة جاما ذوا طاقة متساوية. وتدعى هذه العملية الفناء، وغالبًا ما تدعى أشعة جاما الناتجة أشعة الفناء.
تقذف كميات ضئيلة من أشعة جاما الصادرة عن المواد المشعة الطبيعية في الصخور والتربة أجسامنا بشكل ثابت. تمر بعض هذه المواد يوميًا إلى أجسامنا عبر الهواء الذي نتنفسه والماء الذي نشربه. تُنتج أشعة جاما التي تمر داخل الجسم تأيّنًا في الأنسجة. وإذا كانت بكميات كبيرة فإنها تضر خلايا الجسم. ورغم خطورتها فقد تكون ذات فائدة في معالجة الأورام الحميدة والخبيثة.كما أنها تستخدم أيضًا في الكشف عن صدع الفلزات وحفظ الأطعمة.
شوق المرشدي
توجد ثلاثة أنواع من الإشعاع النشط: جسيمات ألفا، وكان بكويريل أول من تعرف عليها؛ وجسيمات بيتا التي تعرف عليها النيوزيلندي إرنست رذرفورد؛ وأشعة جاما التي تعرف عليها الزوجان الفرنسيان ماري وبيير كوري.
جسيمات ألفا. تحمل شحنات كهربائية موجبة. ويتركب جسيم ألفا من بروتونين ونيوترونين، أي أنه يماثل نواة ذرة الهيليوم. تنطلق جسيمات ألفا بطاقات عالية، ولكنها سرعان ما تفقدها عند مرورها في المادة. وبمقدور ورقتين من أوراق هذه الموسوعة إيقافها.
جُسَيّم ألفا
جسيم ذو شحنة موجبة، وطاقة عالية تطلقه نواة ذرة مشعة، عندما تخضع لتحوُّل نووي. ويُعد جسيم ألفا مطابقًا لنواة ذرة الهيليوم. ويتألف من بروتونين وإلكترونين يرتبطان معًا ارتباطًا وثيقًا. ويزن جُسيم ألفا أكثر من جسيم بيتا بـ 7,000 مرة. وينتقل جسيم ألفا لمسافة قصيرة بسبب كتلته الضخمة. فعلى سبيل المثال، ينتقل جسيم ألفا النموذجي إلى مسافة لا تزيد عن 5سم في الهواء.
جسيمات بيتا.
وهي إلكترونات. تطلق بعض النوي المشعة إلكترونات عادية تحمل شحنات كهربائية سالبة. لكن البعض الآخر يطلق بوزيترونات وهي إلكترونات ذات شحنة موجبة. وتنتقل جسيمات بيتا بسرعة تقارب سرعة الضوء ويستطيع بعضها أن ينفذ خلال 13ملم من الخشب.
جُسَيّم بَيْتا إلكترون يتولد عن نواة ذرة إشعاعية أثناء تعرضها لعملية تحوّل نووي. ومعظم جسيمات بيتا ذات شحنات سالبة تتكون عندما يتحول نيوترون إلى بروتون. وبعضها بوزيترونات وهي إلكترونات ذات شحنة موجبة تنتج عن تحول البروتون. وجسيمات بيتا بالغة الصغر، إذ تعادل فقط 1/1,840 من جسم البروتون. وتمكنها طاقتها العالية من الانطلاق في الجو لمسافات بعيدة واختراق المواد الصلبة التي يعادل سمكها عدة مليمترات. ويقيس العلماء طاقة جسيمات بيتا بحساب المدى الذي تأخذه في اختراق مواد معينة.
أشعة جاما.
أشعة غير مشحونة كهربائيًا. وتشبه هذه الأشعة الأشعة السينية، إلا أنها تكون في الغالب ذات طولٍ موجي أصغر. وهذه الأشعة هي فوتونات (جسيمات الإشعاع الكهرومغنطيسي)، وتنتقل بسرعة الضوء. تخترق أشعة جاما الأجسام بدرجةٍ أكبر من جسيمات ألفا أو بيتا.
أشعة جاما شكل من أشكال الإشعاع الكهرومغنطيسي يشبه الأشعة السينية. ولأشعة جاما طول موجي أقصر من الطول الموجي للأشعة السينية،كما أنهما يختلفان في أصلهما أيضًا. تنتج الأشعة السينية خلال عدة عمليات مختلفة مرتبطة بالإلكترونات التي تدور حول نواة الذرة بينما تنبعث أشعة جاما من النواة نفسها.
تنبعث من نوى اليورانيوم وعناصر إشعاعية طبيعية أخرى جسيمات ألفا أو بيتا مع انبعاث أشعة جاما في الوقت نفسه، وتتحول العناصر بذلك إلى عناصر جديدة. ويمكن أن تنبعث أشعة جاما بمفردها من خلال ما يعرف باسم التحولات التماكبية. ولا يغير بث أشعة جاما تركيب النواة. وبدلاً من ذلك، تفقد جزءًا محدودًا من الطاقة.
ربما تحمل أشعة جاما ملايين الإلكترون فولت من الطاقة وباستطاعتها اختراق أنواع عديدة من المواد. ولكن باستطاعة بعض المواد امتصاص أشعة جاما. على سبيل المثال، تستطيع شريحة من الحديد سمكها 1,3سم امتصاص 50% من أشعة جاما ذات مليون إلكترون فولت. وتعادل هذه القدرة الامتصاصية قدرة 10سم من المياه أو 0,65سم من الرصاص.
تفقد أشعة جاما الطاقة عندما تصطدم مع الذرات خلال مرورها عبر المادة. وخلال هذه الاصطدامات، ربما تفصل أشعة جاما الإلكترونات من الذرات الأم. تُدعى هذه العملية التأين (التحويل إلى أيونات)، لأنها تحول الذرة المتعادلة إلى ذرة مشحونة تدعى الأيون. يُدعى الإلكترون الحر والذرة المشحونة الموجبة الأيون المزدوج. وقد تنبعث أشعة جاما ذات الطاقة العالية من المادة الموجودة بقرب النواة، وذلك بتكوين زوج من الإلكترونات يسميان البوزيترون (جسم موجب ذو كتلة تعادل كتلة الإلكترون) والنقترون (إلكترون عادي ذو شحنة سالبة). وفي هذه العملية يتم امتصاص أشعة جاما. وعملية إيجاد زوج الإلكترونات هذه بوساطة أشعة جاما هي عكس ما يحدث عندما يتحد النيوترون والبوزيترون.فعندما يتحد هذان الجسيمان فإنهما يتلاشيان وينتج عن ذلك شعاعان من أشعة جاما ذوا طاقة متساوية. وتدعى هذه العملية الفناء، وغالبًا ما تدعى أشعة جاما الناتجة أشعة الفناء.
تقذف كميات ضئيلة من أشعة جاما الصادرة عن المواد المشعة الطبيعية في الصخور والتربة أجسامنا بشكل ثابت. تمر بعض هذه المواد يوميًا إلى أجسامنا عبر الهواء الذي نتنفسه والماء الذي نشربه. تُنتج أشعة جاما التي تمر داخل الجسم تأيّنًا في الأنسجة. وإذا كانت بكميات كبيرة فإنها تضر خلايا الجسم. ورغم خطورتها فقد تكون ذات فائدة في معالجة الأورام الحميدة والخبيثة.كما أنها تستخدم أيضًا في الكشف عن صدع الفلزات وحفظ الأطعمة.
شوق المرشدي
لنظائر Isotopes
تختلف العناصر فيما بينها في العدد الذري ( عدد البروتونات ) إلا أن هنالك عناصر تتشابه في العدد الذري وتختلف فيما بينها في العدد الكتلي وتعرف هذه العناصر بالنظائر.
وتعني كلمة نظير ( المكان نفسه ) أي أن لها نفس المكان في الجدول الدوري ، إذ أنها لا تختلف فيما بينها في العدد الذري.
وعادة ً ما يتم التعبيرعن النظائر بدلالة كتلها الذرية ، لأن أعدادها الذرية ثابتة .
مثال 1 :
للهيدروجين ( العدد الذري للهيدروجين = 1 ) ثلاثة نظائر مشهورة ، تشترك جميعها في احتوائها على نفس العدد من البروتونات (العدد الذري) . وتختلف فيما بينها في عدد النيوترونات (العدد الكتلي) .
يسمى كل نظير نسبة إلى عدده الكتلي :
ـ يسمى النظير الأول للهيدروجين ( هيدروجين - 1 ) .
ـ يسمى النظير الثاني للهيدروجين ( هيدروجين - 2 ) أو الديوتيريوم .
ـ يسمى النظير الثالث للهيدروجين ( هيدروجين - 3 ) أو التريتيوم .
شوق المرشدي
تختلف العناصر فيما بينها في العدد الذري ( عدد البروتونات ) إلا أن هنالك عناصر تتشابه في العدد الذري وتختلف فيما بينها في العدد الكتلي وتعرف هذه العناصر بالنظائر.
وتعني كلمة نظير ( المكان نفسه ) أي أن لها نفس المكان في الجدول الدوري ، إذ أنها لا تختلف فيما بينها في العدد الذري.
وعادة ً ما يتم التعبيرعن النظائر بدلالة كتلها الذرية ، لأن أعدادها الذرية ثابتة .
مثال 1 :
للهيدروجين ( العدد الذري للهيدروجين = 1 ) ثلاثة نظائر مشهورة ، تشترك جميعها في احتوائها على نفس العدد من البروتونات (العدد الذري) . وتختلف فيما بينها في عدد النيوترونات (العدد الكتلي) .
يسمى كل نظير نسبة إلى عدده الكتلي :
ـ يسمى النظير الأول للهيدروجين ( هيدروجين - 1 ) .
ـ يسمى النظير الثاني للهيدروجين ( هيدروجين - 2 ) أو الديوتيريوم .
ـ يسمى النظير الثالث للهيدروجين ( هيدروجين - 3 ) أو التريتيوم .
شوق المرشدي
لتحلل الاشعاعي Radioactive decay
اكتشف العالم الفرنسي بيكوريل عام 1896م أن بعض املاح اليورانيوم تصدر اشعة بصورة تلقائية لا تعتمد على حالة اليورانيوم الفيزيائية والكيميائية ، ولقد اطلقت مدام كوري على هذه الظاهرة ( والتي تعرف احياناً باسم التفكك أو الاضمحلال الاشعاعي Radioactive decay ) اسم النشاط الاشعاعي الطبيعي . ولقد تبين فيما بعد أن هناك ثلاثة أنواع من الاشعاعات التي يمكن أن تصدر بهذه الطريقة ، وأن مصدر هذه الاشعاعات هو نواة الذرة . ولقد تعرف رذرفورد على النوع الأول من
هذه الأشعاعات وبين أنه عبارة عن نواة الهيليوم والتي تتكون من بروتونين ونيوترونين واطلق عليه اسم أشعة ألفا Alpha ray أما النوع الثاني فقد تعرف عليه بيكوريل نفسه وبين أنه عبارة عن إلكترونات سريعة واطلق عليه اسم أشعة بيتا Beta ray وبين فيلارد أن النوع الثالث عبارة عن أشعة كهرومغناطيسية ذات تردد عال واطلق عليه اسم أشعة جاما Gamma ray ولقد لعبت الابحاث التي اجريت على هذه الظاهرة دوراً كبيراً في تطور الفيزياء الحديثة .
وتنتج هذه الاشعاعات كما ذكرنا من النواة وذلك نتيجة عدم استقرارها بسبب عدم التناسب بين عدد البروتونات والنيترونات بداخلها مما يجعلها تتفكك إلى عناصر أخف وأكثراستقراراً . ويحدث التحلل النووي عادة في أنوية العناصر الثقيلة ( الاثقل من الرصاص) وذلك نتيجة انخفاض طاقة الترابط بين أنويتها
التحلل الاشعاعي Radioactive decay
كما ذكرنا سابقاً بأن بعض أنوية العناصر تكون غير مستقرة وبالتالي فإنها تسعى لتكون مستقرة وذلك من خلال تحللها والتخلص من جزء من مكوناتها . وهذا التحلل التلقائي مرهون بكون الطاقة الكلية للنظام النهائي (النواة الجديدة ) أقل من الطاقة الكلية للنظان الابتدائي (النواة الاصلية) ومتى ما توفر هذا الامر فحينئذ تكون هناك احتمالية حدوث لهذا التحلل وكلما كان الفرق بين طاقتي النظامين (الابتدائي والجديد) كبيراً كلما كانت هناك اختمالية أكبر لحدوث هذا التحول التلقائي للنواة .
نشاط النواة الاشعاعي .
اثناء دراسة الانشطة الاشعاعية للانوية الغير مستقرة وجد أن هناك ثلاثة أنواع للتحلل والتي تختلف باختلاف طبيعتها وقدراتها النفاذية وهي :
1 – أشعة ألفا ( Alpha decay) : عبارة عن أنوية لذرات الهيليوم وتتمتع نفاذ صغيرة .
2 – اشعة بيتا (beta decay) : عبارة عن إلتكترونات ذات شحنة موجبة أو سالبة وتتمتع بقدرات نفاذ أكبر من أشعة ألفا .
3 – أشعة جاما ( gama decay) : عبارة عن اشعة كهرومغناطيسية وهي ذات طاقة عالية ولها قرة نفاذ عالية جداً .
الانحلال الاشعاعي :
جميع أنماط الانحلال الاشعاعي تعتمد في تحللها على عامل الزمن . ولدراسة هذه المسألة ينبغ التعرف على المصطلحات التالية :
1 – تسمى النواة قبل التحلل بـ النواة الام ( parent)
2 – تسمى النواة بعد التحلل بـ النواة الوليدة ( deugter)
3 – تسمى أي من مكونات النواة (بروتون أو نيترون) بـ النويدة (nuclei)
4 – عندما تكون النواة الوليدة غير مستقرة فإنها تتحلل ايضاً وسمى هذا النوع من النظام الذي يحوي عدة اجيال من الانوى الوليدة الغير مستقرة بـ (سلسلة الانحلال الاشعاعي )
وبعد يمكننا القول بأن ظاهرة الانحلال الاشعاعي هي ظاهرة ذات طبيعة احصائية ولذا فإنه من المستحيل تحديد زمن حدوث انحلال لنويدة معينة أثناء عملية التفكك الاشعاعي لان العملية عتهتمد على الاحتمالات .
ثابت التفكك decay constant λ
يعرف ثابت التفكك بأنه احتمال تفكك أو اضمحلال نويدة عنصر في وحدة الزمن (ثانية واحدة)
خصائص ثابت التفكك :
1 – ثابت التفكك (λ) هو مقدار ثابت لجميع نويدات العتصر الواحد ولا يعتمد على الظروف الخارجية كالحرارة والرطوبة والضغط وغيرها وه عتمد فقط على تركيب النواة للعنصر .
2 – ان قيمة ثابت التفكك لا يعتمد على الزمن بمعنى أنه لا يعتمد على عمر النواة المشعة .
إذاً λ تمثل احتمال تفكك النويدة في الثانية الواحدة ويكون بالتالي احتمال تفكك النواة خلال فترة زمنية dt هو : λdt
وإذا كان لدينا عدد من الانوية عددها (N) فإن عدد الانوية التي سوف تتحلل خلال فترة dt هو :
dN = - N λdt
واشارة السالب تشير إى أن عد الانوية الموجودة يتناقص بسبب عملية التفكك . ويمكن كتابة المعادلة السابقة بالشكل التالي :
dNN = - λdt
وباجراء التكامل على الطرفين :
وهذه المعادلة تشير إلى أن تناقص عدد الذرات سوف يكون بشكل اسي مع الزمن
النشاطية ( Activity (A
تعرف النشاطية لعنصر بأنه عدد الذرات التي تتحلل خلال ثانية واحدة ويمكن العبير عنه بالمعادلة التالية :
تقاس النشاطية بةحدة الكوري ( C) وهذه الوحدة تعرف على أنها نشاط كمية من المادة تتفكك بمعدل
وهناك وحدة تستخدم في النظام (SI) تعرف بـ البكيريل (Bq)
عمر النصف ( half-life)
يعرف عمر النصف بأنه الزمن اللازم لتحلل نصف كمية المادة الاصلية
جميع العناصر المشعة تنتمي إلى واحدة من ثلاث سلاسل تسمى كل واحدة منها سلسلة النشاط الإشعاعي ، تبدأ السلسلة الأولى بنظير اليورانيوم (238) ، والثانية بنظير اليورانيوم (235) ، بينما تبدأ الثالثة بنظير الثوريوم (232) ، وتوضح هذه السلاسل مراحل تحلل العنصر المشع.
الشكل الآتي يوضح سلسلة تحلل اليورانيوم (238) إلى رصاص (206) :
العدد الكتلي
العدد الذري
سلسلة تحلل اليورانيوم (238) الى رصاص (206) .
أولى خطوات هذه السلسلة تتضمن تحول نظير اليورانيوم (238) إلى نظير الثوريوم (234) وينتج بفعل هذا الانحلال انطلاق دقائق ألفا ، ويتم تمثيل هذا التفاعل النووي على النحو التالي:
يتم تمثيل دقائق ألفا الناتجة عن التفاعل بأنوية الهيليوم .
يسمى هذا النوع من التفاعلات والتي يظهر فيها كل من العدد الذري والعدد الكتلي وينتج عنها عناصر جديدة بالتفاعلات النووية.
وفي الخطوة الثانية يتحول الثوريوم إلى نظير البروتاكتينيوم مطلقاً دقيقة بيتا .
ويتم تحول الثوريوم وفق المعادلة النووية التالية :
الرمز يمثل الكترون ( بيتا ) مصدره النواة ، شحنته (-1) وكتلته ( صفر ) .
الخطوة الثالثة تتمثل في تحول البروتاكتينيوم إلى نظير اليورانيوم مطلقاً من جديد دقائق بيتا وذلك وفق المعادلة النووية التالية:
تمثل الخطوة الرابعة تحول نظير اليورانيوم إلى نظير الثوريوم وتنطلق دقائق ألفا بفعل هذا التحول :
ثم يعود الثوريوم في الخطوة الخامسة للتحول إلى نظير الراديوم وتنطلق دقائق ألفا :
والآن يمكنك ملاحظة سبب وجود الراديوم في خام اليورانيوم .
وفي الخطوة السادسة يتحول الراديوم إلى نظير الرادون :
ثم يتحول الرادون في الخطوة السابعة إلى نظير البولونيوم :
وهكذا تستمر سلسلة التحولات ، وينتج في كل مرحلة منها نظير غير مستقر إلى أن يصل اليورانيوم في تحللاته إلى نظير الرصاص (206) المستقر في سلسلة من (14) خطوة .
يسمى هذا النوع من السلاسل بسلسلة النشاط الإشعاعي Radioactive Series أو سلسلة التحلل Decay Series
سرعة التحلل الإشعاعي Rate of Radioactive Decay
تتحلل أنوية العناصر غير المستقرة بسرعات مختلفة ، فبعضها يحتاج لملايين السنين لكي يتحلل ، والبعض الآخر بحاجة لثوان لفعل ذلك.
تسمى الفترة الزمنية اللازمة لتحويل كتلة معينة من العنصر غير المستقر إلى نصف تلك الكتلة بعمر النصف
(half – life ) ويرمز لها بالرمز ( t 1/2 ) .
ولكل نظير غير مستقر عمر نصف محدد خاص به ، فعلى سبيل المثال يبلغ عمر النصف للبزموث (214) (20) دقيقة
( t 1/2 = 20 mi ) ، وهذا يعني أنه لو بدأنا بـ (10) غرام من البزموث ، سيبقى (5) غرام منه بعد مرور (20) دقيقة ، ونحتاج لـ (20) دقيقة أخرى لتحويل الـ (5) غرام من البزموث إلى (2.5) غرام ... وهكذا .
ولملاحظة سرعة كل خطوة والدقائق والأشعة التي تنتج من كل خطوة من خطوات سلسلة النشاط الإشعاعي ، انظر للمخطط التالي :
الزمن المعطى بين الخطوات يمثل فترة نصف العمر :
s : ثانية ، mi : دقيقة ، d : يوم ، m : شهر ، Y : سنة
raneem noor
اكتشف العالم الفرنسي بيكوريل عام 1896م أن بعض املاح اليورانيوم تصدر اشعة بصورة تلقائية لا تعتمد على حالة اليورانيوم الفيزيائية والكيميائية ، ولقد اطلقت مدام كوري على هذه الظاهرة ( والتي تعرف احياناً باسم التفكك أو الاضمحلال الاشعاعي Radioactive decay ) اسم النشاط الاشعاعي الطبيعي . ولقد تبين فيما بعد أن هناك ثلاثة أنواع من الاشعاعات التي يمكن أن تصدر بهذه الطريقة ، وأن مصدر هذه الاشعاعات هو نواة الذرة . ولقد تعرف رذرفورد على النوع الأول من
هذه الأشعاعات وبين أنه عبارة عن نواة الهيليوم والتي تتكون من بروتونين ونيوترونين واطلق عليه اسم أشعة ألفا Alpha ray أما النوع الثاني فقد تعرف عليه بيكوريل نفسه وبين أنه عبارة عن إلكترونات سريعة واطلق عليه اسم أشعة بيتا Beta ray وبين فيلارد أن النوع الثالث عبارة عن أشعة كهرومغناطيسية ذات تردد عال واطلق عليه اسم أشعة جاما Gamma ray ولقد لعبت الابحاث التي اجريت على هذه الظاهرة دوراً كبيراً في تطور الفيزياء الحديثة .
وتنتج هذه الاشعاعات كما ذكرنا من النواة وذلك نتيجة عدم استقرارها بسبب عدم التناسب بين عدد البروتونات والنيترونات بداخلها مما يجعلها تتفكك إلى عناصر أخف وأكثراستقراراً . ويحدث التحلل النووي عادة في أنوية العناصر الثقيلة ( الاثقل من الرصاص) وذلك نتيجة انخفاض طاقة الترابط بين أنويتها
التحلل الاشعاعي Radioactive decay
كما ذكرنا سابقاً بأن بعض أنوية العناصر تكون غير مستقرة وبالتالي فإنها تسعى لتكون مستقرة وذلك من خلال تحللها والتخلص من جزء من مكوناتها . وهذا التحلل التلقائي مرهون بكون الطاقة الكلية للنظام النهائي (النواة الجديدة ) أقل من الطاقة الكلية للنظان الابتدائي (النواة الاصلية) ومتى ما توفر هذا الامر فحينئذ تكون هناك احتمالية حدوث لهذا التحلل وكلما كان الفرق بين طاقتي النظامين (الابتدائي والجديد) كبيراً كلما كانت هناك اختمالية أكبر لحدوث هذا التحول التلقائي للنواة .
نشاط النواة الاشعاعي .
اثناء دراسة الانشطة الاشعاعية للانوية الغير مستقرة وجد أن هناك ثلاثة أنواع للتحلل والتي تختلف باختلاف طبيعتها وقدراتها النفاذية وهي :
1 – أشعة ألفا ( Alpha decay) : عبارة عن أنوية لذرات الهيليوم وتتمتع نفاذ صغيرة .
2 – اشعة بيتا (beta decay) : عبارة عن إلتكترونات ذات شحنة موجبة أو سالبة وتتمتع بقدرات نفاذ أكبر من أشعة ألفا .
3 – أشعة جاما ( gama decay) : عبارة عن اشعة كهرومغناطيسية وهي ذات طاقة عالية ولها قرة نفاذ عالية جداً .
الانحلال الاشعاعي :
جميع أنماط الانحلال الاشعاعي تعتمد في تحللها على عامل الزمن . ولدراسة هذه المسألة ينبغ التعرف على المصطلحات التالية :
1 – تسمى النواة قبل التحلل بـ النواة الام ( parent)
2 – تسمى النواة بعد التحلل بـ النواة الوليدة ( deugter)
3 – تسمى أي من مكونات النواة (بروتون أو نيترون) بـ النويدة (nuclei)
4 – عندما تكون النواة الوليدة غير مستقرة فإنها تتحلل ايضاً وسمى هذا النوع من النظام الذي يحوي عدة اجيال من الانوى الوليدة الغير مستقرة بـ (سلسلة الانحلال الاشعاعي )
وبعد يمكننا القول بأن ظاهرة الانحلال الاشعاعي هي ظاهرة ذات طبيعة احصائية ولذا فإنه من المستحيل تحديد زمن حدوث انحلال لنويدة معينة أثناء عملية التفكك الاشعاعي لان العملية عتهتمد على الاحتمالات .
ثابت التفكك decay constant λ
يعرف ثابت التفكك بأنه احتمال تفكك أو اضمحلال نويدة عنصر في وحدة الزمن (ثانية واحدة)
خصائص ثابت التفكك :
1 – ثابت التفكك (λ) هو مقدار ثابت لجميع نويدات العتصر الواحد ولا يعتمد على الظروف الخارجية كالحرارة والرطوبة والضغط وغيرها وه عتمد فقط على تركيب النواة للعنصر .
2 – ان قيمة ثابت التفكك لا يعتمد على الزمن بمعنى أنه لا يعتمد على عمر النواة المشعة .
إذاً λ تمثل احتمال تفكك النويدة في الثانية الواحدة ويكون بالتالي احتمال تفكك النواة خلال فترة زمنية dt هو : λdt
وإذا كان لدينا عدد من الانوية عددها (N) فإن عدد الانوية التي سوف تتحلل خلال فترة dt هو :
dN = - N λdt
واشارة السالب تشير إى أن عد الانوية الموجودة يتناقص بسبب عملية التفكك . ويمكن كتابة المعادلة السابقة بالشكل التالي :
dNN = - λdt
وباجراء التكامل على الطرفين :
وهذه المعادلة تشير إلى أن تناقص عدد الذرات سوف يكون بشكل اسي مع الزمن
النشاطية ( Activity (A
تعرف النشاطية لعنصر بأنه عدد الذرات التي تتحلل خلال ثانية واحدة ويمكن العبير عنه بالمعادلة التالية :
تقاس النشاطية بةحدة الكوري ( C) وهذه الوحدة تعرف على أنها نشاط كمية من المادة تتفكك بمعدل
وهناك وحدة تستخدم في النظام (SI) تعرف بـ البكيريل (Bq)
عمر النصف ( half-life)
يعرف عمر النصف بأنه الزمن اللازم لتحلل نصف كمية المادة الاصلية
جميع العناصر المشعة تنتمي إلى واحدة من ثلاث سلاسل تسمى كل واحدة منها سلسلة النشاط الإشعاعي ، تبدأ السلسلة الأولى بنظير اليورانيوم (238) ، والثانية بنظير اليورانيوم (235) ، بينما تبدأ الثالثة بنظير الثوريوم (232) ، وتوضح هذه السلاسل مراحل تحلل العنصر المشع.
الشكل الآتي يوضح سلسلة تحلل اليورانيوم (238) إلى رصاص (206) :
العدد الكتلي
العدد الذري
سلسلة تحلل اليورانيوم (238) الى رصاص (206) .
أولى خطوات هذه السلسلة تتضمن تحول نظير اليورانيوم (238) إلى نظير الثوريوم (234) وينتج بفعل هذا الانحلال انطلاق دقائق ألفا ، ويتم تمثيل هذا التفاعل النووي على النحو التالي:
يتم تمثيل دقائق ألفا الناتجة عن التفاعل بأنوية الهيليوم .
يسمى هذا النوع من التفاعلات والتي يظهر فيها كل من العدد الذري والعدد الكتلي وينتج عنها عناصر جديدة بالتفاعلات النووية.
وفي الخطوة الثانية يتحول الثوريوم إلى نظير البروتاكتينيوم مطلقاً دقيقة بيتا .
ويتم تحول الثوريوم وفق المعادلة النووية التالية :
الرمز يمثل الكترون ( بيتا ) مصدره النواة ، شحنته (-1) وكتلته ( صفر ) .
الخطوة الثالثة تتمثل في تحول البروتاكتينيوم إلى نظير اليورانيوم مطلقاً من جديد دقائق بيتا وذلك وفق المعادلة النووية التالية:
تمثل الخطوة الرابعة تحول نظير اليورانيوم إلى نظير الثوريوم وتنطلق دقائق ألفا بفعل هذا التحول :
ثم يعود الثوريوم في الخطوة الخامسة للتحول إلى نظير الراديوم وتنطلق دقائق ألفا :
والآن يمكنك ملاحظة سبب وجود الراديوم في خام اليورانيوم .
وفي الخطوة السادسة يتحول الراديوم إلى نظير الرادون :
ثم يتحول الرادون في الخطوة السابعة إلى نظير البولونيوم :
وهكذا تستمر سلسلة التحولات ، وينتج في كل مرحلة منها نظير غير مستقر إلى أن يصل اليورانيوم في تحللاته إلى نظير الرصاص (206) المستقر في سلسلة من (14) خطوة .
يسمى هذا النوع من السلاسل بسلسلة النشاط الإشعاعي Radioactive Series أو سلسلة التحلل Decay Series
سرعة التحلل الإشعاعي Rate of Radioactive Decay
تتحلل أنوية العناصر غير المستقرة بسرعات مختلفة ، فبعضها يحتاج لملايين السنين لكي يتحلل ، والبعض الآخر بحاجة لثوان لفعل ذلك.
تسمى الفترة الزمنية اللازمة لتحويل كتلة معينة من العنصر غير المستقر إلى نصف تلك الكتلة بعمر النصف
(half – life ) ويرمز لها بالرمز ( t 1/2 ) .
ولكل نظير غير مستقر عمر نصف محدد خاص به ، فعلى سبيل المثال يبلغ عمر النصف للبزموث (214) (20) دقيقة
( t 1/2 = 20 mi ) ، وهذا يعني أنه لو بدأنا بـ (10) غرام من البزموث ، سيبقى (5) غرام منه بعد مرور (20) دقيقة ، ونحتاج لـ (20) دقيقة أخرى لتحويل الـ (5) غرام من البزموث إلى (2.5) غرام ... وهكذا .
ولملاحظة سرعة كل خطوة والدقائق والأشعة التي تنتج من كل خطوة من خطوات سلسلة النشاط الإشعاعي ، انظر للمخطط التالي :
الزمن المعطى بين الخطوات يمثل فترة نصف العمر :
s : ثانية ، mi : دقيقة ، d : يوم ، m : شهر ، Y : سنة
raneem noor
انون النسب الثابتة أو ما يعرف بقانون التركيب المحدد (الثابت)
أن كل مركب كيمـيائي مهما أختلف تحضيره ، فإنه يتـركب من عـناصره نفسها متحدة مع بعضها البعض بنسب ثابتة .
وقد توصل إلى هذا القانون (بروست) الفرنسي الذي أكمل دراسات أنطوان لافوازييه بعد وفاته وتبين له’ أن المركبات تحتوي على نسب ثابتة من العناصر المكونة لها’ ولاتتغير هذه النسب مهما اختلفت طرق تحضير المركب.
فمثلا ملح الطعام النقي سواء حصلنا عليه من مياه البحار أو تم تحضيره من تفاعل كميائي’ فإنه يحتوي دائما على 39,3% من كتلته الصوديوم و60,7% من كتلته كلور
مثال آخر جميع عينات الماء النقي تحتوي على عنصري الهـيدروجين و الأكسـجين بنسـبة كتلة جزء من الهيدروجين إلى ثمانية أجزاء من أكسـجين ( فمثلا:1 جم من الهيدروجين إلى 8 جم من الأكسجين) كذلك، عندما يسمح للهيدروجين بالتفاعل مع الأكسجين لينتج الماء ، فأن الكمـيات النسـبية لكل من الهيدروجين و الأكسـجين التي تتفـاعل تبــقى نفـسها دائـما ، فـكلما تفاعل1جم من الهيدروجين يلاحظ أنه دائما يستهلك فقط 8 جم من الأكسجين ، حتى لـو توافـرت كمـية أكـبر مـن الأكسجين فمثلا إذا خلط 2جم من الهيدروجين مع 8 جم من الأكسجين ، و أشـعل الخلـيط يتكـون 9 جم من المـاء ويبقى 1 جم من الهيدروجين دون تفاعل ، والعكس فعند تحليـل المـاء ، يعطـي دائـما النسـب نفسـها ، مـن غازي الهيدروجين و الأكسجين فمثلا، إذا تفكك 9 جم من الماء ينتج 1 جم من الهيدروجين و 8 جم من الأكسجين ، و إذا تفكك 18 جم من الماء ، ينتج 2 جم من الهيدروجين و 16 جم من الأكسجين ،
ــــــــــــــــــ
أما قانون النسب المتضاعفة فهو أحد القوانين الأساسية في قياس اتحادية العناصر واكتشفه الكيميائي الأنكليزي جون دالتون سنة 1803. ينص القانون على أنه عند اتحاد عنصران كيميائيان وتكوين أكثر من مركب واحد، فإن النسبة بين الكتل المختلفة من أحد العنصرين التي تتحد مع كتلة ثابتة من العنصر الآخر تكون نسبة عددية صحيحة وبسيطة.
مثلا يتفاعل الأكسجين الكربون ليشكلا أول أكسيد الكربون (co) أو ثاني أكسيد الكربون (co2)
مثال آخر :
في المعادلة الآتية
o2 + 2h2 = 2h2o
حجم واحد من o2 : حجمين من h2 : حجمين من بخار الماء h2o
بمعنى لو تفاعل لترين من غاز الأكسجين فإنّه سيتفاعل 4 لترات من غاز الهيدروجين وينتج 4 لترات من بخار الماء.ولو تفاعل 10 لترات من غاز الأكسجين فإنّه سيتفاعل 20 لتر من غاز الهيدروجين وينتج 20 لتر من بخار الماء
__________________
raneem noor
أن كل مركب كيمـيائي مهما أختلف تحضيره ، فإنه يتـركب من عـناصره نفسها متحدة مع بعضها البعض بنسب ثابتة .
وقد توصل إلى هذا القانون (بروست) الفرنسي الذي أكمل دراسات أنطوان لافوازييه بعد وفاته وتبين له’ أن المركبات تحتوي على نسب ثابتة من العناصر المكونة لها’ ولاتتغير هذه النسب مهما اختلفت طرق تحضير المركب.
فمثلا ملح الطعام النقي سواء حصلنا عليه من مياه البحار أو تم تحضيره من تفاعل كميائي’ فإنه يحتوي دائما على 39,3% من كتلته الصوديوم و60,7% من كتلته كلور
مثال آخر جميع عينات الماء النقي تحتوي على عنصري الهـيدروجين و الأكسـجين بنسـبة كتلة جزء من الهيدروجين إلى ثمانية أجزاء من أكسـجين ( فمثلا:1 جم من الهيدروجين إلى 8 جم من الأكسجين) كذلك، عندما يسمح للهيدروجين بالتفاعل مع الأكسجين لينتج الماء ، فأن الكمـيات النسـبية لكل من الهيدروجين و الأكسـجين التي تتفـاعل تبــقى نفـسها دائـما ، فـكلما تفاعل1جم من الهيدروجين يلاحظ أنه دائما يستهلك فقط 8 جم من الأكسجين ، حتى لـو توافـرت كمـية أكـبر مـن الأكسجين فمثلا إذا خلط 2جم من الهيدروجين مع 8 جم من الأكسجين ، و أشـعل الخلـيط يتكـون 9 جم من المـاء ويبقى 1 جم من الهيدروجين دون تفاعل ، والعكس فعند تحليـل المـاء ، يعطـي دائـما النسـب نفسـها ، مـن غازي الهيدروجين و الأكسجين فمثلا، إذا تفكك 9 جم من الماء ينتج 1 جم من الهيدروجين و 8 جم من الأكسجين ، و إذا تفكك 18 جم من الماء ، ينتج 2 جم من الهيدروجين و 16 جم من الأكسجين ،
ــــــــــــــــــ
أما قانون النسب المتضاعفة فهو أحد القوانين الأساسية في قياس اتحادية العناصر واكتشفه الكيميائي الأنكليزي جون دالتون سنة 1803. ينص القانون على أنه عند اتحاد عنصران كيميائيان وتكوين أكثر من مركب واحد، فإن النسبة بين الكتل المختلفة من أحد العنصرين التي تتحد مع كتلة ثابتة من العنصر الآخر تكون نسبة عددية صحيحة وبسيطة.
مثلا يتفاعل الأكسجين الكربون ليشكلا أول أكسيد الكربون (co) أو ثاني أكسيد الكربون (co2)
مثال آخر :
في المعادلة الآتية
o2 + 2h2 = 2h2o
حجم واحد من o2 : حجمين من h2 : حجمين من بخار الماء h2o
بمعنى لو تفاعل لترين من غاز الأكسجين فإنّه سيتفاعل 4 لترات من غاز الهيدروجين وينتج 4 لترات من بخار الماء.ولو تفاعل 10 لترات من غاز الأكسجين فإنّه سيتفاعل 20 لتر من غاز الهيدروجين وينتج 20 لتر من بخار الماء
__________________
raneem noor
أشعة مهبطية
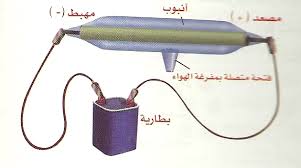
رسم تخطيطي لإنبوب كروكس: المعدات A هو مزود فولتي ضعيف لتسخين الكاثود C (الكاثود البارد كان قد استخدم بواسطة كروكس). B هو مزود طاقة عالي الفولتية لتنشيط الأنود المغلف بالفوسفور P. القناع المضللM يكون متصل بجهد الكاثود, والصورة ينظر فيها إلى الفوسفور كنطاق غير متوهج
أشعة المهبط أو أشعة الكاثود هي سيل من الأشعة غير المنظورة تنبعث من كاثود أنبوبة تفريغ كهربي ضغط الغاز فيها منخفض يتراوح بين 01. : 001. مم زئبق وفرق الجهدبين قطبي المصدر الكهربي يصل إلى 10000 فولت.
خواصها
شوق المرشدي
رسم تخطيطي لإنبوب كروكس: المعدات A هو مزود فولتي ضعيف لتسخين الكاثود C (الكاثود البارد كان قد استخدم بواسطة كروكس). B هو مزود طاقة عالي الفولتية لتنشيط الأنود المغلف بالفوسفور P. القناع المضللM يكون متصل بجهد الكاثود, والصورة ينظر فيها إلى الفوسفور كنطاق غير متوهج
أشعة المهبط أو أشعة الكاثود هي سيل من الأشعة غير المنظورة تنبعث من كاثود أنبوبة تفريغ كهربي ضغط الغاز فيها منخفض يتراوح بين 01. : 001. مم زئبق وفرق الجهدبين قطبي المصدر الكهربي يصل إلى 10000 فولت.
خواصها
- تسير في خطوط مستقيمة من المهبط (الكاثود) إلى المصعد (الأنود) تبسيطاً بشكل موازٍ للحقل الكهربائي المطبق بين المصعد والمهبط.
- لها تأثير حراري حيث أنها تحدث توهج على جدار أنبوب التفريغ.
- تتكون من دقائق مادية صغيرة. أي ان لها كتلة
- تتأثر بالمجال المغناطيسي والكهربائي بطريقة تدل على أن شحنتها سالبة.
- لا تتغير بتغير نوع مادة المهبط أو نوع الغاز المخلخل مما يدل على انها تدخل في تركيب جميع المواد.
- تسير هذه الاشعة داخل الأنبوبة في خطوط مستقيمة تبسيطاً بشكل موازٍ للحقل الكهربائي المطبق بين المصعد والمهبط أي عمودياً على سطح المهبط (الكاثود). وكذلك لو نظرنا إلى أحد خصائص الضوء سنجدها تحمل صفة الاستقامة مثل أشعة الكاثود، بحيث لو أننا وضعنا جسماً معيناً في ضوء الشمس سيتكون ظل لهذا الجسم.
- عند اصطدام هذه الأشعة بسطح معدني رقيق فإنها ترفع درجة حرارته حتى التوهج (أي أنها تحمل طاقة حركية)، كذلك الضوء يحمل هذه الصفة، حيث لو أننا لمسنا مصباح سيارة مثلا بعد مشوار طويل في الليل سنجد أنه ساخن أي يحمل طاقة حرارية فهذه الطاقة تحولت من الطاقة الضوئية.
- تحرك عجلة خفيفة عند اصطدامها بها أي أن لها كمية حركة (أو كتلة)، ولكن لونظرنا إلى الضوء سنجد أنه لا يحمل هذه الصفة، حيث لو أننا سلطنا مصباح على مروحة قابلة للدوران حول محور لن تدور هذه المروحة ولكن سيحدث العكس عند أشعة الكاثود (أي ستدور المروحة).
- تنحرف هذه الأشعة عند دخولها مجالاً مغناطيسياً عمودياً على اتجاهها (أي أنها تمتلك شحنات كهربائية سالبة)، ولكن لو سلطنا ضوء مصباح على المولد الكهربائي سنجد أن الضوء يسير بلا انحراف أو تكسر أو حيود فهذا يفسر أن الضوء لا يحمل هذه الصفة ولا يتأثر بالمجال المغناطيسي.
شوق المرشدي
مفهوم الذرة Atom
إن عالمنا المادي يحتوي على أشياء كثيرة جدا مثل الخشب والحديد والزجاج والسكر وكل هذه الأشياء نسميها المادة. ونعني بالمادة كل شيء يشغل حيزا في الفضاء وله وزن.ولنضرب مثلا بسيطا من أمثلة هذه المواد ( الماء) إذا أخذنا كمية من الماء وأمكننا تقسيمها إلى أقسام صغيرة وبقينا نقسمها حتى نصل ولو نظريا إلى جزء صغير من الماء لا يمكن أن نقسمه إلى أصغر منه بالطريقة العادية لعمليات التقسيم والفصل. وهذا الجزء الصغير جدا يبقى محتفظا بخواص الماء الأصلية من حيث لونه وطعمه وخواصه الكيمائية. نسمي هذا الجزء المتناهي في الصغر بالجزيء
إذا مررنا التيار الكهربي في الماء فإن هذا الجزيء سوف يتحلل إلى غازين هما الأكسيجين والهدروجين وهما لا يشبهان الماء في أي من خواصه بل هما أبسط منه تركيبا . ونسمي المواد التي يمكن أن تتحلل بالكهربية أو بغيرها من الوسائل إلى ما هو أبسط منها مثل الماء بالمركب Compound ونسمي المادة التي لا يمكن أن تتحلل إلى أبسط منها بالعنصر El�ment وأصغر جزء من المركبات كالماء مثلا الجزيء Mol�cule
ولكن الجزيء من المواد المختلفة يحتوي على وحدة أصغر منه تسمى الذرة Atome أو مجموعة من الذرات تسمى Atomes وقد تكون مختلفة في حالة المركبات ومتشابهة كما في حالة العناصر . ويجب أنلاحظ أن جزيء المركب يحتوي على الأقل على ذرتين مختلفتين في نوعهما وهناك أنواع كثيرة من الجزيئات كما أن هناك أنواع كثيرة من المواد . ولكن لا يوجد في العالم غير 92 عنصرا وبذلك لا يكون هناك غير 92 ذرة .
وعندما نذكر ذلك لابد أن ننوه عن جهود العلماء الذين فتحوا آفاق الطاقة الذرية وأمكنهم أن يحولوا العناصر إلى بعضها البعض بل أمكنهم استنباط عناصر جديدة من العناصر القديمة الموجودة.ولقد وصل عدد العناصر المعروفة 102عنصرا .كما أنه يمكننا استخدام أنواع مختلفة من اللبنات لبناء عمارة مثلا ,فإنه يمكننا كذلك استخدام عدة أنواع من الذرات لتركيب الجزيئات . ومعظم المواد المعروفة للإنسان تتكون من عدد قليل من العناصر أو الذرات المختلفة الأنواع مرتبطة مع بعضها بنسب مختلفة .
ولقد كان العلم الإنجليزي الفيزيائي جوزاف تومسن J.J. Thomson 1897 أول من أعلن أن الذرات إذا أحيطت بظروف خاصة فإنه يمكنها أن تطلق أجزاء متناهية في الصغر , وكان ذلك حدثا كبيرا قضى على أن الذرة هي لأدق شيء في الوجود وأنها لا تتحلل إلى ما هو أبسط منها إلا أنه تم إدراج مفهوم جديد لمكونات الذرة وهو الإلكترون Electron والإلكترونات إجمالا متشابهة بغض النظر عن المواد التي تنطلق منها وقد ساعدت هذه النظرية في دراسة الذرة وتركيبة كل مادة على الوجه السليم فكانت خلاصة تركيب الذرة لكل مادة
تركيبة الذرة
تتركب الذرة أساسا من نواة مؤلفة من بروتونات وهي التي تكون الجزء الأكبر من المادة وهي ذات شحنة كهربية موجبة + والنيترونات وتماثلها في العدد ولكنها عنصر محايد كهربيا في تركيبة الذرة أما الجزء الفاعل في الذرة فهو الإلكترون أو الكهرب فهو مكون ذو شحنة كهربية سلبية Electron ومنه جاءت تسمية الإلكترونيات والكهرباء
وللذرة أجزاء أخرى الميزترون mesotron واليزيترون positron والأنتي بروتون Anti-proton وهذه الأجزاء لا تظهر في الأحوال العادية ولكنها تظهر لمدة قصيرة عند تحطيم الذرة أو يمكن استنباطها بطرق علمية مختلفة
وحسب النظرية الإلكترونية تتكون الذرة من ثلاث أجزاء رئيسية:
1. الإلكترونات وهي محملة بشحنة سالبة
2. البروتونات وهي محملة بشحنة موجبة ويبلغ وزن البروتون 1840 مرة وزن الإلكترون
3. النيترون ولا يحمل أي شحنة كهربية ووزنه يساوي وزن البروتون
مثال : ذرة الهيدروجين
تتركب الذرة في جميع المواد على المكونات الثلاث السابقة وتختلف الذرات عن بعضها في عدد المكونات من الإلكترونات والبروتونات والنترونات وطريقة ترتيبها في الذرة .
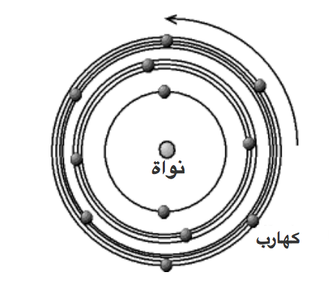
ولقد قدم العالم الدنمركي نيلز بوهر N.Bohr والمولود سنة 1885 مقاربة لصورة الذرة وهي مقبولة ومازالت معتمدة ومأخوذ بها في تركيبة الذرة فهي عبارة عن نواة يدور حولها بسرعة كبيرة عدد من الإلكترونات مما تشكل سحابة ويكون الدوران في مدار يشبه المجموعة الشمسية ( تذكروا قول الله :وكل في فلك يسبحون. ) وتسمى هذه المدارات بالسويّات أما النواة فهي لب الذرة وتتكون من البروتونات والنيترونات التي تكون أساسا كتلة الذرة ويسمى عدد البروتونات الموجودة في نواة الذرة بالعدد الذري وهو يساوي في مقدار الإلكترونات ويخالفه نوع الشحنة
يبدأ العدد الذري بالرقم 1 للهيدروجين وينتهي عند 92 لليورنيوم وأعلى من ذلك للعناصر الجديدة المستنبطة من اليورنيوم
ولتصوير مدى صغر ذرة الهدروجين حسب بعض العلماء أنه لو صفت ذرات الهيدروجين في خط واحد بحيث تكون متجاورة فإن 250 مليون ذرة منها تشغل طولا قدره بوصة واحدة.
ولنتصور مدى صغر الإلكترون حسب أنه لو صفت الإلكترونات بجوار بعضها فإن 100.000 إلكترون منها تشغل مسافة تساوي قطر ذرة واحدة من الهيدروجين.
أما بالنسبة للبروتون والنيترون أمكن حساب أنه لو وضع 1800بروتون أو نيترون بجوار بعضها فإنها تشغل ما يساوي قطره إلكترون واحد .
شوق المرشدي
مثال : السيلسيوم - السيليكون
إن عالمنا المادي يحتوي على أشياء كثيرة جدا مثل الخشب والحديد والزجاج والسكر وكل هذه الأشياء نسميها المادة. ونعني بالمادة كل شيء يشغل حيزا في الفضاء وله وزن.ولنضرب مثلا بسيطا من أمثلة هذه المواد ( الماء) إذا أخذنا كمية من الماء وأمكننا تقسيمها إلى أقسام صغيرة وبقينا نقسمها حتى نصل ولو نظريا إلى جزء صغير من الماء لا يمكن أن نقسمه إلى أصغر منه بالطريقة العادية لعمليات التقسيم والفصل. وهذا الجزء الصغير جدا يبقى محتفظا بخواص الماء الأصلية من حيث لونه وطعمه وخواصه الكيمائية. نسمي هذا الجزء المتناهي في الصغر بالجزيء
إذا مررنا التيار الكهربي في الماء فإن هذا الجزيء سوف يتحلل إلى غازين هما الأكسيجين والهدروجين وهما لا يشبهان الماء في أي من خواصه بل هما أبسط منه تركيبا . ونسمي المواد التي يمكن أن تتحلل بالكهربية أو بغيرها من الوسائل إلى ما هو أبسط منها مثل الماء بالمركب Compound ونسمي المادة التي لا يمكن أن تتحلل إلى أبسط منها بالعنصر El�ment وأصغر جزء من المركبات كالماء مثلا الجزيء Mol�cule
ولكن الجزيء من المواد المختلفة يحتوي على وحدة أصغر منه تسمى الذرة Atome أو مجموعة من الذرات تسمى Atomes وقد تكون مختلفة في حالة المركبات ومتشابهة كما في حالة العناصر . ويجب أنلاحظ أن جزيء المركب يحتوي على الأقل على ذرتين مختلفتين في نوعهما وهناك أنواع كثيرة من الجزيئات كما أن هناك أنواع كثيرة من المواد . ولكن لا يوجد في العالم غير 92 عنصرا وبذلك لا يكون هناك غير 92 ذرة .
وعندما نذكر ذلك لابد أن ننوه عن جهود العلماء الذين فتحوا آفاق الطاقة الذرية وأمكنهم أن يحولوا العناصر إلى بعضها البعض بل أمكنهم استنباط عناصر جديدة من العناصر القديمة الموجودة.ولقد وصل عدد العناصر المعروفة 102عنصرا .كما أنه يمكننا استخدام أنواع مختلفة من اللبنات لبناء عمارة مثلا ,فإنه يمكننا كذلك استخدام عدة أنواع من الذرات لتركيب الجزيئات . ومعظم المواد المعروفة للإنسان تتكون من عدد قليل من العناصر أو الذرات المختلفة الأنواع مرتبطة مع بعضها بنسب مختلفة .
ولقد كان العلم الإنجليزي الفيزيائي جوزاف تومسن J.J. Thomson 1897 أول من أعلن أن الذرات إذا أحيطت بظروف خاصة فإنه يمكنها أن تطلق أجزاء متناهية في الصغر , وكان ذلك حدثا كبيرا قضى على أن الذرة هي لأدق شيء في الوجود وأنها لا تتحلل إلى ما هو أبسط منها إلا أنه تم إدراج مفهوم جديد لمكونات الذرة وهو الإلكترون Electron والإلكترونات إجمالا متشابهة بغض النظر عن المواد التي تنطلق منها وقد ساعدت هذه النظرية في دراسة الذرة وتركيبة كل مادة على الوجه السليم فكانت خلاصة تركيب الذرة لكل مادة
تركيبة الذرة
تتركب الذرة أساسا من نواة مؤلفة من بروتونات وهي التي تكون الجزء الأكبر من المادة وهي ذات شحنة كهربية موجبة + والنيترونات وتماثلها في العدد ولكنها عنصر محايد كهربيا في تركيبة الذرة أما الجزء الفاعل في الذرة فهو الإلكترون أو الكهرب فهو مكون ذو شحنة كهربية سلبية Electron ومنه جاءت تسمية الإلكترونيات والكهرباء
وللذرة أجزاء أخرى الميزترون mesotron واليزيترون positron والأنتي بروتون Anti-proton وهذه الأجزاء لا تظهر في الأحوال العادية ولكنها تظهر لمدة قصيرة عند تحطيم الذرة أو يمكن استنباطها بطرق علمية مختلفة
وحسب النظرية الإلكترونية تتكون الذرة من ثلاث أجزاء رئيسية:
1. الإلكترونات وهي محملة بشحنة سالبة
2. البروتونات وهي محملة بشحنة موجبة ويبلغ وزن البروتون 1840 مرة وزن الإلكترون
3. النيترون ولا يحمل أي شحنة كهربية ووزنه يساوي وزن البروتون
مثال : ذرة الهيدروجين
تتركب الذرة في جميع المواد على المكونات الثلاث السابقة وتختلف الذرات عن بعضها في عدد المكونات من الإلكترونات والبروتونات والنترونات وطريقة ترتيبها في الذرة .
ولقد قدم العالم الدنمركي نيلز بوهر N.Bohr والمولود سنة 1885 مقاربة لصورة الذرة وهي مقبولة ومازالت معتمدة ومأخوذ بها في تركيبة الذرة فهي عبارة عن نواة يدور حولها بسرعة كبيرة عدد من الإلكترونات مما تشكل سحابة ويكون الدوران في مدار يشبه المجموعة الشمسية ( تذكروا قول الله :وكل في فلك يسبحون. ) وتسمى هذه المدارات بالسويّات أما النواة فهي لب الذرة وتتكون من البروتونات والنيترونات التي تكون أساسا كتلة الذرة ويسمى عدد البروتونات الموجودة في نواة الذرة بالعدد الذري وهو يساوي في مقدار الإلكترونات ويخالفه نوع الشحنة
يبدأ العدد الذري بالرقم 1 للهيدروجين وينتهي عند 92 لليورنيوم وأعلى من ذلك للعناصر الجديدة المستنبطة من اليورنيوم
ولتصوير مدى صغر ذرة الهدروجين حسب بعض العلماء أنه لو صفت ذرات الهيدروجين في خط واحد بحيث تكون متجاورة فإن 250 مليون ذرة منها تشغل طولا قدره بوصة واحدة.
ولنتصور مدى صغر الإلكترون حسب أنه لو صفت الإلكترونات بجوار بعضها فإن 100.000 إلكترون منها تشغل مسافة تساوي قطر ذرة واحدة من الهيدروجين.
أما بالنسبة للبروتون والنيترون أمكن حساب أنه لو وضع 1800بروتون أو نيترون بجوار بعضها فإنها تشغل ما يساوي قطره إلكترون واحد .
شوق المرشدي
مثال : السيلسيوم - السيليكون
ن عالمنا المادي يحتوي على أشياء كثيرة جدا مثل الخشب والحديد والزجاج والسكر وكل هذه الأشياء نسميها المادة. ونعني بالمادة كل شيء يشغل حيزا في الفضاء وله وزن.ولنضرب مثلا بسيطا من أمثلة هذه المواد ( الماء) إذا أخذنا كمية من الماء وأمكننا تقسيمها إلى أقسام صغيرة وبقينا نقسمها حتى نصل ولو نظريا إلى جزء صغير من الماء لا يمكن أن نقسمه إلى أصغر منه بالطريقة العادية لعمليات التقسيم والفصل. وهذا الجزء الصغير جدا يبقى محتفظا بخواص الماء الأصلية من حيث لونه وطعمه وخواصه الكيمائية. نسمي هذا الجزء المتناهي في الصغر بالجزيء
إذا مررنا التيار الكهربي في الماء فإن هذا الجزيء سوف يتحلل إلى غازين هما الأكسيجين والهدروجين وهما لا يشبهان الماء في أي من خواصه بل هما أبسط منه تركيبا . ونسمي المواد التي يمكن أن تتحلل بالكهربية أو بغيرها من الوسائل إلى ما هو أبسط منها مثل الماء بالمركب Compound ونسمي المادة التي لا يمكن أن تتحلل إلى أبسط منها بالعنصر El�ment وأصغر جزء من المركبات كالماء مثلا الجزيء Mol�cule
ولكن الجزيء من المواد المختلفة يحتوي على وحدة أصغر منه تسمى الذرة Atome أو مجموعة من الذرات تسمى Atomes وقد تكون مختلفة في حالة المركبات ومتشابهة كما في حالة العناصر . ويجب أنلاحظ أن جزيء المركب يحتوي على الأقل على ذرتين مختلفتين في نوعهما وهناك أنواع كثيرة من الجزيئات كما أن هناك أنواع كثيرة من المواد . ولكن لا يوجد في العالم غير 92 عنصرا وبذلك لا يكون هناك غير 92 ذرة .
وعندما نذكر ذلك لابد أن ننوه عن جهود العلماء الذين فتحوا آفاق الطاقة الذرية وأمكنهم أن يحولوا العناصر إلى بعضها البعض بل أمكنهم استنباط عناصر جديدة من العناصر القديمة الموجودة.ولقد وصل عدد العناصر المعروفة 102عنصرا .كما أنه يمكننا استخدام أنواع مختلفة من اللبنات لبناء عمارة مثلا ,فإنه يمكننا كذلك استخدام عدة أنواع من الذرات لتركيب الجزيئات . ومعظم المواد المعروفة للإنسان تتكون من عدد قليل من العناصر أو الذرات المختلفة الأنواع مرتبطة مع بعضها بنسب مختلفة .
Joseph John Thomson
ولقد كان العلم الإنجليزي الفيزيائي جوزاف تومسن J.J. Thomson 1897 أول من أعلن أن الذرات إذا أحيطت بظروف خاصة فإنه يمكنها أن تطلق أجزاء متناهية في الصغر , وكان ذلك حدثا كبيرا قضى على أن الذرة هي لأدق شيء في الوجود وأنها لا تتحلل إلى ما هو أبسط منها إلا أنه تم إدراج مفهوم جديد لمكونات الذرة وهو الإلكترون Electron والإلكترونات إجمالا متشابهة بغض النظر عن المواد التي تنطلق منها وقد ساعدت هذه النظرية في دراسة الذرة وتركيبة كل مادة على الوجه السليم فكانت خلاصة تركيب الذرة لكل مادة
تركيبة الذرة
تتركب الذرة أساسا من نواة مؤلفة من بروتونات وهي التي تكون الجزء الأكبر من المادة وهي ذات شحنة كهربية موجبة + والنيترونات وتماثلها في العدد ولكنها عنصر محايد كهربيا في تركيبة الذرة أما الجزء الفاعل في الذرة فهو الإلكترون أو الكهرب فهو مكون ذو شحنة كهربية سلبية Electron ومنه جاءت تسمية الإلكترونيات والكهرباء
وللذرة أجزاء أخرى الميزترون mesotron واليزيترون positron والأنتي بروتون Anti-proton وهذه الأجزاء لا تظهر في الأحوال العادية ولكنها تظهر لمدة قصيرة عند تحطيم الذرة أو يمكن استنباطها بطرق علمية مختلفة
وحسب النظرية الإلكترونية تتكون الذرة من ثلاث أجزاء رئيسية:
1. الإلكترونات وهي محملة بشحنة سالبة
2. البروتونات وهي محملة بشحنة موجبة ويبلغ وزن البروتون 1840 مرة وزن الإلكترون
3. النيترون ولا يحمل أي شحنة كهربية ووزنه يساوي وزن البروتون
مثال : ذرة الهيدروجين
تتركب الذرة في جميع المواد على المكونات الثلاث السابقة وتختلف الذرات عن بعضها في عدد المكونات من الإلكترونات والبروتونات والنترونات وطريقة ترتيبها في الذرة .
ولقد قدم العالم الدنمركي نيلز بوهر N.Bohr والمولود سنة 1885 مقاربة لصورة الذرة وهي مقبولة ومازالت معتمدة ومأخوذ بها في تركيبة الذرة فهي عبارة عن نواة يدور حولها بسرعة كبيرة عدد من الإلكترونات مما تشكل سحابة ويكون الدوران في مدار يشبه المجموعة الشمسية ( تذكروا قول الله :وكل في فلك يسبحون. ) وتسمى هذه المدارات بالسويّات أما النواة فهي لب الذرة وتتكون من البروتونات والنيترونات التي تكون أساسا كتلة الذرة ويسمى عدد البروتونات الموجودة في نواة الذرة بالعدد الذري وهو يساوي في مقدار الإلكترونات ويخالفه نوع الشحنة
نيلز بوهر
Niels Henrik David Bohr
حائز على جائز نوبل سنة 1922
يبدأ العدد الذري بالرقم 1 للهيدروجين وينتهي عند 92 لليورنيوم وأعلى من ذلك للعناصر الجديدة المستنبطة من اليورنيوم
ولتصوير مدى صغر ذرة الهدروجين حسب بعض العلماء أنه لو صفت ذرات الهيدروجين في خط واحد بحيث تكون متجاورة فإن 250 مليون ذرة منها تشغل طولا قدره بوصة واحدة.
ولنتصور مدى صغر الإلكترون حسب أنه لو صفت الإلكترونات بجوار بعضها فإن 100.000 إلكترون منها تشغل مسافة تساوي قطر ذرة واحدة من الهيدروجين.
أما بالنسبة للبروتون والنيترون أمكن حساب أنه لو وضع 1800بروتون أو نيترون بجوار بعضها فإنها تشغل ما يساوي قطره إلكترون واحد .
مثال : السيلسيوم - السيليكون
raneem noor
إذا مررنا التيار الكهربي في الماء فإن هذا الجزيء سوف يتحلل إلى غازين هما الأكسيجين والهدروجين وهما لا يشبهان الماء في أي من خواصه بل هما أبسط منه تركيبا . ونسمي المواد التي يمكن أن تتحلل بالكهربية أو بغيرها من الوسائل إلى ما هو أبسط منها مثل الماء بالمركب Compound ونسمي المادة التي لا يمكن أن تتحلل إلى أبسط منها بالعنصر El�ment وأصغر جزء من المركبات كالماء مثلا الجزيء Mol�cule
ولكن الجزيء من المواد المختلفة يحتوي على وحدة أصغر منه تسمى الذرة Atome أو مجموعة من الذرات تسمى Atomes وقد تكون مختلفة في حالة المركبات ومتشابهة كما في حالة العناصر . ويجب أنلاحظ أن جزيء المركب يحتوي على الأقل على ذرتين مختلفتين في نوعهما وهناك أنواع كثيرة من الجزيئات كما أن هناك أنواع كثيرة من المواد . ولكن لا يوجد في العالم غير 92 عنصرا وبذلك لا يكون هناك غير 92 ذرة .
وعندما نذكر ذلك لابد أن ننوه عن جهود العلماء الذين فتحوا آفاق الطاقة الذرية وأمكنهم أن يحولوا العناصر إلى بعضها البعض بل أمكنهم استنباط عناصر جديدة من العناصر القديمة الموجودة.ولقد وصل عدد العناصر المعروفة 102عنصرا .كما أنه يمكننا استخدام أنواع مختلفة من اللبنات لبناء عمارة مثلا ,فإنه يمكننا كذلك استخدام عدة أنواع من الذرات لتركيب الجزيئات . ومعظم المواد المعروفة للإنسان تتكون من عدد قليل من العناصر أو الذرات المختلفة الأنواع مرتبطة مع بعضها بنسب مختلفة .
Joseph John Thomson
ولقد كان العلم الإنجليزي الفيزيائي جوزاف تومسن J.J. Thomson 1897 أول من أعلن أن الذرات إذا أحيطت بظروف خاصة فإنه يمكنها أن تطلق أجزاء متناهية في الصغر , وكان ذلك حدثا كبيرا قضى على أن الذرة هي لأدق شيء في الوجود وأنها لا تتحلل إلى ما هو أبسط منها إلا أنه تم إدراج مفهوم جديد لمكونات الذرة وهو الإلكترون Electron والإلكترونات إجمالا متشابهة بغض النظر عن المواد التي تنطلق منها وقد ساعدت هذه النظرية في دراسة الذرة وتركيبة كل مادة على الوجه السليم فكانت خلاصة تركيب الذرة لكل مادة
تركيبة الذرة
تتركب الذرة أساسا من نواة مؤلفة من بروتونات وهي التي تكون الجزء الأكبر من المادة وهي ذات شحنة كهربية موجبة + والنيترونات وتماثلها في العدد ولكنها عنصر محايد كهربيا في تركيبة الذرة أما الجزء الفاعل في الذرة فهو الإلكترون أو الكهرب فهو مكون ذو شحنة كهربية سلبية Electron ومنه جاءت تسمية الإلكترونيات والكهرباء
وللذرة أجزاء أخرى الميزترون mesotron واليزيترون positron والأنتي بروتون Anti-proton وهذه الأجزاء لا تظهر في الأحوال العادية ولكنها تظهر لمدة قصيرة عند تحطيم الذرة أو يمكن استنباطها بطرق علمية مختلفة
وحسب النظرية الإلكترونية تتكون الذرة من ثلاث أجزاء رئيسية:
1. الإلكترونات وهي محملة بشحنة سالبة
2. البروتونات وهي محملة بشحنة موجبة ويبلغ وزن البروتون 1840 مرة وزن الإلكترون
3. النيترون ولا يحمل أي شحنة كهربية ووزنه يساوي وزن البروتون
مثال : ذرة الهيدروجين
تتركب الذرة في جميع المواد على المكونات الثلاث السابقة وتختلف الذرات عن بعضها في عدد المكونات من الإلكترونات والبروتونات والنترونات وطريقة ترتيبها في الذرة .
ولقد قدم العالم الدنمركي نيلز بوهر N.Bohr والمولود سنة 1885 مقاربة لصورة الذرة وهي مقبولة ومازالت معتمدة ومأخوذ بها في تركيبة الذرة فهي عبارة عن نواة يدور حولها بسرعة كبيرة عدد من الإلكترونات مما تشكل سحابة ويكون الدوران في مدار يشبه المجموعة الشمسية ( تذكروا قول الله :وكل في فلك يسبحون. ) وتسمى هذه المدارات بالسويّات أما النواة فهي لب الذرة وتتكون من البروتونات والنيترونات التي تكون أساسا كتلة الذرة ويسمى عدد البروتونات الموجودة في نواة الذرة بالعدد الذري وهو يساوي في مقدار الإلكترونات ويخالفه نوع الشحنة
نيلز بوهر
Niels Henrik David Bohr
حائز على جائز نوبل سنة 1922
يبدأ العدد الذري بالرقم 1 للهيدروجين وينتهي عند 92 لليورنيوم وأعلى من ذلك للعناصر الجديدة المستنبطة من اليورنيوم
ولتصوير مدى صغر ذرة الهدروجين حسب بعض العلماء أنه لو صفت ذرات الهيدروجين في خط واحد بحيث تكون متجاورة فإن 250 مليون ذرة منها تشغل طولا قدره بوصة واحدة.
ولنتصور مدى صغر الإلكترون حسب أنه لو صفت الإلكترونات بجوار بعضها فإن 100.000 إلكترون منها تشغل مسافة تساوي قطر ذرة واحدة من الهيدروجين.
أما بالنسبة للبروتون والنيترون أمكن حساب أنه لو وضع 1800بروتون أو نيترون بجوار بعضها فإنها تشغل ما يساوي قطره إلكترون واحد .
مثال : السيلسيوم - السيليكون
raneem noor
- افكار الفلاسفة الإغريق حول المادة :
* ديمقريطس Democritus ( ٣٧٠-٤٦٠ ) ق.م :
* ديمقريطس Democritus ( ٣٧٠-٤٦٠ ) ق.م :
- تتكون المادة من ذرات تتحرك في الفراغ .
- الذرات الصلبة ، متجانسة ، لاتتحطم ولاتتجزأ .
- الأنواع المختلفة من الذرات لها أحجام وأشكال مختلفة .
- حجم الذرات وشكلها وحركتها يحدد خواص المادة .
- لا وجود للفراغ .
- الماده مكونة من التراب ، والنار ، والهواء ، والماء .
- الذرات لاتتجزأ ولاتتكسر.
- تختلف ذرات أي عنصر عن ذرات العناصر الأخرى .
- في التفاعلات الكميائية : تنفصل الذرات ، أو تتحد ، أو يعاد ترتيبها .
- شوق المرشدي
المخــلوط والعناصر والمركباتالمخلوط : عباره عن عدة مواد مخلطه ببعضها البعض المواد الموجوده في المخلوط تحافظ على صفاتها ويمكن فصلها بطرق كيميائيه مختلفه هنالك نوعين من المخاليــط
انــواع المخــاليط هي :
1 - متــجانس : مخلوط يتكــون من مــادتين او اكثــر تظهــر كماده واحده مخــلوط كهذا يدعى محلول .
2- غيــر متجانس : مخــلوط من مادتيــن او اكثــر لكنــه لا يــظهر كمــاده واحــده .
العنــصر :عباره عن مواد نقيه مبنيه من نفس النوع من الذرات لا يمكن تحليلها الى ابسط منها .
حتى لو اجرينــا على العنصر عملية كيميائيه او فيزيائيه لا يتحول هذا العنصر الى مواد جديده وانما يبقى كما هو .
للعنـــصر نوعين :
عنـــصر طبيعي : موجود في الطبيعه مثــل النحـــاس , الحديد .
عنــــصر صنــاعي : تحضر فــي المختبــرات مثــل المغنيزيوم .
YouTube Video
المــركــب : هــو عباره عــن مــاده مكــونه مــن عنــاصر (ذرات مختلــفه ) مــثال :
المــــاء عباره عـــن مركب مكــتون من ذرتــين هيدروجيــن وذرة اكســـجين واحده .
صــدأ الحديد هـــو مركب ايضـــا مــركب من حديــد واكســجين
مـــلاحظه : المـــركب يختلــف في صفاته عــن صفـــات المواد التـــي تكونه
مـــثال : الماء هو مــاده غير قابله للأشتعال لكنهــا تتركب من الاوكسجيــن والاوكسجــين
مـــاده قـــابلــه للأشتــعال .
raneem noor
انــواع المخــاليط هي :
1 - متــجانس : مخلوط يتكــون من مــادتين او اكثــر تظهــر كماده واحده مخــلوط كهذا يدعى محلول .
2- غيــر متجانس : مخــلوط من مادتيــن او اكثــر لكنــه لا يــظهر كمــاده واحــده .
العنــصر :عباره عن مواد نقيه مبنيه من نفس النوع من الذرات لا يمكن تحليلها الى ابسط منها .
حتى لو اجرينــا على العنصر عملية كيميائيه او فيزيائيه لا يتحول هذا العنصر الى مواد جديده وانما يبقى كما هو .
للعنـــصر نوعين :
عنـــصر طبيعي : موجود في الطبيعه مثــل النحـــاس , الحديد .
عنــــصر صنــاعي : تحضر فــي المختبــرات مثــل المغنيزيوم .
YouTube Video
المــركــب : هــو عباره عــن مــاده مكــونه مــن عنــاصر (ذرات مختلــفه ) مــثال :
المــــاء عباره عـــن مركب مكــتون من ذرتــين هيدروجيــن وذرة اكســـجين واحده .
صــدأ الحديد هـــو مركب ايضـــا مــركب من حديــد واكســجين
مـــلاحظه : المـــركب يختلــف في صفاته عــن صفـــات المواد التـــي تكونه
مـــثال : الماء هو مــاده غير قابله للأشتعال لكنهــا تتركب من الاوكسجيــن والاوكسجــين
مـــاده قـــابلــه للأشتــعال .
raneem noor
1- المقدمه
لحمد لله رب العالمين والصلاة والسلام على أشرف المرسلين معلم الأمة ومرشدها سيدنا
محمد صلى الله عليه وسلم النبي الأمين وعلى آله وصحبه أجمعين وبعد فهذا تقرير الكيمياء
يتكلم عن المادة هي كل ماله كتلة ويشغل حيزا من الفراغ وأنها توجد على حلات ثلاث
إضافة الى الحالة الربعة سوف تتعرف لها في هذه البحث
المادة هي كل ما له كتلة وكل ما يتكون منه الأجسام الفيزيائية، من غير حساب الطاقة لهذه
الأجسام (بالرغم من أنها قد تغيير كتلة الجسم) , و قد تغير اعتقاد الانسان كثيرا عبر
العصور حول هذا التركيب المادي من تقسيم الطبيعة الى أربعة عناصر اساسية الى
اكتشاف العناصر الكيميائية الى اكتشاف الذرة .
يتكون الكون الطبيعى "الذى يشتمل على كائنات حيه" من مادة وطاقه وهما يعتبران اساس
جميع الظواهر المحسوسة
2-تعريف المادة
هى كل ما له حجم وكتلة ويشغل حيزا و تتحول المادة من حاله الى اخرى
ونلاحظ ان المادة عندما يحدث لها التغير يكون تغير كيميائى او تغير فيزيائى.
3-التغير الكيميائى
هو التغير الذى يحدث فى تركيب المادة وينتج عنه مواد جديدة
4-التغير الفيزيائى
هو التغير الذى يحدث فى تركيب المادة ولاينتج عنه مواد جديدة اىيحدث فى مظهر المادة
فقط وعند دراسة المادة وجدا انها اما ان تكون متجانسه او غير متجانس
و تتكون المادة من وحدات بنائيه صغيرة وتسمى الجزيئات ومفردها الجزئ ويلاحظ
ان الجزئ يتكون من وحدات بنائيه اصغر تسمى ذرات ويلاحظ ان جزيئات المادة الواحدة
اذا كانت متجانسه تكون متشابه وجزيئات المادة اذا كانت غير.
متجانسه تكون غير متشابه
5-حالات المادة
أولاً : الحاله الصلبه
تتميز المواد الصلبه بان لها شكل معين وحجم معين وتتحول المادة من الحاله الصلبه الى
الحاله السائله وتسمى هذة العمليه بعملية الانصهار.
ثانياً : الحاله السائله
وتتميز المواد السائله بانها تاخذ شكل الاناء ولها حجم معين وتتحول المادة من الحاله
السائله الى الحاله الصلبه وتسمى هذة العمليه بعملية التجمد.
ثالثاً :الحاله الغازيه
وتتميز المواد الغازيه بان ليس لها شكل معين ولا حجم معين وتتحول المادة من الحاله
الغازيه الى الحاله السائله وتسمى هذة العمليه بعملية التكثيف اما عند تحول المادة من
الحاله السائله الى الحاله الغازيه تسمى بعمليه التبخر.
أما الحالة الرابعة من المادة وهي " البلازما " وتتكون البلازما عبر مراحل تدريجية تتم بإرتفاع درجة الحرارة, حيث تتفكك جزيئات الغاز إلى ذرات في المرحلة الأولى. ثم يتبع ذلك في المرحلة الثانية تأيين لذرات الغازات نتيجة التصادمات التي تؤدي إلى إنطلاق الإلكترونات من المدارات الخارجية للذرات, وبذلك تتكون البلازما من خليط من الذرات المتعادلة والأيونات الموجبة والإلكترونات. والبلازما هي الحالة الشائعة للمادة في الكون حيث تشكل 99% من المادة. إلا أنها نادرة جداً على الأرض إلا في الحالات التي يقوم الإنسان بصنعها مثل " مصابيح الفلورنست ".
6-خصائص حالات المادة
الحالة الصلبة
1.تتحرك دقائقها حركة موضعية اهتزازية.
2.لها شكل ثابت.
3.لها حجم ثابت.
4.غير قابلة للانضغاط.
5.طاقتها الحركية قليلة.
الحالة السائلة
1.تتحرك دقائقها حركة انتقالية ودائمة وعشوائية.
2.تأخذ شكل الوعاء الذي يوضع فيه.
3.لها حجم ثابت.
4.صعبة الانضغاط.
5.قابلة للجريان.
6.طاقتها الحركية عالية.
الحالة الغازية
1.تتحرك دقائقها حركة انتقالية ودائمة وعشوائية وسريعة
وفي خطوط مستقيمة وبكافة الاتجاهات.
2.تأخذ شكل الوعاء الذي يوضع فيه.
3.حجمها يعتمد على حجم الوعاء الذي توضع فيه.
4.قابلة للانضغاط بسهولة.
5.تمتاز بخاصية الانتشار.
6.طاقتها الحركية عالية جداً.
تغير الحالة الفيزيائية
7-حالات تحول المادة
الانصهار
هو تحول المادة بالحرارة من الحاله الصلبه الى الحاله السائلة وتتميز المواد الصلبه
بان قوة الترابط الجزيئية تكون كبيرة جدا والمسافات البينية تكون صغيرة جدا
وتهتز الجزيئات فى مكانها ولاتتحرك من مكانها لذلك تحتفظ المواد الصلبه بشكل
ثابت وحجم ثابت وعند تسخين المادة الصلبه اى تزويد جزيئاتها بالحرارة فأنها
تهتز بسرعة أكبر للتغلب على قوة التجاذب بين هذة الجزيئات بمساعدة الحرارة التى
تكتسبها من التسخين وعند درجة حرارة معينه تسمى درجة الانصهار تتغلب الجزيئات على
قوة التماسك بينها وتتحرك من مواضعها فتتحول المادة من الحالة الصلبة الى الحالة
السائلة فيما يعرف بالانصهار.
التصعيد أو التبخر
هو تحول المادة بالحرارة من الحاله السائله الى الحاله الغازيه وتتحرك جزيئات السائل
حركه مستمرة ولكنها لاتبتعد كثيرا من بعضها ونلاحظ ان قوة الترابط الجزيئيه فى هذة
الحاله صغيرة جدا
8-الجزئ
هــو وحــدة بنــاء المـــادة وهو اصغــر جزء من المـــادة يمكـــن ان يوجــد منفـــــردا ويظل
محتفظـــــا بخـواص المــــادة وصفاتهــــا ونلاحـــــظ ان جزيئـات المـــــادة فى حالة حركـــــه
مستمـــرة هذة الحركه أكبـــــر ما يمكــــن تكــــون فى حـالة المـــواد الغازيــــه ويتبعهــــا
السوائل أما جزيئــــات المواد الصلبـــــه فحركتهــا قليله جدا فهــــى تهتز فى مكانهــــــا فقط
بدون ان تنتقل إلى مكـــــان اخـــــر توجــــد مسافـــات بينيـه اى فراغـات بين جزيئــــات
9-المادة وتكون كألاتى:
المــواد الصلبـــه: تكون فيهــا المسافــــات البينيـه للجزيئـــات صغيرة جــدا
المواد السائلـــه :تكــون فيها المسافــات البينية للجزيئات متوسطة الحجم
الغــازات تكـــون فيهــــا المسافـــات البينيــه للجزيئـــــات كبيــرة جـــــــدا
والجــزئ يتكـــون من وحـــدة بنائيـــه اصغــــر منــــــه وتسمــــى الــــذرةونلاحـــظ ان
جـــزئ الاكســـجين يتكـــون من ارتبــــاط ذرتـــى اكســــجين وجــــزئ الهيـــــدروجين
يتكـــــون من ارتبــــاط ذرتــــى هيــــدروجــــين وجــــزئ المـــــاء يتكــــون من ارتبــــاط
ذرتـــــى هيدروجــــين مع ذرة اكســــجين وجــــزئ ملـــح الطعــــــام ويسميـــــه
العلمـــــــــاء كلــــوريد الصوديــــــوم يتكــــــون مـــن ارتبــــــاط ذرة صوديــــــوم مـــــــــع
ذرة كلـــــــــور.
ملاحظه :
إن التغير في الحالة الفيزيائية يحدث أيضاً عند تحول الماء السائل إلى بخار أو العكس.
وعند تغير الحالة الفيزيائية للمادة لايتغير تركيبها الكيميائي، ولكن التغير يحدث فقط للمسافة بين دقائقها وقوى التجاذب بينها.
فعند تسخين الثلج تهتز الدقائق أكثر وتزيد سرعتها ، وتأخذ الدقائق بالانزلاق على بعضها ، وتبدأ بالذوبان.
وعند تسخين الماء السائل تزداد سرعة الدقائق وتأخذ بالتصادم فيما بينها مما يوفر لبعض الدقائق الموجودة على سطح السائل طاقة حركية كافية فتهرب من السطح وتتحول إلى بخار.
10-تفسير بعض خصائص المادة
الانتشار
إذا فتح أحدهم غطاء زجاجة عطر في الغرفة التي أنت بها ، فإنك سرعان ما تشعر بذلك، فالرائحة تنتشر بسرعة خلال الغرفة، وتعرف من خلال حاسة الشم بالذي حصل.
الانتشار خاصية تمتاز بها الغازات وتحدث عند اختلاط دقائق الغاز ذاتياً بالهواء.
ولكن هل تنتشر جميع الغازات بنفس السرعة؟
الانضغاط
هل دقائق الغاز متباعدة أم متقاربة؟
هل قوى التجاذب بين دقائق الغاز كبيرة أم قليلة؟
هل سرعة دقائق الغاز عالية أم منخفضة؟
إن تعريض الغاز للضغط، يؤدي إلى تقارب الجزيئات فتزداد معه قوى التجاذب بين الدقائق وتتباطأ وقد تتحول بمزيد من الضغط إلى سائل.
فسر سبب كون المواد الصلبة غير قابلة للانضغاط؟
التكاثف
أيهما يملك طاقة حركية أكبر الماء السائل أم بخاره؟
ماذا يحدث إذا مر البخار فوق سطح بارد؟
تمتلك دقائق البخار طاقة حركية عالية، وعند تعرض البخار لسطح بارد تقل الطاقة الحركية لدقائقه وتتقارب ، وتزداد قوى التجاذب بينها وتتحول إلى سائل.
التبخر
هل يحدث التبخر عند درجة حرارة معينة، أم عند أي درجة حرارة؟
عند أي جزء من السائل يحدث التبخر؟
كيف يحدث التبخر؟
تتحرك دقائق السائل حركة دائمة وعشوائية وفي كافة الاتجاهات، وتسمى هذه الحركة بالحركة البراونية ( نسبة إلى مكتشفها روبرت براون ).
يحدث تصادم بين دقائق السائل بفعل الحركة البراونية مما يؤدي إلى فقدان بعض الدقائق لطاقتها الحركية واكتساب بعضها الآخر لتلك الطاقة، فإذا صادف أن اكتسبت إحدى الدقائق الموجودة على السطح طاقة كافية، فإنها تنفلت من سطح السائل وتتحول إلى بخار.
11-الخاتمة ::
الحمد لله الذي أتم عليَّ نعمه، ووالى عليَّ مننه، وأعانني فأكملت هذا البخث بهذه الصورة التي أرجو أن أنال بها رضاه،وأن يكون تقرير نافعاً محققاً للغرض منه،وقد توصلت من خلاله إلى عدة نتائج من أهمها:
1. يربط بين حالة المادة و خولصه العامة .
2. يوجد العلاقة بين خواص المادة وقوةالترابط بين مكوناتها..
3. وجود الحالة الرابعة معه الحالات ثلاث للمادة وتسمه البلازما .
raneem noor
لحمد لله رب العالمين والصلاة والسلام على أشرف المرسلين معلم الأمة ومرشدها سيدنا
محمد صلى الله عليه وسلم النبي الأمين وعلى آله وصحبه أجمعين وبعد فهذا تقرير الكيمياء
يتكلم عن المادة هي كل ماله كتلة ويشغل حيزا من الفراغ وأنها توجد على حلات ثلاث
إضافة الى الحالة الربعة سوف تتعرف لها في هذه البحث
المادة هي كل ما له كتلة وكل ما يتكون منه الأجسام الفيزيائية، من غير حساب الطاقة لهذه
الأجسام (بالرغم من أنها قد تغيير كتلة الجسم) , و قد تغير اعتقاد الانسان كثيرا عبر
العصور حول هذا التركيب المادي من تقسيم الطبيعة الى أربعة عناصر اساسية الى
اكتشاف العناصر الكيميائية الى اكتشاف الذرة .
يتكون الكون الطبيعى "الذى يشتمل على كائنات حيه" من مادة وطاقه وهما يعتبران اساس
جميع الظواهر المحسوسة
2-تعريف المادة
هى كل ما له حجم وكتلة ويشغل حيزا و تتحول المادة من حاله الى اخرى
ونلاحظ ان المادة عندما يحدث لها التغير يكون تغير كيميائى او تغير فيزيائى.
3-التغير الكيميائى
هو التغير الذى يحدث فى تركيب المادة وينتج عنه مواد جديدة
4-التغير الفيزيائى
هو التغير الذى يحدث فى تركيب المادة ولاينتج عنه مواد جديدة اىيحدث فى مظهر المادة
فقط وعند دراسة المادة وجدا انها اما ان تكون متجانسه او غير متجانس
و تتكون المادة من وحدات بنائيه صغيرة وتسمى الجزيئات ومفردها الجزئ ويلاحظ
ان الجزئ يتكون من وحدات بنائيه اصغر تسمى ذرات ويلاحظ ان جزيئات المادة الواحدة
اذا كانت متجانسه تكون متشابه وجزيئات المادة اذا كانت غير.
متجانسه تكون غير متشابه
5-حالات المادة
أولاً : الحاله الصلبه
تتميز المواد الصلبه بان لها شكل معين وحجم معين وتتحول المادة من الحاله الصلبه الى
الحاله السائله وتسمى هذة العمليه بعملية الانصهار.
ثانياً : الحاله السائله
وتتميز المواد السائله بانها تاخذ شكل الاناء ولها حجم معين وتتحول المادة من الحاله
السائله الى الحاله الصلبه وتسمى هذة العمليه بعملية التجمد.
ثالثاً :الحاله الغازيه
وتتميز المواد الغازيه بان ليس لها شكل معين ولا حجم معين وتتحول المادة من الحاله
الغازيه الى الحاله السائله وتسمى هذة العمليه بعملية التكثيف اما عند تحول المادة من
الحاله السائله الى الحاله الغازيه تسمى بعمليه التبخر.
أما الحالة الرابعة من المادة وهي " البلازما " وتتكون البلازما عبر مراحل تدريجية تتم بإرتفاع درجة الحرارة, حيث تتفكك جزيئات الغاز إلى ذرات في المرحلة الأولى. ثم يتبع ذلك في المرحلة الثانية تأيين لذرات الغازات نتيجة التصادمات التي تؤدي إلى إنطلاق الإلكترونات من المدارات الخارجية للذرات, وبذلك تتكون البلازما من خليط من الذرات المتعادلة والأيونات الموجبة والإلكترونات. والبلازما هي الحالة الشائعة للمادة في الكون حيث تشكل 99% من المادة. إلا أنها نادرة جداً على الأرض إلا في الحالات التي يقوم الإنسان بصنعها مثل " مصابيح الفلورنست ".
6-خصائص حالات المادة
الحالة الصلبة
1.تتحرك دقائقها حركة موضعية اهتزازية.
2.لها شكل ثابت.
3.لها حجم ثابت.
4.غير قابلة للانضغاط.
5.طاقتها الحركية قليلة.
الحالة السائلة
1.تتحرك دقائقها حركة انتقالية ودائمة وعشوائية.
2.تأخذ شكل الوعاء الذي يوضع فيه.
3.لها حجم ثابت.
4.صعبة الانضغاط.
5.قابلة للجريان.
6.طاقتها الحركية عالية.
الحالة الغازية
1.تتحرك دقائقها حركة انتقالية ودائمة وعشوائية وسريعة
وفي خطوط مستقيمة وبكافة الاتجاهات.
2.تأخذ شكل الوعاء الذي يوضع فيه.
3.حجمها يعتمد على حجم الوعاء الذي توضع فيه.
4.قابلة للانضغاط بسهولة.
5.تمتاز بخاصية الانتشار.
6.طاقتها الحركية عالية جداً.
تغير الحالة الفيزيائية
7-حالات تحول المادة
الانصهار
هو تحول المادة بالحرارة من الحاله الصلبه الى الحاله السائلة وتتميز المواد الصلبه
بان قوة الترابط الجزيئية تكون كبيرة جدا والمسافات البينية تكون صغيرة جدا
وتهتز الجزيئات فى مكانها ولاتتحرك من مكانها لذلك تحتفظ المواد الصلبه بشكل
ثابت وحجم ثابت وعند تسخين المادة الصلبه اى تزويد جزيئاتها بالحرارة فأنها
تهتز بسرعة أكبر للتغلب على قوة التجاذب بين هذة الجزيئات بمساعدة الحرارة التى
تكتسبها من التسخين وعند درجة حرارة معينه تسمى درجة الانصهار تتغلب الجزيئات على
قوة التماسك بينها وتتحرك من مواضعها فتتحول المادة من الحالة الصلبة الى الحالة
السائلة فيما يعرف بالانصهار.
التصعيد أو التبخر
هو تحول المادة بالحرارة من الحاله السائله الى الحاله الغازيه وتتحرك جزيئات السائل
حركه مستمرة ولكنها لاتبتعد كثيرا من بعضها ونلاحظ ان قوة الترابط الجزيئيه فى هذة
الحاله صغيرة جدا
8-الجزئ
هــو وحــدة بنــاء المـــادة وهو اصغــر جزء من المـــادة يمكـــن ان يوجــد منفـــــردا ويظل
محتفظـــــا بخـواص المــــادة وصفاتهــــا ونلاحـــــظ ان جزيئـات المـــــادة فى حالة حركـــــه
مستمـــرة هذة الحركه أكبـــــر ما يمكــــن تكــــون فى حـالة المـــواد الغازيــــه ويتبعهــــا
السوائل أما جزيئــــات المواد الصلبـــــه فحركتهــا قليله جدا فهــــى تهتز فى مكانهــــــا فقط
بدون ان تنتقل إلى مكـــــان اخـــــر توجــــد مسافـــات بينيـه اى فراغـات بين جزيئــــات
9-المادة وتكون كألاتى:
المــواد الصلبـــه: تكون فيهــا المسافــــات البينيـه للجزيئـــات صغيرة جــدا
المواد السائلـــه :تكــون فيها المسافــات البينية للجزيئات متوسطة الحجم
الغــازات تكـــون فيهــــا المسافـــات البينيــه للجزيئـــــات كبيــرة جـــــــدا
والجــزئ يتكـــون من وحـــدة بنائيـــه اصغــــر منــــــه وتسمــــى الــــذرةونلاحـــظ ان
جـــزئ الاكســـجين يتكـــون من ارتبــــاط ذرتـــى اكســــجين وجــــزئ الهيـــــدروجين
يتكـــــون من ارتبــــاط ذرتــــى هيــــدروجــــين وجــــزئ المـــــاء يتكــــون من ارتبــــاط
ذرتـــــى هيدروجــــين مع ذرة اكســــجين وجــــزئ ملـــح الطعــــــام ويسميـــــه
العلمـــــــــاء كلــــوريد الصوديــــــوم يتكــــــون مـــن ارتبــــــاط ذرة صوديــــــوم مـــــــــع
ذرة كلـــــــــور.
ملاحظه :
إن التغير في الحالة الفيزيائية يحدث أيضاً عند تحول الماء السائل إلى بخار أو العكس.
وعند تغير الحالة الفيزيائية للمادة لايتغير تركيبها الكيميائي، ولكن التغير يحدث فقط للمسافة بين دقائقها وقوى التجاذب بينها.
فعند تسخين الثلج تهتز الدقائق أكثر وتزيد سرعتها ، وتأخذ الدقائق بالانزلاق على بعضها ، وتبدأ بالذوبان.
وعند تسخين الماء السائل تزداد سرعة الدقائق وتأخذ بالتصادم فيما بينها مما يوفر لبعض الدقائق الموجودة على سطح السائل طاقة حركية كافية فتهرب من السطح وتتحول إلى بخار.
10-تفسير بعض خصائص المادة
الانتشار
إذا فتح أحدهم غطاء زجاجة عطر في الغرفة التي أنت بها ، فإنك سرعان ما تشعر بذلك، فالرائحة تنتشر بسرعة خلال الغرفة، وتعرف من خلال حاسة الشم بالذي حصل.
الانتشار خاصية تمتاز بها الغازات وتحدث عند اختلاط دقائق الغاز ذاتياً بالهواء.
ولكن هل تنتشر جميع الغازات بنفس السرعة؟
الانضغاط
هل دقائق الغاز متباعدة أم متقاربة؟
هل قوى التجاذب بين دقائق الغاز كبيرة أم قليلة؟
هل سرعة دقائق الغاز عالية أم منخفضة؟
إن تعريض الغاز للضغط، يؤدي إلى تقارب الجزيئات فتزداد معه قوى التجاذب بين الدقائق وتتباطأ وقد تتحول بمزيد من الضغط إلى سائل.
فسر سبب كون المواد الصلبة غير قابلة للانضغاط؟
التكاثف
أيهما يملك طاقة حركية أكبر الماء السائل أم بخاره؟
ماذا يحدث إذا مر البخار فوق سطح بارد؟
تمتلك دقائق البخار طاقة حركية عالية، وعند تعرض البخار لسطح بارد تقل الطاقة الحركية لدقائقه وتتقارب ، وتزداد قوى التجاذب بينها وتتحول إلى سائل.
التبخر
هل يحدث التبخر عند درجة حرارة معينة، أم عند أي درجة حرارة؟
عند أي جزء من السائل يحدث التبخر؟
كيف يحدث التبخر؟
تتحرك دقائق السائل حركة دائمة وعشوائية وفي كافة الاتجاهات، وتسمى هذه الحركة بالحركة البراونية ( نسبة إلى مكتشفها روبرت براون ).
يحدث تصادم بين دقائق السائل بفعل الحركة البراونية مما يؤدي إلى فقدان بعض الدقائق لطاقتها الحركية واكتساب بعضها الآخر لتلك الطاقة، فإذا صادف أن اكتسبت إحدى الدقائق الموجودة على السطح طاقة كافية، فإنها تنفلت من سطح السائل وتتحول إلى بخار.
11-الخاتمة ::
الحمد لله الذي أتم عليَّ نعمه، ووالى عليَّ مننه، وأعانني فأكملت هذا البخث بهذه الصورة التي أرجو أن أنال بها رضاه،وأن يكون تقرير نافعاً محققاً للغرض منه،وقد توصلت من خلاله إلى عدة نتائج من أهمها:
1. يربط بين حالة المادة و خولصه العامة .
2. يوجد العلاقة بين خواص المادة وقوةالترابط بين مكوناتها..
3. وجود الحالة الرابعة معه الحالات ثلاث للمادة وتسمه البلازما .
raneem noor
العنصر و المركب و المخلوط
المخلوط : عباره عن عدة مواد مخلطه ببعضها البعض المواد الموجوده في المخلوط تحافظ على صفاتها ويمكن فصلها بطرق كيميائيه مختلفه هنالك نوعين من المخاليــط انــواع المخــاليط هي
1 - متــجانس : مخلوط يتكــون من مــادتين او اكثــر تظهــر كماده واحده مخــلوط كهذا يدعى محلول .
2- غيــر متجانس : مخــلوط من مادتيــن او اكثــر لكنــه لا يــظهر كمــاده واحــده .
العنــصر :عباره عن مواد نقيه مبنيه من نفس النوع من الذرات لا يمكن تحليلها الى ابسط منها .حتى لو اجرينــا على العنصر عملية كيميائيه او فيزيائيه لا يتحول هذا العنصر الى مواد جديده وانما يبقى كما هو .
للعنـــصر نوعين :
عنـــصر طبيعي : موجود في الطبيعه مثــل النحـــاس , الحديد .
عنــــصر صنــاعي : تحضر فــي المختبــرات مثــل المغنيزيوم .
المــركــب : هــو عباره عــن مــاده مكــونه مــن عنــاصر (ذرات مختلــفه ) مــثال : المــــاء عباره عـــن مركب مكــتون من ذرتــين هيدروجيــن وذرة اكســـجين واحده .
صــدأ الحديد هـــو مركب ايضـــا مــركب من حديــد واكســجين
مـــلاحظه : المـــركب يختلــف في صفاته عــن صفـــات المواد التـــي تكونه
مـــثال : الماء هو مــاده غير قابله للأشتعال لكنهــا تتركب من الاوكسجيــن والاوكسجــين
مـــاده قـــابلــه للأشتــعال .
شوق المرشدي
المخلوط : عباره عن عدة مواد مخلطه ببعضها البعض المواد الموجوده في المخلوط تحافظ على صفاتها ويمكن فصلها بطرق كيميائيه مختلفه هنالك نوعين من المخاليــط انــواع المخــاليط هي
1 - متــجانس : مخلوط يتكــون من مــادتين او اكثــر تظهــر كماده واحده مخــلوط كهذا يدعى محلول .
2- غيــر متجانس : مخــلوط من مادتيــن او اكثــر لكنــه لا يــظهر كمــاده واحــده .
العنــصر :عباره عن مواد نقيه مبنيه من نفس النوع من الذرات لا يمكن تحليلها الى ابسط منها .حتى لو اجرينــا على العنصر عملية كيميائيه او فيزيائيه لا يتحول هذا العنصر الى مواد جديده وانما يبقى كما هو .
للعنـــصر نوعين :
عنـــصر طبيعي : موجود في الطبيعه مثــل النحـــاس , الحديد .
عنــــصر صنــاعي : تحضر فــي المختبــرات مثــل المغنيزيوم .
المــركــب : هــو عباره عــن مــاده مكــونه مــن عنــاصر (ذرات مختلــفه ) مــثال : المــــاء عباره عـــن مركب مكــتون من ذرتــين هيدروجيــن وذرة اكســـجين واحده .
صــدأ الحديد هـــو مركب ايضـــا مــركب من حديــد واكســجين
مـــلاحظه : المـــركب يختلــف في صفاته عــن صفـــات المواد التـــي تكونه
مـــثال : الماء هو مــاده غير قابله للأشتعال لكنهــا تتركب من الاوكسجيــن والاوكسجــين
مـــاده قـــابلــه للأشتــعال .
شوق المرشدي
طوات الطريقة العلمية
نذكر فيما يلي أمثلة لمكونات سلوكية أساسية تتضمنها خطوات الطريقة العلمية، وهي ذات فائدة للمعلم وللباحث المتخصص على حد سواء في أكثر من ناحية، ويتناول القسم الأول من التحليل القدرات والمهارات المتضمنة في خطوات الطريقة العلمية، بينما يتناول القسم الثاني الاتجاهات العلمية . وطبيعي أن هذا التنظيم قُصِد به التبسيط لأن الاتجاهات العلمية في الواقع يصعُب فصلها عن القدرة على التفكير العلمي وممارسة الطريقة العلمية .
* أولاً: القدرات والمهارات المُتضمنة في خطوات التفكير العلمي:
تشمل خطوات التفكير العلمي المكونات السلوكية التالية :
* الشعور بالمشكلة وتحديدها:
يشمل إدراك مشكلة في سياق عبارة أو مقال أو حدث، والتمييز بين المشكلات الهامة وغير الهامة، والتركيز على المشكلة الأساسية وتحديدها في عبارات واضحة، وتحليل المشكلة إلى عناصرها الرئيسية، والدقة في تعريف المصطلحات الهامة المتضمنة في العبارة أو العبارات التي تصوغ المشكلة .
* جمع المعلومات المتصلة بالمشكلة:
استخدام مراجع ومصادر متعددة موثوق بصحتها في جمع البيانات والمعلومات، وإجراء المقابلات الشخصية المقننة والمفتوحة وإجراء التجارب للحصول على معلومات معينة، والتمييز بين مصادر المعلومات الموثوق في صحتها والتي يُعتمد عليها والمصادر التي لا يُعتمد عليها، والمعلومات المتصلة بالمشكلة وغير المتصلة بها . والتمييز بين الحقائق والملاحظات والفروض المقترحة كحل للمشكلة .
* فرض الفروض الممكنة واختيار أنسبها:
إدراك أن الفروض حلول ممكنة تخضع للاختبارات والتجريب وأنها ليست حلولاً نهائية للمشكلة، والتمييز بين الفرض والافتراض والحقيقة، وتقدير قيمة الفروض المقترحة بالنسبة للمشكلة واختيار أنسب هذه الفروض للبدء باختباره. وصياغة الفرض في عبارات يسهُل فهمها واختبار صحتها . والتمييز بين الفروض الجيدة التي تتفق مع الحقائق والوقائع وبين الفروض الضعيفة التي لا تتفق معها .
* اختبار صحة الفروض:
تصميم تجارب محكمة الضبط لاختبار صحة الفروض المُقترحة، وإدراك العامل أو العوامل المتغيرة في التجربة التي تتطلب الضبط، وإدراك أن هناك بعض الأخطاء المحتملة في أدوات ووسائل القياس، وتحديد قيمة هذا الخطأ عند استخدامها في الحصول على بيانات، والتمييز بين الملاحظات الهامة والأقل أهمية وغير الهامة أثناء التجريب .
* تفسير البيانات والوصول إلى حل للمشكلة:
كسب المهارات الأساسية اللازمة للتفسير مثل تنظيم البيانات في جداول ورسوم بيانية، والقدرة على قراءة الجداول والرسومات البيانية وغيرها، والقدرة على إجراء بعض العمليات الرياضية والإحصائية البسيطة، وتفسير البيانات الإحصائية، والتمييز بين الفرض والنتيجة والافتراض، وصياغة حل أو حلول المشكلة في عبارات دقيقة مفهومة .
* استخدام النتائج أو التعميمات في مواقف جديدة:
يُراعى أن تكون النتائج والأحكام التي نتوصل إليها في البحث في حدود الأدلة المتوفرة في البحث، وإدراك أوجه الشبة والاختلاف بين المواقف الجديدة والموقف المعين في البحث. وإدراك أن التعميمات التي نتوصل إليها في بحث معين لا تمتد إلى مواقف جديدة وتنطبق عليها إلا إذا كان هناك قدر كاف من التشابه بين هذه المواقف الجديدة ومواقف البحث .
ومعرفة أن التنبؤات بالنسبة للمواقف الجديدة تخضع للتجربة والتحقق حتى ولو كانت الظروف التي تُستخدم فيها النتائج أو التعميمات متشابهة مع المواقف في البحث .
* ثانياً: الاتجاهات العلمية المُتضمنة في خطوات التفكير العلمي:
يتصف الشخص ذو الاتجاهات العلمية بالخصائص السلوكية التالية :
* اتساع الأفق العقلي وتفتح العقلية:
تحرر العقل والتفكير من التحيز والجمود، والخرافات والقيود التي تفرض على الشخص أفكاراً خاطئة وأنماطاً غير سليمة من التفكير . والإصغاء إلى آراء الآخرين وتفهُّم هذه الآراء واحترامها حتى لو تعارضت مع آرائه الشخصية أو خالفها تماماً . ورحابة صدر الباحث وتقبُّل النقد الموجه إلى آرائه من الآخرين، والاستعداد لتغيير أو تعديل الفكرة أو الرأي إذا ثبُت خطأها في ضوء ما يستجد من حقائق وأدلة مقنعة وصحيحة، والاعتقاد في نسبية الحقيقة العلمية، وأن الحقائق التي نتوصل إليها في البحث العلمي ليست مطلقة ونهائية .
* حب الاستطلاع والرغبة المستمرة في التعلم:
الرغبة في البحث عن إجابات وتفسيرات مقبولة لتساؤلاته عما يحدث أو يوجد حوله من أحداث وأشياء وظواهر مختلفة، والمثابرة والرغبة المستمرة في زيادة معلوماته وخبراته، واستخدام مصادر متعددة لهذا الغرض ومنها الاستفادة من خبرات الآخرين .
* البحث وراء المسببات الحقيقية للأحداث والظواهر:
الاعتقاد بأن لأي حدث أو ظاهرة مسببات ووجوب دراسة الأحداث والظواهر التي يدركها الباحث من حوله ويبحث عن مسبباتها الحقيقية، وعدم الاعتقاد في الخرافات، وعدم المبالغة في دور الصدفة، وعدم الاعتقاد في ضرورة وجود علاقة سببية بين حدثين معينين لمجرد حدوثهما في نفس الوقت أو حدوث أحدهما بعد الآخر .
* توخي الدقة وكفاية الأدلة للوصول إلى القرارات والأحكام:
الدقة في جمع الأدلة والملاحظات من مصادر متعددة موثوق بها وعدم التسرع في الوصول إلى القرارات والقفز إلى النتائج ما لم تدعمها الأدلة والملاحظات الكافية. واستخدام معايير الدقة والموضوعية والكفاية في تقدير ما يجمعه من أدلة وملاحظات .
* الاعتقاد في أهمية الدور الاجتماعي للعلم والبحث العلمي:
الإيمان بدور العلم والبحث العلمي في إيجاد حلول علمية لما تواجه المجتمعات من مشكلات وتحديات في مختلف المجالات التربوية والاقتصادية والصحية .. ، والإيمان بأن العلم لا يتعارض مع الأخلاق والقيم الدينية، وتوجيه العلم والبحث العلمي إلى ما يحقق سعادة ورفاهية البشرية في كل مكان .
Hأنواع البحوثA
هناك أكثر من أساس يمكن أن نبني عليه تقسيم البحوث، فقد تُقسم على أساس الظواهر التي تدرسها إلى : بحوث طبيعية، وبحوث بيولوجية، وبحوث اجتماعية . والواقع أنه ليس هناك فصل تام بين هذه الأقسام، فقد يكون هناك بحوث طبيعية بيولوجية، وبحوث بيولوجية اجتماعية.
والبعض يختصر هذه التقسيمات إلى نوعين رئيسين هما البحوث الطبيعية، والبحوث السلوكية، ويدخل تحت هذا النوع الأخير البحوث التربوية والنفسية .
وسوف نذكر فيما يلي تقسيمين من أكثر التقسيمات شيوعاً واستخداماً وعلى الأخص في المجالات التربوية والنفسية .
1 ـ تقسيم البحوث حسب طبيعتها والدوافع إلى البحث إلى نوعين رئيسين هما:
(أ) ـ بحوث أساسية أو بحتة : Pure or Basic Research
(ب) ـ بحوث تطبيقية : Applied Research
والبحوث الأساسية أو البحتة وهي تُسمى أحياناً بالبحوث النظرية لتشير إلى النشاط العلمي الذي يكون غرضه المباشر والقريب إلى حقائق وقوانين علمية ونظريات محققة. وهو بذلك يسهم في نمو المعرفة العلمية وفي تحقيق فهم أشمل وأعمق لها بصرف النظر عن الاهتمام بالتطبيقات العلمية لهذه المعرفة.
وأما البحوث التطبيقية فتشير إلى النشاط العلمي الذي يكون الغرض الأساسي والمباشر منه تطبيق المعرفة العلمية المتوفرة، أو التوصل إلى معرفة لها قيمتها وفائدتها العملية في حل بعض المشكلات الآنية المُلحّة. وهذا النوع من البحوث له قيمته في حل المشكلات الميدانية وتطوير أساليب العمل وإنتاجيته في المجالات التطبيقية كالتربية والتعليم، والصحة، والزراعة، والصناعة .. الخ.
2 ـ وتُقسم البحوث حسب مناهج البحث والأساليب المستخدمة فيها إلى أنواع ثلاثة رئيسة هي :
(أ) بحوث وصفية Descriptive research
(ب) بحوث تاريخية Historical research
(ج) بحوث تجريبية Experimental research
وتهدف البحوث الوصفية إلى وصف ظواهر أو أحداث معينة وجمع الحقائق والمعلومات عنها ووصف الظروف الخاصة بها وتقرير حالتها كما توجد عليه في الواقع . وفي كثير من الحالات لا تقف البحوث الوصفية عند حد الوصف أو التشخيص الوصفي، وتهتم أيضاً بتقرير ما ينبغي أن تكون عليه الظواهر أو الأحداث التي يتناولها البحث .
وذلك في ضوء قيم أو معايير معينة، واقتراح الخطوات أو الأساليب التي يمكن أن تُتبع للوصول بها إلى الصورة التي ينبغي أن تكون عليه في ضوء هذه المعايير أو القيم .
ويُستخدم لجمع البيانات والمعلومات في أنواع البحوث الوصفية أساليب ووسائل متعددة مثل الملاحظة، والمقابلة، والاختبارات، والاستفتاءات .
والبحوث التاريخية لها أيضاً طبيعتها الوصفية فهي تصف وتسجل الأحداث والوقائع التي جرت وتمت في الماضي، ولكنها لا تقف عند مجرد الوصف والتأريخ لمعرفة الماضي فحسب، وإنما تتضمن تحليلاً وتفسيراً للماضي بغية اكتشاف تعميمات تساعدنا على فهم الحاضر بل والتنبؤ بأشياء وأحداث في المستقبل . ويركز البحث التاريخي عادة على التغير والتطور في الأفكار والاتجاهات والممارسات لدى الأفراد أو الجماعات أو المؤسسات الاجتماعية المختلفة.
ويستخدم الباحث التاريخي نوعين من المصادر للحصول على المادة العلمية وهما المصادر الأولية والثانوية، وهو يبذل أقصى جهده للحصول على هذه المادة من مصادرها الأولية كلما أمكن ذلك .
وأما البحوث التجريبية فهي التي تبحث المشكلات والظواهر على أساس من المنهج التجريبي أو منهج البحث العلمي القائم على الملاحظة وفرض الفروض والتجربة الدقيقة المضبوطة للتحقق من صحة هذه الفروض . ولعل أهم ما تتميز به البحوث التجريبية على غيرها من أنواع البحوث الوصفية والتاريخية هو كفاية الضبط للمتغيرات والتحكم فيها عن قصد من جانب الباحث.
وتعتبر التجربة العلمية مصدراً رئيسياً للوصول إلى النتائج أو الحلول بالنسبة للمشكلات التي يدرسها البحث التجريبي، ولكن في نفس الوقت تستخدم المصادر الأخرى في الحصول على البيانات والمعلومات التي يحتاج إليها البحث بعد أن يُخضعها الباحث للفحص الدقيق والتحقق من صحتها وموضوعيتها .
المشكلة في البحث التربوي
يناقش هذا الموضوع النقاط التالية:
ـ مصادر الحصول على المشكلة.
ـ اختيار المشكلة وتقويمها.
ـ وضع خطة لبحث المشكلة.
أولاً : مصادر الحصول على المشكلة
من المُسلّم به أنه ما لم يتوفر للبحث مشكلة واضحة محددة مُلحة فإن كل عمل يقوم به الباحث سوف يكون مشكوكاً في قيمته، وكيف يمكن أن نتصور قيام بناء جيد على أساس غير سليم؟ ويمكن القول أن مرحلة اختيار الباحث لمشكلة تربوية تصلح للبحث والدراسة من أهم مراحل البحث التربوي.
لذلك نحاول التعرف فيما يلي على بعض المصادر التي تنمي لدى الباحث حساسية بالمشكلات التربوية، والتي عن طريقها يمكن أن يتوصل إلى مشكلة مناسبة للبحث :
1 ـ التخصص :
تخصص الباحث في مجال معين يوفر له خبرة بمشكلات هذا المجال سواء تلك التي تم بحثها ودراستها، أو المشكلات التي لم تُدرس بعد، وكلما اتصفت هذه الخبرة بالعمق والشمول كلما ساعدته في فهم أبعاد هذه المشكلات.
فالمعلمة المتخصصة في تدريس الرياضيات في المرحلة التأسيسية هي الأكثر دراية بالمشكلات المُلحّة التي تواجه تدريس الرياضيات في هذه المرحلة.
2 ـ برامج الدراسات العليا:
وتتمثل في البرامج التي توفرها الجامعات لطلاب البحوث، وقد تستغرق فترة دراسة هذه البرامج عام دراسي أو أكثر.
وتشتمل هذه البرامج على دراسات نظرية وأخرى تطبيقية (منها: مقررات مناهج البحث، والإحصاء وحلقات البحث، وعلوم الحاسب الآلي.. ) تزود الطالب بخلفية علمية لا تمكنه فقط من اختيار مشكلة البحث بل تفيده في جميع مراحل إعداد البحث.
ويتخلل هذه البرامج عرض خطط البحث التي يقترحها الباحثون ومناقشتها وتقويمها من جانب الأساتذة وزملائهم المشاركين في السيمنار (حلقة المناقشة)، وكل هذه النشاطات تساهم في زيادة حساسية الطالب لمشكلات المجال الذي يهم بالبحث فيه.
3 ـ الخبرة العملية:
الخبرة العملية كالعمل في ميدان التدريس مثلاً لفترة كافية تلعب دوراً هاماً في الإحساس ببعض المشكلات المُلحّة في واقع الميدان والحاجة إلى دراسات للتوصل إلى حلول علمية لها. فكل مدرس يواجه مشكلات يومية داخل حجرة الدراسة وخارجها ترتبط بما يُدرِّسه من مقررات وأساليب تدريسها وتقويمها، وكيفية الاستفادة من مستحدثات التكنولوجيا في رفع كفاية التدريس.
كما أن المشكلة التي يختارها الباحث بنفسه في ضوء خبرته العملية كثيراً ما يكون لها أهمية عند الباحث، الأمر الذي يجعله مثابراً خلال بحثه في محاولة الوصول إلى حلول واقعية لها.
4 ـ الدراسة المسحية للبحوث السابقة والجارية:
تساهم دراسة البحوث السابقة والجارية في الميدان في معرفة المشكلات التي بُحثت، والدراسة التحليلية لهذه البحوث أو ملخصاتها يمكن أن تكشف للطالب عن نواحي النقص في الدراسات السابقة والتي ما زالت تحتاج إلى إجراء بحوث حولها.
كما أن كثيراً من هذه البحوث تشتمل في نهاياتها على توصيات ومقترحات بإجراء بحوث معينة ترتبط بمشكلة البحث، وهذا لا يساعد الطالب فقط في اختيار مشكلة لبحثه، بل وتمنع من تكرار دراسة المشكلات التي سبق دراستها.
وفي بعض الحالات تنتهي البحوث بنتائج غير مؤكدة لعدم توافر البيانات، أو أن النتائج قامت على بيانات محدودة كأن تكون عينة البحث صغيرة جداً، ويمكن في هذه الحالات إجراء بحوث تُستخدم فيها عينات كبيرة وممثلة إلى حد كبير لمجتمعها الأصلي.
جدير بالذكر أن إجراء بحث بحيث يأتي صورة طبق الأصل لبحوث سابقة أمر غير مرغوب فيه، لكن في بعض الحالات قد تكون المشكلة ذات أهمية بحيث تحتاج إلى أكثر من بحث واحد للوصول إلى نتائج يُعتمد عليها.
ثانياً : اختيار المشكلة وتقويمها
هناك عدة اعتبارات لا بد أن يراعيها الباحث المبتدئ قبل اختياره لمشكلة بحثه، وترتبط هذه الاعتبارات بالجوانب التالية:
1 ـ حداثة المشكلة:
يجب أن تكون المشكلة جديدة ومبتكرة ولم يسبق دراستها من جانب باحثين آخرين، لكن هذا لا يعني أن جميع المشكلات التي سبق دراستها لم تعد جديرة بالبحث مرة أخرى.
ففي ضوء التطورات المعرفية والثقافية تأخذ المشكلات التربوية أبعاداً مختلفة، ويُعتبر تكرار بعض البحوث السابقة باستخدام تصميمات وأساليب وأدوات جديدة للبحث من الأعمال ذات القيمة العلمية.
2 ـ أهمية المشكلة وقيمتها العملية:
يساعد في تحديد أهمية المشكلة وقيمتها بحث عدد من التساؤلات هي:
ـ هل يُحتمل أن تضيف نتائج بحث المشكلة شيئاً جديداً إلى المعرفة العلمية الحاضرة ؟ أو لها تأثير مباشر في الممارسات التربوية الحالية في ميدان التربية والتعليم ؟
ـ هل يحتاج المجال إلى دراسات من هذا النوع ؟
ـ هل توجد نواحي نقص معينة في المعرفة الحالية ـ في مجال البحث ـ ويلزم إجراء بحوث لاستكمال هذا النقص ؟
ويحتاج الميدان التربوي إلى بحوث ذات قيمة عملية أو تطبيقية مباشرة. وهذا يتطلب أن يدرس الباحث المشكلات الموجودة فعلاً في الواقع التعليمي.
وعلى سبيل المثال هناك حاجة إلى بحوث في مجالات: نقص دافعية المتعلمين، واستخدام تكنولوجيا التعليم في التدريس، ومشكلات الرسوب والفاقد في التعليم.
3 ـ اهتمام الباحث بالمشكلة:
إن دراسة الباحث لمشكلة تحظى باهتمامه الشخصي تجعله أكثر مثابرة وصبراً واستمتاعاً بالبحث حتى إتمامه، وذلك لأن دافعيته وميله الذاتي للعمل يكون أكبر، وتزداد احتمالات تحقيق النجاح في البحث. ويتطلب هذا من طالب البحث أن يسأل نفسه أسئلة كالتالي:
ـ هل موضوع البحث يشبع الميول والدوافع الحقيقية في نفسي؟
ـ هل دافعي واهتمامي بإجراء البحث هو مجرد رغبتي في الحصول على درجة علمية أو امتيازات أدبية ومادية، وحتى لو كان موضوع البحث لا يتوفر له درجة اهتمام كافية من ناحيتي؟
وبالطبع ينبغي ألا يختار الطالب مشكلة معينة لكي يُدعِّم وجهة نظر يؤمن بها مسبقاً ومتحيز لها. كأن يكون مقتنعاً بأهمية "الاختلاط بين الجنسين في الجامعة" فيجري البحث لكي يؤكد صحة هذه الفكرة بغض النظر عما إذا جاءت النتائج مُدعمة لوجهة نظره أو مخالفة لها.
4 ـ كفاية خبرات الباحث وقدراته على بحث المشكلة:
ينبغي أن يتوفر لدى الطالب المهارات والقدرات اللازمة لدراسة المشكلة وإتمام البحث. ومن الأسئلة التي يمكن أن يوجهها الطالب لنفسه في هذا المجال ما يلي:
ـ هل يتوفر لي الخبرات اللازمة لدراسة المشكلة التي اخترتها؟
ـ ما هي المهارات والمعارف التي تنقصني لدراسة المشكلة؟
ففي كثير من الحالات قد يختار الباحث مشكلة معينة لبحثها وبعد أن يقطع في بحثه جزءاً كبيراً يكتشف أن خبرته وقدراته البحثية لا تمكنه من دراسة المشكلة على الوجه الأمثل، أو أنه غير قادر على إنجاز الجوانب الإحصائية الخاصة بنتائج البحث وتفسيرها.
5 ـ توفر البيانات ومصدرها:
ينبغي أن يضع الباحث عند اختياره لمشكلة البحث مدى إمكانية الحصول على البيانات اللازمة لدراسة المشكلة، فقد يكون الحصول على البيانات صعباً بسبب بعد مصادرها، أو لاعتبارات سياسية أو اجتماعية . ولذا ينبغي أن يسأل الباحث نفسه من البداية أسئلة منها:
ـ هل البيانات اللازمة للبحث يسهل الحصول عليها؟
ـ إذا كانت هناك صعوبات في الحصول على بيانات معينة، فهل يمكن تحديد مشكلة البحث وجعله في حدود البيانات المتاحة والممكن توفيرها؟
6 ـ الإشراف والوقت والتكلفة:
على الطالب أن يختار مشكلة بحثية يمكن أن يجد الأستاذ المتخصص في مجال هذه المشكلة . كما أن عليه ألا يختار مشكلة واسعة يحتاج إلى وقت طويل جداً لدراستها. وعليه أيضاً في اختياره لمشكلة بحثه التكاليف التي يحتاج إليها تنفيذ البحث وإلى أي مدى يمكن أن يوفرها في حدود إمكاناته المالية المتاحة؟
raneem noor
نذكر فيما يلي أمثلة لمكونات سلوكية أساسية تتضمنها خطوات الطريقة العلمية، وهي ذات فائدة للمعلم وللباحث المتخصص على حد سواء في أكثر من ناحية، ويتناول القسم الأول من التحليل القدرات والمهارات المتضمنة في خطوات الطريقة العلمية، بينما يتناول القسم الثاني الاتجاهات العلمية . وطبيعي أن هذا التنظيم قُصِد به التبسيط لأن الاتجاهات العلمية في الواقع يصعُب فصلها عن القدرة على التفكير العلمي وممارسة الطريقة العلمية .
* أولاً: القدرات والمهارات المُتضمنة في خطوات التفكير العلمي:
تشمل خطوات التفكير العلمي المكونات السلوكية التالية :
* الشعور بالمشكلة وتحديدها:
يشمل إدراك مشكلة في سياق عبارة أو مقال أو حدث، والتمييز بين المشكلات الهامة وغير الهامة، والتركيز على المشكلة الأساسية وتحديدها في عبارات واضحة، وتحليل المشكلة إلى عناصرها الرئيسية، والدقة في تعريف المصطلحات الهامة المتضمنة في العبارة أو العبارات التي تصوغ المشكلة .
* جمع المعلومات المتصلة بالمشكلة:
استخدام مراجع ومصادر متعددة موثوق بصحتها في جمع البيانات والمعلومات، وإجراء المقابلات الشخصية المقننة والمفتوحة وإجراء التجارب للحصول على معلومات معينة، والتمييز بين مصادر المعلومات الموثوق في صحتها والتي يُعتمد عليها والمصادر التي لا يُعتمد عليها، والمعلومات المتصلة بالمشكلة وغير المتصلة بها . والتمييز بين الحقائق والملاحظات والفروض المقترحة كحل للمشكلة .
* فرض الفروض الممكنة واختيار أنسبها:
إدراك أن الفروض حلول ممكنة تخضع للاختبارات والتجريب وأنها ليست حلولاً نهائية للمشكلة، والتمييز بين الفرض والافتراض والحقيقة، وتقدير قيمة الفروض المقترحة بالنسبة للمشكلة واختيار أنسب هذه الفروض للبدء باختباره. وصياغة الفرض في عبارات يسهُل فهمها واختبار صحتها . والتمييز بين الفروض الجيدة التي تتفق مع الحقائق والوقائع وبين الفروض الضعيفة التي لا تتفق معها .
* اختبار صحة الفروض:
تصميم تجارب محكمة الضبط لاختبار صحة الفروض المُقترحة، وإدراك العامل أو العوامل المتغيرة في التجربة التي تتطلب الضبط، وإدراك أن هناك بعض الأخطاء المحتملة في أدوات ووسائل القياس، وتحديد قيمة هذا الخطأ عند استخدامها في الحصول على بيانات، والتمييز بين الملاحظات الهامة والأقل أهمية وغير الهامة أثناء التجريب .
* تفسير البيانات والوصول إلى حل للمشكلة:
كسب المهارات الأساسية اللازمة للتفسير مثل تنظيم البيانات في جداول ورسوم بيانية، والقدرة على قراءة الجداول والرسومات البيانية وغيرها، والقدرة على إجراء بعض العمليات الرياضية والإحصائية البسيطة، وتفسير البيانات الإحصائية، والتمييز بين الفرض والنتيجة والافتراض، وصياغة حل أو حلول المشكلة في عبارات دقيقة مفهومة .
* استخدام النتائج أو التعميمات في مواقف جديدة:
يُراعى أن تكون النتائج والأحكام التي نتوصل إليها في البحث في حدود الأدلة المتوفرة في البحث، وإدراك أوجه الشبة والاختلاف بين المواقف الجديدة والموقف المعين في البحث. وإدراك أن التعميمات التي نتوصل إليها في بحث معين لا تمتد إلى مواقف جديدة وتنطبق عليها إلا إذا كان هناك قدر كاف من التشابه بين هذه المواقف الجديدة ومواقف البحث .
ومعرفة أن التنبؤات بالنسبة للمواقف الجديدة تخضع للتجربة والتحقق حتى ولو كانت الظروف التي تُستخدم فيها النتائج أو التعميمات متشابهة مع المواقف في البحث .
* ثانياً: الاتجاهات العلمية المُتضمنة في خطوات التفكير العلمي:
يتصف الشخص ذو الاتجاهات العلمية بالخصائص السلوكية التالية :
* اتساع الأفق العقلي وتفتح العقلية:
تحرر العقل والتفكير من التحيز والجمود، والخرافات والقيود التي تفرض على الشخص أفكاراً خاطئة وأنماطاً غير سليمة من التفكير . والإصغاء إلى آراء الآخرين وتفهُّم هذه الآراء واحترامها حتى لو تعارضت مع آرائه الشخصية أو خالفها تماماً . ورحابة صدر الباحث وتقبُّل النقد الموجه إلى آرائه من الآخرين، والاستعداد لتغيير أو تعديل الفكرة أو الرأي إذا ثبُت خطأها في ضوء ما يستجد من حقائق وأدلة مقنعة وصحيحة، والاعتقاد في نسبية الحقيقة العلمية، وأن الحقائق التي نتوصل إليها في البحث العلمي ليست مطلقة ونهائية .
* حب الاستطلاع والرغبة المستمرة في التعلم:
الرغبة في البحث عن إجابات وتفسيرات مقبولة لتساؤلاته عما يحدث أو يوجد حوله من أحداث وأشياء وظواهر مختلفة، والمثابرة والرغبة المستمرة في زيادة معلوماته وخبراته، واستخدام مصادر متعددة لهذا الغرض ومنها الاستفادة من خبرات الآخرين .
* البحث وراء المسببات الحقيقية للأحداث والظواهر:
الاعتقاد بأن لأي حدث أو ظاهرة مسببات ووجوب دراسة الأحداث والظواهر التي يدركها الباحث من حوله ويبحث عن مسبباتها الحقيقية، وعدم الاعتقاد في الخرافات، وعدم المبالغة في دور الصدفة، وعدم الاعتقاد في ضرورة وجود علاقة سببية بين حدثين معينين لمجرد حدوثهما في نفس الوقت أو حدوث أحدهما بعد الآخر .
* توخي الدقة وكفاية الأدلة للوصول إلى القرارات والأحكام:
الدقة في جمع الأدلة والملاحظات من مصادر متعددة موثوق بها وعدم التسرع في الوصول إلى القرارات والقفز إلى النتائج ما لم تدعمها الأدلة والملاحظات الكافية. واستخدام معايير الدقة والموضوعية والكفاية في تقدير ما يجمعه من أدلة وملاحظات .
* الاعتقاد في أهمية الدور الاجتماعي للعلم والبحث العلمي:
الإيمان بدور العلم والبحث العلمي في إيجاد حلول علمية لما تواجه المجتمعات من مشكلات وتحديات في مختلف المجالات التربوية والاقتصادية والصحية .. ، والإيمان بأن العلم لا يتعارض مع الأخلاق والقيم الدينية، وتوجيه العلم والبحث العلمي إلى ما يحقق سعادة ورفاهية البشرية في كل مكان .
Hأنواع البحوثA
هناك أكثر من أساس يمكن أن نبني عليه تقسيم البحوث، فقد تُقسم على أساس الظواهر التي تدرسها إلى : بحوث طبيعية، وبحوث بيولوجية، وبحوث اجتماعية . والواقع أنه ليس هناك فصل تام بين هذه الأقسام، فقد يكون هناك بحوث طبيعية بيولوجية، وبحوث بيولوجية اجتماعية.
والبعض يختصر هذه التقسيمات إلى نوعين رئيسين هما البحوث الطبيعية، والبحوث السلوكية، ويدخل تحت هذا النوع الأخير البحوث التربوية والنفسية .
وسوف نذكر فيما يلي تقسيمين من أكثر التقسيمات شيوعاً واستخداماً وعلى الأخص في المجالات التربوية والنفسية .
1 ـ تقسيم البحوث حسب طبيعتها والدوافع إلى البحث إلى نوعين رئيسين هما:
(أ) ـ بحوث أساسية أو بحتة : Pure or Basic Research
(ب) ـ بحوث تطبيقية : Applied Research
والبحوث الأساسية أو البحتة وهي تُسمى أحياناً بالبحوث النظرية لتشير إلى النشاط العلمي الذي يكون غرضه المباشر والقريب إلى حقائق وقوانين علمية ونظريات محققة. وهو بذلك يسهم في نمو المعرفة العلمية وفي تحقيق فهم أشمل وأعمق لها بصرف النظر عن الاهتمام بالتطبيقات العلمية لهذه المعرفة.
وأما البحوث التطبيقية فتشير إلى النشاط العلمي الذي يكون الغرض الأساسي والمباشر منه تطبيق المعرفة العلمية المتوفرة، أو التوصل إلى معرفة لها قيمتها وفائدتها العملية في حل بعض المشكلات الآنية المُلحّة. وهذا النوع من البحوث له قيمته في حل المشكلات الميدانية وتطوير أساليب العمل وإنتاجيته في المجالات التطبيقية كالتربية والتعليم، والصحة، والزراعة، والصناعة .. الخ.
2 ـ وتُقسم البحوث حسب مناهج البحث والأساليب المستخدمة فيها إلى أنواع ثلاثة رئيسة هي :
(أ) بحوث وصفية Descriptive research
(ب) بحوث تاريخية Historical research
(ج) بحوث تجريبية Experimental research
وتهدف البحوث الوصفية إلى وصف ظواهر أو أحداث معينة وجمع الحقائق والمعلومات عنها ووصف الظروف الخاصة بها وتقرير حالتها كما توجد عليه في الواقع . وفي كثير من الحالات لا تقف البحوث الوصفية عند حد الوصف أو التشخيص الوصفي، وتهتم أيضاً بتقرير ما ينبغي أن تكون عليه الظواهر أو الأحداث التي يتناولها البحث .
وذلك في ضوء قيم أو معايير معينة، واقتراح الخطوات أو الأساليب التي يمكن أن تُتبع للوصول بها إلى الصورة التي ينبغي أن تكون عليه في ضوء هذه المعايير أو القيم .
ويُستخدم لجمع البيانات والمعلومات في أنواع البحوث الوصفية أساليب ووسائل متعددة مثل الملاحظة، والمقابلة، والاختبارات، والاستفتاءات .
والبحوث التاريخية لها أيضاً طبيعتها الوصفية فهي تصف وتسجل الأحداث والوقائع التي جرت وتمت في الماضي، ولكنها لا تقف عند مجرد الوصف والتأريخ لمعرفة الماضي فحسب، وإنما تتضمن تحليلاً وتفسيراً للماضي بغية اكتشاف تعميمات تساعدنا على فهم الحاضر بل والتنبؤ بأشياء وأحداث في المستقبل . ويركز البحث التاريخي عادة على التغير والتطور في الأفكار والاتجاهات والممارسات لدى الأفراد أو الجماعات أو المؤسسات الاجتماعية المختلفة.
ويستخدم الباحث التاريخي نوعين من المصادر للحصول على المادة العلمية وهما المصادر الأولية والثانوية، وهو يبذل أقصى جهده للحصول على هذه المادة من مصادرها الأولية كلما أمكن ذلك .
وأما البحوث التجريبية فهي التي تبحث المشكلات والظواهر على أساس من المنهج التجريبي أو منهج البحث العلمي القائم على الملاحظة وفرض الفروض والتجربة الدقيقة المضبوطة للتحقق من صحة هذه الفروض . ولعل أهم ما تتميز به البحوث التجريبية على غيرها من أنواع البحوث الوصفية والتاريخية هو كفاية الضبط للمتغيرات والتحكم فيها عن قصد من جانب الباحث.
وتعتبر التجربة العلمية مصدراً رئيسياً للوصول إلى النتائج أو الحلول بالنسبة للمشكلات التي يدرسها البحث التجريبي، ولكن في نفس الوقت تستخدم المصادر الأخرى في الحصول على البيانات والمعلومات التي يحتاج إليها البحث بعد أن يُخضعها الباحث للفحص الدقيق والتحقق من صحتها وموضوعيتها .
المشكلة في البحث التربوي
يناقش هذا الموضوع النقاط التالية:
ـ مصادر الحصول على المشكلة.
ـ اختيار المشكلة وتقويمها.
ـ وضع خطة لبحث المشكلة.
أولاً : مصادر الحصول على المشكلة
من المُسلّم به أنه ما لم يتوفر للبحث مشكلة واضحة محددة مُلحة فإن كل عمل يقوم به الباحث سوف يكون مشكوكاً في قيمته، وكيف يمكن أن نتصور قيام بناء جيد على أساس غير سليم؟ ويمكن القول أن مرحلة اختيار الباحث لمشكلة تربوية تصلح للبحث والدراسة من أهم مراحل البحث التربوي.
لذلك نحاول التعرف فيما يلي على بعض المصادر التي تنمي لدى الباحث حساسية بالمشكلات التربوية، والتي عن طريقها يمكن أن يتوصل إلى مشكلة مناسبة للبحث :
1 ـ التخصص :
تخصص الباحث في مجال معين يوفر له خبرة بمشكلات هذا المجال سواء تلك التي تم بحثها ودراستها، أو المشكلات التي لم تُدرس بعد، وكلما اتصفت هذه الخبرة بالعمق والشمول كلما ساعدته في فهم أبعاد هذه المشكلات.
فالمعلمة المتخصصة في تدريس الرياضيات في المرحلة التأسيسية هي الأكثر دراية بالمشكلات المُلحّة التي تواجه تدريس الرياضيات في هذه المرحلة.
2 ـ برامج الدراسات العليا:
وتتمثل في البرامج التي توفرها الجامعات لطلاب البحوث، وقد تستغرق فترة دراسة هذه البرامج عام دراسي أو أكثر.
وتشتمل هذه البرامج على دراسات نظرية وأخرى تطبيقية (منها: مقررات مناهج البحث، والإحصاء وحلقات البحث، وعلوم الحاسب الآلي.. ) تزود الطالب بخلفية علمية لا تمكنه فقط من اختيار مشكلة البحث بل تفيده في جميع مراحل إعداد البحث.
ويتخلل هذه البرامج عرض خطط البحث التي يقترحها الباحثون ومناقشتها وتقويمها من جانب الأساتذة وزملائهم المشاركين في السيمنار (حلقة المناقشة)، وكل هذه النشاطات تساهم في زيادة حساسية الطالب لمشكلات المجال الذي يهم بالبحث فيه.
3 ـ الخبرة العملية:
الخبرة العملية كالعمل في ميدان التدريس مثلاً لفترة كافية تلعب دوراً هاماً في الإحساس ببعض المشكلات المُلحّة في واقع الميدان والحاجة إلى دراسات للتوصل إلى حلول علمية لها. فكل مدرس يواجه مشكلات يومية داخل حجرة الدراسة وخارجها ترتبط بما يُدرِّسه من مقررات وأساليب تدريسها وتقويمها، وكيفية الاستفادة من مستحدثات التكنولوجيا في رفع كفاية التدريس.
كما أن المشكلة التي يختارها الباحث بنفسه في ضوء خبرته العملية كثيراً ما يكون لها أهمية عند الباحث، الأمر الذي يجعله مثابراً خلال بحثه في محاولة الوصول إلى حلول واقعية لها.
4 ـ الدراسة المسحية للبحوث السابقة والجارية:
تساهم دراسة البحوث السابقة والجارية في الميدان في معرفة المشكلات التي بُحثت، والدراسة التحليلية لهذه البحوث أو ملخصاتها يمكن أن تكشف للطالب عن نواحي النقص في الدراسات السابقة والتي ما زالت تحتاج إلى إجراء بحوث حولها.
كما أن كثيراً من هذه البحوث تشتمل في نهاياتها على توصيات ومقترحات بإجراء بحوث معينة ترتبط بمشكلة البحث، وهذا لا يساعد الطالب فقط في اختيار مشكلة لبحثه، بل وتمنع من تكرار دراسة المشكلات التي سبق دراستها.
وفي بعض الحالات تنتهي البحوث بنتائج غير مؤكدة لعدم توافر البيانات، أو أن النتائج قامت على بيانات محدودة كأن تكون عينة البحث صغيرة جداً، ويمكن في هذه الحالات إجراء بحوث تُستخدم فيها عينات كبيرة وممثلة إلى حد كبير لمجتمعها الأصلي.
جدير بالذكر أن إجراء بحث بحيث يأتي صورة طبق الأصل لبحوث سابقة أمر غير مرغوب فيه، لكن في بعض الحالات قد تكون المشكلة ذات أهمية بحيث تحتاج إلى أكثر من بحث واحد للوصول إلى نتائج يُعتمد عليها.
ثانياً : اختيار المشكلة وتقويمها
هناك عدة اعتبارات لا بد أن يراعيها الباحث المبتدئ قبل اختياره لمشكلة بحثه، وترتبط هذه الاعتبارات بالجوانب التالية:
1 ـ حداثة المشكلة:
يجب أن تكون المشكلة جديدة ومبتكرة ولم يسبق دراستها من جانب باحثين آخرين، لكن هذا لا يعني أن جميع المشكلات التي سبق دراستها لم تعد جديرة بالبحث مرة أخرى.
ففي ضوء التطورات المعرفية والثقافية تأخذ المشكلات التربوية أبعاداً مختلفة، ويُعتبر تكرار بعض البحوث السابقة باستخدام تصميمات وأساليب وأدوات جديدة للبحث من الأعمال ذات القيمة العلمية.
2 ـ أهمية المشكلة وقيمتها العملية:
يساعد في تحديد أهمية المشكلة وقيمتها بحث عدد من التساؤلات هي:
ـ هل يُحتمل أن تضيف نتائج بحث المشكلة شيئاً جديداً إلى المعرفة العلمية الحاضرة ؟ أو لها تأثير مباشر في الممارسات التربوية الحالية في ميدان التربية والتعليم ؟
ـ هل يحتاج المجال إلى دراسات من هذا النوع ؟
ـ هل توجد نواحي نقص معينة في المعرفة الحالية ـ في مجال البحث ـ ويلزم إجراء بحوث لاستكمال هذا النقص ؟
ويحتاج الميدان التربوي إلى بحوث ذات قيمة عملية أو تطبيقية مباشرة. وهذا يتطلب أن يدرس الباحث المشكلات الموجودة فعلاً في الواقع التعليمي.
وعلى سبيل المثال هناك حاجة إلى بحوث في مجالات: نقص دافعية المتعلمين، واستخدام تكنولوجيا التعليم في التدريس، ومشكلات الرسوب والفاقد في التعليم.
3 ـ اهتمام الباحث بالمشكلة:
إن دراسة الباحث لمشكلة تحظى باهتمامه الشخصي تجعله أكثر مثابرة وصبراً واستمتاعاً بالبحث حتى إتمامه، وذلك لأن دافعيته وميله الذاتي للعمل يكون أكبر، وتزداد احتمالات تحقيق النجاح في البحث. ويتطلب هذا من طالب البحث أن يسأل نفسه أسئلة كالتالي:
ـ هل موضوع البحث يشبع الميول والدوافع الحقيقية في نفسي؟
ـ هل دافعي واهتمامي بإجراء البحث هو مجرد رغبتي في الحصول على درجة علمية أو امتيازات أدبية ومادية، وحتى لو كان موضوع البحث لا يتوفر له درجة اهتمام كافية من ناحيتي؟
وبالطبع ينبغي ألا يختار الطالب مشكلة معينة لكي يُدعِّم وجهة نظر يؤمن بها مسبقاً ومتحيز لها. كأن يكون مقتنعاً بأهمية "الاختلاط بين الجنسين في الجامعة" فيجري البحث لكي يؤكد صحة هذه الفكرة بغض النظر عما إذا جاءت النتائج مُدعمة لوجهة نظره أو مخالفة لها.
4 ـ كفاية خبرات الباحث وقدراته على بحث المشكلة:
ينبغي أن يتوفر لدى الطالب المهارات والقدرات اللازمة لدراسة المشكلة وإتمام البحث. ومن الأسئلة التي يمكن أن يوجهها الطالب لنفسه في هذا المجال ما يلي:
ـ هل يتوفر لي الخبرات اللازمة لدراسة المشكلة التي اخترتها؟
ـ ما هي المهارات والمعارف التي تنقصني لدراسة المشكلة؟
ففي كثير من الحالات قد يختار الباحث مشكلة معينة لبحثها وبعد أن يقطع في بحثه جزءاً كبيراً يكتشف أن خبرته وقدراته البحثية لا تمكنه من دراسة المشكلة على الوجه الأمثل، أو أنه غير قادر على إنجاز الجوانب الإحصائية الخاصة بنتائج البحث وتفسيرها.
5 ـ توفر البيانات ومصدرها:
ينبغي أن يضع الباحث عند اختياره لمشكلة البحث مدى إمكانية الحصول على البيانات اللازمة لدراسة المشكلة، فقد يكون الحصول على البيانات صعباً بسبب بعد مصادرها، أو لاعتبارات سياسية أو اجتماعية . ولذا ينبغي أن يسأل الباحث نفسه من البداية أسئلة منها:
ـ هل البيانات اللازمة للبحث يسهل الحصول عليها؟
ـ إذا كانت هناك صعوبات في الحصول على بيانات معينة، فهل يمكن تحديد مشكلة البحث وجعله في حدود البيانات المتاحة والممكن توفيرها؟
6 ـ الإشراف والوقت والتكلفة:
على الطالب أن يختار مشكلة بحثية يمكن أن يجد الأستاذ المتخصص في مجال هذه المشكلة . كما أن عليه ألا يختار مشكلة واسعة يحتاج إلى وقت طويل جداً لدراستها. وعليه أيضاً في اختياره لمشكلة بحثه التكاليف التي يحتاج إليها تنفيذ البحث وإلى أي مدى يمكن أن يوفرها في حدود إمكاناته المالية المتاحة؟
raneem noor
فصل المواد
يمكن فصل المواد المختلطة أو المتحدة مع بعضها البعض بطرق مختلفة، ويمكن تصنيف هذه الطرق بشكل عام تحت طريقتين رئيستين:
طرق فصل فيزيائية
وهي طرق يتم من خلالها فصل المواد عن بعضها البعض دون التأثير في تركيب المادة.
مثل: عملية التسخين، عملية الترشيح ،استخدام المغناطيس
طرق فصل كيميائية
وهي طرق يتم من خلالها فصل المواد عن بعضها البعض عن طريق التأثير في تركيب المادة.
مثل: عملية التسخين، عملية التحليل الكهربي.
بعض التغيرات نافع وبعضها ضار
التغيرات النافعة
تحولات المـــاء – ذوبان السكـر – ذوبان المــلح
احتراق الفحـــم – احتراق الغــــذاء
التغيرات الضارة
تسوس الأسنان – صدأ الحديد – حرائق الغابات
احتراق السكــر– عفن المواد الغذائية
تحولات المـــاء
الماء مركب كيميائي مكون من ذرتي هيدروجين وذرة من الاكسجين. ينتشر الماء على الأرض بأشكاله المختلفة، السائل و الصلب و الغازي .
يستطيع الماء التحول الى ثلاث حالات في الطبيعة هي الصلبة والسائلة والغازية:
الحالة الصلبة: يكون فيها الماء على شكل جليد أو ثلج أبيض اللون ناصع ، يوجد على هذه الحالة عندما تكون درجة حرارة الماء أقل من الصفر المئوي.
الحالة السائلة: يكون فيها الماء سائلا شفافا، وهي الحالة الأكثر شيوعا للماء. ويوجد الماء على صورته السائلة في درجات الحرارة ما بين الصفر المئوي، ودرجة الغليان، وهي 100 درجة مئوية.
وتوجد عدة طرق لتحويل الماء الى الحالة الغازية منها :
الغليان
يتبخر الماء عند غليه بدرجة 100 مئوية
التبخر
عملية تبخر الماء لاتحتاج لدرجات حرارة عالية بل يمكن أن يتبخر الماء عند 30درجة مئوية وتزداد سرعة التبخر بزيادة درجة الحرارة وهذا ما يفسر جفاف الملابس وتبخر مياه البحر الذي يكون السحب حيث ان مياه البحار لا تغلى لكنها تتبخر وتنتج بخار الماء بالاضافة الحالات الثلاثة توجد حالتان هما التكاثف والتسامي
التكاثف
هو تحول الماء من الحالة الغازية إلى الحالة السائلة نتيجة تبريد بخار الماء وأوضح مثال هو السحب والضباب بالاضافة الى قطرات الندى الذي تتكون على على السيارات صباحا وعلى نظارة الشخص عند خروجه من مكان حار إلى بارد والعكس
التسامي
هو تحول الماء من الحالة الصلبة الى الحالةالغازية
مثال ذلك هو تبخر الثلج الموجود على الشوارع في الدول ذات الطقس البارد والجاف جدا
الحالة الغازية : هي الحالة التي يتحول فيها الماء من سائل الى غاز ويكون فيها الماء على شكل بخار، ويكون الماء بالحالة الغازية بدرجات حرارة مختلفة.
لماذا لا تتجمد المحيطات في فصل الشتاء حتى القاع؟
لماذا يكون التجمد على السطح فحسب؟
في الجواب حكمة ربانية وهي ان الماء عندما تنخفض حرارته وتبلغ 4 درجات مئوية فإن سطحه يتجمد ويزداد حجمه ،على العكس من كل السوائل والجوامد الاخرى، وبالتالي ينخفض وزنه ويطفو على السطح ويصبح بينه وبين الماء عازل هو الهواء وهذا ما يحافظ على حياة الكائنات البحرية ويحميها من التجمد
شوق المرشدي
يمكن فصل المواد المختلطة أو المتحدة مع بعضها البعض بطرق مختلفة، ويمكن تصنيف هذه الطرق بشكل عام تحت طريقتين رئيستين:
طرق فصل فيزيائية
وهي طرق يتم من خلالها فصل المواد عن بعضها البعض دون التأثير في تركيب المادة.
مثل: عملية التسخين، عملية الترشيح ،استخدام المغناطيس
طرق فصل كيميائية
وهي طرق يتم من خلالها فصل المواد عن بعضها البعض عن طريق التأثير في تركيب المادة.
مثل: عملية التسخين، عملية التحليل الكهربي.
بعض التغيرات نافع وبعضها ضار
التغيرات النافعة
تحولات المـــاء – ذوبان السكـر – ذوبان المــلح
احتراق الفحـــم – احتراق الغــــذاء
التغيرات الضارة
تسوس الأسنان – صدأ الحديد – حرائق الغابات
احتراق السكــر– عفن المواد الغذائية
تحولات المـــاء
الماء مركب كيميائي مكون من ذرتي هيدروجين وذرة من الاكسجين. ينتشر الماء على الأرض بأشكاله المختلفة، السائل و الصلب و الغازي .
يستطيع الماء التحول الى ثلاث حالات في الطبيعة هي الصلبة والسائلة والغازية:
الحالة الصلبة: يكون فيها الماء على شكل جليد أو ثلج أبيض اللون ناصع ، يوجد على هذه الحالة عندما تكون درجة حرارة الماء أقل من الصفر المئوي.
الحالة السائلة: يكون فيها الماء سائلا شفافا، وهي الحالة الأكثر شيوعا للماء. ويوجد الماء على صورته السائلة في درجات الحرارة ما بين الصفر المئوي، ودرجة الغليان، وهي 100 درجة مئوية.
وتوجد عدة طرق لتحويل الماء الى الحالة الغازية منها :
الغليان
يتبخر الماء عند غليه بدرجة 100 مئوية
التبخر
عملية تبخر الماء لاتحتاج لدرجات حرارة عالية بل يمكن أن يتبخر الماء عند 30درجة مئوية وتزداد سرعة التبخر بزيادة درجة الحرارة وهذا ما يفسر جفاف الملابس وتبخر مياه البحر الذي يكون السحب حيث ان مياه البحار لا تغلى لكنها تتبخر وتنتج بخار الماء بالاضافة الحالات الثلاثة توجد حالتان هما التكاثف والتسامي
التكاثف
هو تحول الماء من الحالة الغازية إلى الحالة السائلة نتيجة تبريد بخار الماء وأوضح مثال هو السحب والضباب بالاضافة الى قطرات الندى الذي تتكون على على السيارات صباحا وعلى نظارة الشخص عند خروجه من مكان حار إلى بارد والعكس
التسامي
هو تحول الماء من الحالة الصلبة الى الحالةالغازية
مثال ذلك هو تبخر الثلج الموجود على الشوارع في الدول ذات الطقس البارد والجاف جدا
الحالة الغازية : هي الحالة التي يتحول فيها الماء من سائل الى غاز ويكون فيها الماء على شكل بخار، ويكون الماء بالحالة الغازية بدرجات حرارة مختلفة.
لماذا لا تتجمد المحيطات في فصل الشتاء حتى القاع؟
لماذا يكون التجمد على السطح فحسب؟
في الجواب حكمة ربانية وهي ان الماء عندما تنخفض حرارته وتبلغ 4 درجات مئوية فإن سطحه يتجمد ويزداد حجمه ،على العكس من كل السوائل والجوامد الاخرى، وبالتالي ينخفض وزنه ويطفو على السطح ويصبح بينه وبين الماء عازل هو الهواء وهذا ما يحافظ على حياة الكائنات البحرية ويحميها من التجمد
شوق المرشدي
ن توجد البلازما؟
غالبا معظم المواد الموجودة فى هذا الكون الفسيح توجد على شكل بلازما. هذه البلازما تكون عند درجات حرارة عالية وكثافة عالية ايضا، وتتغير هذه الظروف من مكان إلى آخر، فعلى سبيل المثال تبلغ درجة حرارة مركز الشمس عشرة ملايين درجة مئوية بينما على سطحها فإن درجة الحرارة تصل إلى ستة الاف درجة مئوية، ومن هنا فإن البلازما داخل الشمس تختلف تماما عن خارجها. ولكن على الكرة الأرضية حيث توجد المادة غالبا فى الحالة الصلبة، وطبقات الغلاف الجوى عبارة عن غاز غير متأين، أى أنه لا يوجد حالة بلازما طبيعية على سطح الأرض. ولكن هل يمكن عمل بلازما فى المختبر؟ إذا كنت تقرأ هذا المقال تحت ضوء مصباح فلورسنت (النيون) فإن مصدر هذا الضوء هو عبارة عن بلازما مصنعة، فعند مرور التيار الكهربى داخل غاز (غاز الزئبق) تحت ضغط منخفض فإنه يعمل على تأين الغاز مخلفا خليطا من الأيونات الموجبة والالكترونات، ما تلبث ان تتحد مع بعضها البعض وتكون النتيجة انبعاث الضوء الساطع، وتستمر هاتان العمليتان (التأين والاتحاد) طالما استمر التيار الكهربى فى السريان. هذا مثال على مصدر بلازما ذات درجة حرارة منخفضة موجود فى بيتك.
لكن قديما وحتى يومنا هذا اهتم علماء الفيزياء الفلكية بكشف اسرار الكون وفهم ماذا يحدث على سطح الشمس والنجوم الاخرى. لذلك حاول العلماء تصنيع نفس البلازما الموجودة فى النجوم داخل المختبر، ولصنع هذه البلازما طور العلماء اجهزة مختلفة قادرة على توليد طاقة هائلة لانتاج بلازما بنفس ظروف البلازما الموجودة فى الطبيعة، كان احد هذه الاجهزة هو جهاز التحديد المغناطيسى Magnitec-confinment devices. وتمت معرفة معلومات كثيرة عن تركيب وفهم السطح الخارجى للغلاف الشمسى. ولكن ماذا عن البلازما الموجودة داخل الشمس ذات درجات الحرارة العالية جدا. كيف يمكن تصنيعها فى المختبر؟
فى الحقيقة وحتى عهد قريب وبتطور اجهرة الليزر اصبح بالامكان الحصول على بلازما مشابهة لتلك الموجودة على اى نجم سواء داخله أو خارجه.
الحصول على بلازما بواسطة اشعة الليزر؟
نعلم أن الضوء هو عبارة عن تذبذب مجالين متعامدين احدهما كهربى والاخر مغناطيسى. والليزر ما هو الا عبارة عن ضوء له خصائص مميزة تجعل شدة اشعاعه (الطاقة لكل وحدة مساحات لكل وحدة زمن) تزداد بزيادة المجال الكهربى والمغناطيسى لموجاته.
ولكن هل يمكن أن يكون الضوء الناتج من اشعة الليزر أقوى من الأجسام الصلبة؟ إن شدة المجال الكهربى لشعاع الليزر تبلغ 5x1011v/m عندما تكون شدة اشعاعه 3x1020W/m2، وفى أيامنا هذه تصل شدة اشعاع بعض انواع الليزر إلى مايقارب 1022W/m2. وبالمقارنة بشدة اشعاع مصباح كهربى عادى (60Watt) على بعد متر او مترين فهى لا تزيد عن 0.1W/m2. حيث أن المجال الكهربى لهذه الاشعة يفوق بكثير المجال الكهربى الذى يربط ذرات المواد الصلبة بعضها ببعض وبذلك فإن المجال الكهربى لشعاع الليزر سوف يؤثر على الكترونات المواد الصلبة ويفصلها عن الذرات تاركا أيونات موجبةـ وبهذا يحول الليزر جزء من المادة الصلبة إلى حالة بلازما. يتضح مما سبق أنه يمكن استخدام اشعة الليزر المركزة لانتاج بلازما عند درجات حرارة عالية جدا داخل المختبر وبتكلفة قليلة. يوضح شكل (1) كيفية تصنيع بلازما فى المختبر باستخدام الليزر.
ولهذا النظام العديد من التطبيقات الهامة فى مجال الفيزياء الفلكية حيث يتم اختيار نوع مادة الهدف وتصميمه بشكل هندسى معين حتى تكون البلازما الناتجة فى المختبر مشابهة لظروف البلازما الحقيقية للنجم المراد دراسته. بالاضافة إلى إلى ذلك فإن البلازما تستخدم فى العديد من الصناعات.
التطبيقات الصناعية للبلازما
صناعة الدوائر الالكترونية المتكاملة
تستخدم البلازما ذات درجات الحرارة المنخفضة فى العديد من المجالات الهامة على سبيل المثال، معظم الدوائر المتكاملة المعقدة جدا والتى تدخل فى تركيب كل جهاز الكترونى، هذه الدوائر الالكترونية تحتوى على عشرات الالاف من الترانزستورات والمكثفات موصلة ببعضها البعض بواسطة اسلاك قطرها فى حدود 0.1 ميكرومتر، هذا النوع من التكنولوجيا الدقيقة والمعقدة تصنع باستخدام البلارما، حيث تقوم البلازما بنحت الدوائر الالكترونية على شريحة السيليكون بناءا على القناع المعدنى الموضوع امام الشريحة.
فى هذه العملية يكون النحت على شريحة السليكون كالاتى:-
حيث أن الالكترونات داخل البلازما حرة الحركة وطاقتها اعلى من الايونات الموجبة فإنها تصل إلى اطراف البلازما بسرعة وتقوم بدورها بجذب الايونات الموجبة اتجاهها وتعجلها باتجاه الشريحة وعند اصطدام الايونات الموجبة بالمناطق المكشوفة على الشريحة تقوم بنحتها، وبعدها يستبدل القناع المعدنى باخر مطبوع عليه الدوائر الكهربية الخاصة بالطبقة الثانية وهكذا بالنسبة للطبقة الثالثة والرابعة ...... والخ حتى تتم عملية النحت.
هنالك طريقة اخرى متبعة وهى تعتمد على استخدام مركب Carbon tetrafluoride CF4 كمصدر لانتاج البلازما، وعندها يتحول هذا المركب إلى اجزاء اخرى منها ذرات الفلورين. هذه الذرات تتفاعل مع ذرات السيليكون المكونة للشريحة وتكون مركب جديد هو Silicon tetrafluoride والذى يمكن ازالته اثناء عملية الضخ. يتضح مما سبق أن هذه الطريقة هى عملية كيميائية تقوم فيها ذرات الفلورين بالتهام السليكون المراد ازالته. وهذه العملية اسرع من عملية النحت المذكورة سابقا.
وتجدر الاشارة إلى أن البحث والتطوير جارى منذ عام 1980 وحتى الأن للحصول على بلازما منتظمة لتغطى اكبر مساحة ممكنة حيث كانت شريحة السيليكون المستخدمة قديما تبلغ 2سم2 اما الأن فهى تصل إلى 20سم2، وهذه البلازما لها استخدامات عديدة فهى تستخدم فى شاشات اجهزة الكمبيوتر المتنقلة Notebook computer كمصدر ضوئى، والتى ادت إلى تطور كبير فى مجال تكنولوجيا شاشات العرض. ويسعى العلماء حاليا للحصول على شاشة مساحتها 1متر مربع وسمكها لايزيد عن 4-5 سم لاستخدامها كشاشة تلفزيون يمكن تعليقها فى المنازل والمحلات دون ان تشغل حيز من الغرفة، وهذا سوف يتحقق بالوصول إلى بلازما متجانسة على مساحة 1متر مربع.
raneem noor
حافظة على نظافة البيئة
تستخدم البلازما حاليا فى العديد من الدول المتقدمة فى التخلص من المواد السامة الملوثة للبيئة معتمدين على العمليات الكيميائية الفريدة التى تتم داخل البلازما. حيث يمكن ان تقوم البلازما بتحويل المواد السامة المنبعثة من مداخن المصانع ومن عوادم السيارات مثل غاز اكسيد الكبريت (SO) واكسيد النيتريك (NO) إلى مواد غير سامة. فعلى سبيل المثال غاز NO قبل ان يخرج من المدخنة إلى الغلاف الجوى، توجه عليه حزمة من الالكترونات ذات طاقة عالية من جهاز مثبت فى منتصف المدخنة تعمل على تأيين الغازات الموجودة (المادة السامة NO والهواء) أى تحولها إلى حالة بلازما. وقبل خروجها إلى الجو تكون مرحلة التأيين قد انتهت وتتكون جزيئات النيتروجين والاكسجين نتيجة لعملية اعادة الاتحاد. وبهذا نكون قد حولنا الغازات الملوثة إلى غازات نافعة وبتكاليف قليلة.
يجدر الاشارة هنا أنه تم حديثا التوجه إلى معالجة الغازات المنطلقة من عوادم السيارات، حيث تم تركيب جهاز بلازما فى عادم السيارة ليعالج الغازات السامة قبل خروجها إلى الجو.
كذلك اجريت تجارب عديدة على الفضلات الصلبة والسائلة حيث تستخدم بلازما عند درجات حرارة عالية تصل إلى 6000 درجة مئوية تعمل على تبخير وتحطيم المواد السامة وتحولها إلى غازات غير سامة، وفى نهاية العملية يكون ماتبقى من مواد صلبة فى صورة زجاج. وتم فى امريكا العام الماضى التخلص من حوالى 4000 مستودع يحتوى على فضلات صلبة وملوثة للبيئة بواسطة البلازما. وقد كانت هذه الفضلات تدفن فى باطن الارض مما كانت تسبب اخطار تلوث. وباستخدام البلازما يمكن حاليا التخلص من 200 كيلو جرام من المواد السامة فى الساعة.
غالبا معظم المواد الموجودة فى هذا الكون الفسيح توجد على شكل بلازما. هذه البلازما تكون عند درجات حرارة عالية وكثافة عالية ايضا، وتتغير هذه الظروف من مكان إلى آخر، فعلى سبيل المثال تبلغ درجة حرارة مركز الشمس عشرة ملايين درجة مئوية بينما على سطحها فإن درجة الحرارة تصل إلى ستة الاف درجة مئوية، ومن هنا فإن البلازما داخل الشمس تختلف تماما عن خارجها. ولكن على الكرة الأرضية حيث توجد المادة غالبا فى الحالة الصلبة، وطبقات الغلاف الجوى عبارة عن غاز غير متأين، أى أنه لا يوجد حالة بلازما طبيعية على سطح الأرض. ولكن هل يمكن عمل بلازما فى المختبر؟ إذا كنت تقرأ هذا المقال تحت ضوء مصباح فلورسنت (النيون) فإن مصدر هذا الضوء هو عبارة عن بلازما مصنعة، فعند مرور التيار الكهربى داخل غاز (غاز الزئبق) تحت ضغط منخفض فإنه يعمل على تأين الغاز مخلفا خليطا من الأيونات الموجبة والالكترونات، ما تلبث ان تتحد مع بعضها البعض وتكون النتيجة انبعاث الضوء الساطع، وتستمر هاتان العمليتان (التأين والاتحاد) طالما استمر التيار الكهربى فى السريان. هذا مثال على مصدر بلازما ذات درجة حرارة منخفضة موجود فى بيتك.
لكن قديما وحتى يومنا هذا اهتم علماء الفيزياء الفلكية بكشف اسرار الكون وفهم ماذا يحدث على سطح الشمس والنجوم الاخرى. لذلك حاول العلماء تصنيع نفس البلازما الموجودة فى النجوم داخل المختبر، ولصنع هذه البلازما طور العلماء اجهزة مختلفة قادرة على توليد طاقة هائلة لانتاج بلازما بنفس ظروف البلازما الموجودة فى الطبيعة، كان احد هذه الاجهزة هو جهاز التحديد المغناطيسى Magnitec-confinment devices. وتمت معرفة معلومات كثيرة عن تركيب وفهم السطح الخارجى للغلاف الشمسى. ولكن ماذا عن البلازما الموجودة داخل الشمس ذات درجات الحرارة العالية جدا. كيف يمكن تصنيعها فى المختبر؟
فى الحقيقة وحتى عهد قريب وبتطور اجهرة الليزر اصبح بالامكان الحصول على بلازما مشابهة لتلك الموجودة على اى نجم سواء داخله أو خارجه.
الحصول على بلازما بواسطة اشعة الليزر؟
نعلم أن الضوء هو عبارة عن تذبذب مجالين متعامدين احدهما كهربى والاخر مغناطيسى. والليزر ما هو الا عبارة عن ضوء له خصائص مميزة تجعل شدة اشعاعه (الطاقة لكل وحدة مساحات لكل وحدة زمن) تزداد بزيادة المجال الكهربى والمغناطيسى لموجاته.
ولكن هل يمكن أن يكون الضوء الناتج من اشعة الليزر أقوى من الأجسام الصلبة؟ إن شدة المجال الكهربى لشعاع الليزر تبلغ 5x1011v/m عندما تكون شدة اشعاعه 3x1020W/m2، وفى أيامنا هذه تصل شدة اشعاع بعض انواع الليزر إلى مايقارب 1022W/m2. وبالمقارنة بشدة اشعاع مصباح كهربى عادى (60Watt) على بعد متر او مترين فهى لا تزيد عن 0.1W/m2. حيث أن المجال الكهربى لهذه الاشعة يفوق بكثير المجال الكهربى الذى يربط ذرات المواد الصلبة بعضها ببعض وبذلك فإن المجال الكهربى لشعاع الليزر سوف يؤثر على الكترونات المواد الصلبة ويفصلها عن الذرات تاركا أيونات موجبةـ وبهذا يحول الليزر جزء من المادة الصلبة إلى حالة بلازما. يتضح مما سبق أنه يمكن استخدام اشعة الليزر المركزة لانتاج بلازما عند درجات حرارة عالية جدا داخل المختبر وبتكلفة قليلة. يوضح شكل (1) كيفية تصنيع بلازما فى المختبر باستخدام الليزر.
ولهذا النظام العديد من التطبيقات الهامة فى مجال الفيزياء الفلكية حيث يتم اختيار نوع مادة الهدف وتصميمه بشكل هندسى معين حتى تكون البلازما الناتجة فى المختبر مشابهة لظروف البلازما الحقيقية للنجم المراد دراسته. بالاضافة إلى إلى ذلك فإن البلازما تستخدم فى العديد من الصناعات.
التطبيقات الصناعية للبلازما
صناعة الدوائر الالكترونية المتكاملة
تستخدم البلازما ذات درجات الحرارة المنخفضة فى العديد من المجالات الهامة على سبيل المثال، معظم الدوائر المتكاملة المعقدة جدا والتى تدخل فى تركيب كل جهاز الكترونى، هذه الدوائر الالكترونية تحتوى على عشرات الالاف من الترانزستورات والمكثفات موصلة ببعضها البعض بواسطة اسلاك قطرها فى حدود 0.1 ميكرومتر، هذا النوع من التكنولوجيا الدقيقة والمعقدة تصنع باستخدام البلارما، حيث تقوم البلازما بنحت الدوائر الالكترونية على شريحة السيليكون بناءا على القناع المعدنى الموضوع امام الشريحة.
فى هذه العملية يكون النحت على شريحة السليكون كالاتى:-
حيث أن الالكترونات داخل البلازما حرة الحركة وطاقتها اعلى من الايونات الموجبة فإنها تصل إلى اطراف البلازما بسرعة وتقوم بدورها بجذب الايونات الموجبة اتجاهها وتعجلها باتجاه الشريحة وعند اصطدام الايونات الموجبة بالمناطق المكشوفة على الشريحة تقوم بنحتها، وبعدها يستبدل القناع المعدنى باخر مطبوع عليه الدوائر الكهربية الخاصة بالطبقة الثانية وهكذا بالنسبة للطبقة الثالثة والرابعة ...... والخ حتى تتم عملية النحت.
هنالك طريقة اخرى متبعة وهى تعتمد على استخدام مركب Carbon tetrafluoride CF4 كمصدر لانتاج البلازما، وعندها يتحول هذا المركب إلى اجزاء اخرى منها ذرات الفلورين. هذه الذرات تتفاعل مع ذرات السيليكون المكونة للشريحة وتكون مركب جديد هو Silicon tetrafluoride والذى يمكن ازالته اثناء عملية الضخ. يتضح مما سبق أن هذه الطريقة هى عملية كيميائية تقوم فيها ذرات الفلورين بالتهام السليكون المراد ازالته. وهذه العملية اسرع من عملية النحت المذكورة سابقا.
وتجدر الاشارة إلى أن البحث والتطوير جارى منذ عام 1980 وحتى الأن للحصول على بلازما منتظمة لتغطى اكبر مساحة ممكنة حيث كانت شريحة السيليكون المستخدمة قديما تبلغ 2سم2 اما الأن فهى تصل إلى 20سم2، وهذه البلازما لها استخدامات عديدة فهى تستخدم فى شاشات اجهزة الكمبيوتر المتنقلة Notebook computer كمصدر ضوئى، والتى ادت إلى تطور كبير فى مجال تكنولوجيا شاشات العرض. ويسعى العلماء حاليا للحصول على شاشة مساحتها 1متر مربع وسمكها لايزيد عن 4-5 سم لاستخدامها كشاشة تلفزيون يمكن تعليقها فى المنازل والمحلات دون ان تشغل حيز من الغرفة، وهذا سوف يتحقق بالوصول إلى بلازما متجانسة على مساحة 1متر مربع.
raneem noor
حافظة على نظافة البيئة
تستخدم البلازما حاليا فى العديد من الدول المتقدمة فى التخلص من المواد السامة الملوثة للبيئة معتمدين على العمليات الكيميائية الفريدة التى تتم داخل البلازما. حيث يمكن ان تقوم البلازما بتحويل المواد السامة المنبعثة من مداخن المصانع ومن عوادم السيارات مثل غاز اكسيد الكبريت (SO) واكسيد النيتريك (NO) إلى مواد غير سامة. فعلى سبيل المثال غاز NO قبل ان يخرج من المدخنة إلى الغلاف الجوى، توجه عليه حزمة من الالكترونات ذات طاقة عالية من جهاز مثبت فى منتصف المدخنة تعمل على تأيين الغازات الموجودة (المادة السامة NO والهواء) أى تحولها إلى حالة بلازما. وقبل خروجها إلى الجو تكون مرحلة التأيين قد انتهت وتتكون جزيئات النيتروجين والاكسجين نتيجة لعملية اعادة الاتحاد. وبهذا نكون قد حولنا الغازات الملوثة إلى غازات نافعة وبتكاليف قليلة.
يجدر الاشارة هنا أنه تم حديثا التوجه إلى معالجة الغازات المنطلقة من عوادم السيارات، حيث تم تركيب جهاز بلازما فى عادم السيارة ليعالج الغازات السامة قبل خروجها إلى الجو.
كذلك اجريت تجارب عديدة على الفضلات الصلبة والسائلة حيث تستخدم بلازما عند درجات حرارة عالية تصل إلى 6000 درجة مئوية تعمل على تبخير وتحطيم المواد السامة وتحولها إلى غازات غير سامة، وفى نهاية العملية يكون ماتبقى من مواد صلبة فى صورة زجاج. وتم فى امريكا العام الماضى التخلص من حوالى 4000 مستودع يحتوى على فضلات صلبة وملوثة للبيئة بواسطة البلازما. وقد كانت هذه الفضلات تدفن فى باطن الارض مما كانت تسبب اخطار تلوث. وباستخدام البلازما يمكن حاليا التخلص من 200 كيلو جرام من المواد السامة فى الساعة.
تغيرات المادة
المادة هي : كل شيء يشغل حيزاً من الفراغ وله ثقل .
المادة عرضة للتغير نتيجة تعرضها لظروف معينة كالحرارة والضغط أو تفاعلها مع مواد أخرى وهناك نوعين من التغيرات التي يمكن أن تطرأ على المادة في حالاتها وأشكالها المختلفة :
التغير الكيميائي : هو أي تغير يحدث على مادة أو مجموعة مواد مؤدياً إلى تغييرها وإنتاج مادة أو مواد من نوع جديد (تغيرات تطرأ على المادة فتنتج مواد جديدة مختلفة في خواصها عن المادة الأصلية.
مثل: احتراق الفحم، فساد الحليب، تحلل الماء كهربياً ).
التغير الفيزيائي : هي تغيرات تحدث في حالة المادة من حيث الشكل والمظهر الخارجي مرتبط بتغير درجة الحرارة أي هو تغير في نوع المادة فقط دون حدوث أي تغير في خواصها الأخرى ( تغيرات تطرأ على المادة وتظل المادة محتفظة بهويتها مثل: كسر الزجاج، تبخر الماء، ذوبان السكر في الماء).
أشكال المادة
العنصر
مادة أولية لا يمكن تحليلها إلى مواد أبسط منها لا بالطرق الفيزيائية ولا بالطرق الكيميائية .
مثل الأكسجين ، الكربون ، الحديد
المركب
مادة ناتجة من اتحاد عنصرين أو أكثر اتحاداً كيميائياً .
مثل الماء ، الملح ، السكر .
المخلوط
مادتين أو أكثر مجتمعة مع بعضها دون اتحاد كيميائي .
مثل الهواء ، الأكسجين في الماء ، ملح وسكر .
شوق المرشدي
المادة هي : كل شيء يشغل حيزاً من الفراغ وله ثقل .
المادة عرضة للتغير نتيجة تعرضها لظروف معينة كالحرارة والضغط أو تفاعلها مع مواد أخرى وهناك نوعين من التغيرات التي يمكن أن تطرأ على المادة في حالاتها وأشكالها المختلفة :
التغير الكيميائي : هو أي تغير يحدث على مادة أو مجموعة مواد مؤدياً إلى تغييرها وإنتاج مادة أو مواد من نوع جديد (تغيرات تطرأ على المادة فتنتج مواد جديدة مختلفة في خواصها عن المادة الأصلية.
مثل: احتراق الفحم، فساد الحليب، تحلل الماء كهربياً ).
التغير الفيزيائي : هي تغيرات تحدث في حالة المادة من حيث الشكل والمظهر الخارجي مرتبط بتغير درجة الحرارة أي هو تغير في نوع المادة فقط دون حدوث أي تغير في خواصها الأخرى ( تغيرات تطرأ على المادة وتظل المادة محتفظة بهويتها مثل: كسر الزجاج، تبخر الماء، ذوبان السكر في الماء).
أشكال المادة
العنصر
مادة أولية لا يمكن تحليلها إلى مواد أبسط منها لا بالطرق الفيزيائية ولا بالطرق الكيميائية .
مثل الأكسجين ، الكربون ، الحديد
المركب
مادة ناتجة من اتحاد عنصرين أو أكثر اتحاداً كيميائياً .
مثل الماء ، الملح ، السكر .
المخلوط
مادتين أو أكثر مجتمعة مع بعضها دون اتحاد كيميائي .
مثل الهواء ، الأكسجين في الماء ، ملح وسكر .
شوق المرشدي
طبقة الأوزون وأهميتها
إن طبقة الأوزون هي الطبقة التي تحتوي علي غاز الأوزون في طبقات الجو العليا من الغلاف الجوي والتي تقع في الغلاف الاستراتوسفيري للغلاف الجوي، وطبقة الأوزون تحيط بالغلاف الجوي إحاطة كامـلة علي ارتفاع يتراوح مابين 20 و 30 كيلـو متر من سطـح الأرض ويتراوح سمكها من 2-8 كيلو متر.
وتقوم طبقة الأوزون بدور المرشح الطبيعى والدرع الواقى الذى يحيط بالأرض ليحميها من الجزء الضار من الأشعة فوق البنفسجية (Ultra Violet - B) ذات الأضرار الجسيمة بصحة الإنسان والحيوان على حد سواء، كما تقلل من نمو النبات وإنتاج المحاصيل الزراعية، وتؤثر على نظم البيئة المائية.
إن النشاط البشري وما استحدثه الإنسان من تكنولوجيا في تخليق المواد الكيميائية قد أدي بعض منها إلي تدمير طبقة الأوزون ومن أهم المواد الكيميائية التي تستنفد طبقة الأوزون:
أ- الكلوروفلوروكربونات والهيدروكلوروفلوروكربونات المستخدمة بكثرة في أجهزة التبريد والتكييف المنزلية والتجارية والصناعية.
ب- الهالونات المستخدمة في أنظمة مكافحة الحرائق.
ج- مادة بروميد الميثيل المستخدمة كمبيد حشري في تخزين المحاصيل الزراعية وتعقيم التربة الزراعية.
د- بعض المذيبات المستخدمة فى تنظيف الأجزاء الميكانيكية و المعدنية والدوائر الالكترونية مثل مادة رابع كلوريد الكربون.
وتحتوى هذه الغازات عادة على ذرات من الكلور أو البروم تنفصل نتيجة لتأثرها بالأشعة فوق البنفسجية فتتجه إلى أقرب وحدة من غاز الأوزون الذى يتكون من ثلاث ذرات أوكسجين وتضم إليها إحداها تاركة ذرتين (وحدة لا تقاوم الأشعة فوق البنفسجية) وتمضى ذرة الكلور ومعها ذرة الأوكسجين إلى أن تلتقى بذرة أوكسجين أخرى منفردة، فتلتحم ذرتا الأوكسجين مع بعضهما مكونة وحدة أوكسجين (وحدة لا تقاوم الأشعة فوق البنفسجية) وتنفصل ذرة الكلور وتمضى إلى وحدة أوزون أخرى لتفعل معها نفس الشىء – وهكذا تتكرر عملية الهدم هذه ملايين المرات وذلك فى الطبقات العليا (الاستراتوسفيرية).
الكيماويات التي تدمر طبقة الأوزون وتصنيفها
إن مصدر التهديد يأتى نتيجة أعمال وتكنولوجيا ابتدعها الإنسان بالإضافة إلى مجموعة من الممارسات البسيطة فى الحيــاة اليومية العادية لإنسان القرن العشرين ومنها انبعاث غازات:
أ- (CFCs) الكلوروفلوروكلربون و(HCFCs) الهيدروكلوروفلوروكربون والمستخدمة فى أجهزة التبريد والتكييف المنزلية والتجارية والصناعية وأجهزة التكييف المركزية، وفى أجهزة تكييف السيارات.
ب- CFCs المستخدمة فى الايروسولات والتى تنطلق فى الفضاء عند استخدام بخاخات العطور والمبيدات الحشرية والأدوية.
ج- بعض المذيبات المستخدمة فى تنظيف الأجزاء الميكانيكية والمعدنية والدوائر الإلكترونية.
د- الهالونات المستخدمة فى أنظمة مكافحة الحرائق.
هـ- بروميد الميثيل المستخدم كمبيد حشرى فى التخزين وتعقيم التربة الزراعية.
كيف يتم تآكل طبقة الأوزون
الأضرار البيئية والصحية الناجمة عن تآكل طبقة الأوزون
ويعد تآكل طبقة الأوزون من أكبر الأمثلة على الخطر الماثل أمام سكان الأرض جميعا على اختلاف ظروفهم البيئية، ودون تحيز على نحو تحركت معه الجماعة الدولية بعيدا عن مجال النصح والإرشاد إلى وضع المسألة فى شكل قانونى بحت مقترن بالجزاء، وصار الالتزام الدولى بذلك من قبيل الالتزام بتحقيق نتيجة وليس الالتزام ببذل عناية أو ما يسمى بالالتزام بغاية نوهى فى بساطة التخلص إن عاجلا أو آجلا من المواد المستنفذة لطبقة الأوزون.
إن الأضرار البيئية الناتجة عن تآكل طبقة الأوزون تتمثل بصورة كبيرة في التغيرات المناخية الحادثة لكوكب الأرض ومنها التغيرات الفجائية في الطقس والمناخ والتصحر وحرائق الغابات والارتفاع في مستوي سطح البحر لشواطئ عديدة في العالم وإحداث خلل في التوازن البيئي والأضرار الصحية تتمثل في حدوث بعض سرطانات الجلد وضعف المناعة الطبيعية للإنسان وبعض أمراض العيون مثل عتامة العين إذا ما تعرض الكائنات الحية مثل الإنسان والحيوان لكميات كبيرة من الجزء الضار من الأشعة فوق البنفسجية.
raneem noor
إن طبقة الأوزون هي الطبقة التي تحتوي علي غاز الأوزون في طبقات الجو العليا من الغلاف الجوي والتي تقع في الغلاف الاستراتوسفيري للغلاف الجوي، وطبقة الأوزون تحيط بالغلاف الجوي إحاطة كامـلة علي ارتفاع يتراوح مابين 20 و 30 كيلـو متر من سطـح الأرض ويتراوح سمكها من 2-8 كيلو متر.
وتقوم طبقة الأوزون بدور المرشح الطبيعى والدرع الواقى الذى يحيط بالأرض ليحميها من الجزء الضار من الأشعة فوق البنفسجية (Ultra Violet - B) ذات الأضرار الجسيمة بصحة الإنسان والحيوان على حد سواء، كما تقلل من نمو النبات وإنتاج المحاصيل الزراعية، وتؤثر على نظم البيئة المائية.
إن النشاط البشري وما استحدثه الإنسان من تكنولوجيا في تخليق المواد الكيميائية قد أدي بعض منها إلي تدمير طبقة الأوزون ومن أهم المواد الكيميائية التي تستنفد طبقة الأوزون:
أ- الكلوروفلوروكربونات والهيدروكلوروفلوروكربونات المستخدمة بكثرة في أجهزة التبريد والتكييف المنزلية والتجارية والصناعية.
ب- الهالونات المستخدمة في أنظمة مكافحة الحرائق.
ج- مادة بروميد الميثيل المستخدمة كمبيد حشري في تخزين المحاصيل الزراعية وتعقيم التربة الزراعية.
د- بعض المذيبات المستخدمة فى تنظيف الأجزاء الميكانيكية و المعدنية والدوائر الالكترونية مثل مادة رابع كلوريد الكربون.
وتحتوى هذه الغازات عادة على ذرات من الكلور أو البروم تنفصل نتيجة لتأثرها بالأشعة فوق البنفسجية فتتجه إلى أقرب وحدة من غاز الأوزون الذى يتكون من ثلاث ذرات أوكسجين وتضم إليها إحداها تاركة ذرتين (وحدة لا تقاوم الأشعة فوق البنفسجية) وتمضى ذرة الكلور ومعها ذرة الأوكسجين إلى أن تلتقى بذرة أوكسجين أخرى منفردة، فتلتحم ذرتا الأوكسجين مع بعضهما مكونة وحدة أوكسجين (وحدة لا تقاوم الأشعة فوق البنفسجية) وتنفصل ذرة الكلور وتمضى إلى وحدة أوزون أخرى لتفعل معها نفس الشىء – وهكذا تتكرر عملية الهدم هذه ملايين المرات وذلك فى الطبقات العليا (الاستراتوسفيرية).
الكيماويات التي تدمر طبقة الأوزون وتصنيفها
إن مصدر التهديد يأتى نتيجة أعمال وتكنولوجيا ابتدعها الإنسان بالإضافة إلى مجموعة من الممارسات البسيطة فى الحيــاة اليومية العادية لإنسان القرن العشرين ومنها انبعاث غازات:
أ- (CFCs) الكلوروفلوروكلربون و(HCFCs) الهيدروكلوروفلوروكربون والمستخدمة فى أجهزة التبريد والتكييف المنزلية والتجارية والصناعية وأجهزة التكييف المركزية، وفى أجهزة تكييف السيارات.
ب- CFCs المستخدمة فى الايروسولات والتى تنطلق فى الفضاء عند استخدام بخاخات العطور والمبيدات الحشرية والأدوية.
ج- بعض المذيبات المستخدمة فى تنظيف الأجزاء الميكانيكية والمعدنية والدوائر الإلكترونية.
د- الهالونات المستخدمة فى أنظمة مكافحة الحرائق.
هـ- بروميد الميثيل المستخدم كمبيد حشرى فى التخزين وتعقيم التربة الزراعية.
كيف يتم تآكل طبقة الأوزون
الأضرار البيئية والصحية الناجمة عن تآكل طبقة الأوزون
ويعد تآكل طبقة الأوزون من أكبر الأمثلة على الخطر الماثل أمام سكان الأرض جميعا على اختلاف ظروفهم البيئية، ودون تحيز على نحو تحركت معه الجماعة الدولية بعيدا عن مجال النصح والإرشاد إلى وضع المسألة فى شكل قانونى بحت مقترن بالجزاء، وصار الالتزام الدولى بذلك من قبيل الالتزام بتحقيق نتيجة وليس الالتزام ببذل عناية أو ما يسمى بالالتزام بغاية نوهى فى بساطة التخلص إن عاجلا أو آجلا من المواد المستنفذة لطبقة الأوزون.
إن الأضرار البيئية الناتجة عن تآكل طبقة الأوزون تتمثل بصورة كبيرة في التغيرات المناخية الحادثة لكوكب الأرض ومنها التغيرات الفجائية في الطقس والمناخ والتصحر وحرائق الغابات والارتفاع في مستوي سطح البحر لشواطئ عديدة في العالم وإحداث خلل في التوازن البيئي والأضرار الصحية تتمثل في حدوث بعض سرطانات الجلد وضعف المناعة الطبيعية للإنسان وبعض أمراض العيون مثل عتامة العين إذا ما تعرض الكائنات الحية مثل الإنسان والحيوان لكميات كبيرة من الجزء الضار من الأشعة فوق البنفسجية.
raneem noor
التوازن
على الرغم من انتشار مفهوم التوازن بشكل واسع في العلوم، إلا أنه يظهر في أدبيات الكيمياء كلما توفر عدد من الحالات المختلفة في التركيب الكيميائي. على سبي المثال، في خليط من مركبات كيميائية مختلفة يمكنها التفاعل مع بعضها، أو مادة بمقدورها التواجد بأكثر من حالة. لا يعد نظام من المواد الكيميائية في حالة التوازن - على الرغم من امتلاكه لتركيب غير متغير - ثابتاً، لأن الجزيئات في حالة تفاعل مستمر مع بعضهاالبعض، وهذا يؤدي إلى ظهور حالة التوازن الدينامي. لذا فإن المفهوم يصف الحالة التي تكون فيها متغيرات مثل التركيب الكيميائي ثابتة مع مرور الوقت. لا تكون المواد الكيميائية الموجودة في الأنظمة الحية في حالة توازن، وإنما هي بعيدة جداً عن حالة التوازن.
سلمى المسدي
التفاعل
التفاعل الكيميائي هو تحول في التركيب الدقيق للجزيئات. ويمكن أن ينتج التفاعل الكيميائي من مهاجمة جزيئات لجزيئات أخرى لتكوين جزيئات أكبر, أو جزيئات تتفكك لتكوين جزيئين أو أكثر أقل حجما, أو إعادة ترتيب الذرات في نفس الجزيء أو خلال جزيئات أخرى. وتتضمن التفاعلات الكيميائية غالبا تكوين أو تكسير روابط كيميائية.
سلمى المسدي
الصناعة الكيميائية
تمثل الصناعة الكيميائية نشاطاً اقتصادياً مهماً، حيث قدرت مبيعات أكبر 50 مصنعاً للمواد الكيميائية في العالم سنة 2004 بـ 587 مليار دولار أمريكي وبهامش ربح 8.1% ومصاريف بحث وتطوير بنسبة 2.1% من مجمل المبيعات.[24]
سلمى المسدي
فروع الكيمياء
تقسم الكيمياء إلى عدة فروع رئيسية ومنها : تنقسم الكيمياء بصفة عامة إلى عدة فروع رئيسية، كما يوجد أيضا تفرعات لهذه الفروع, وموضوعات ذات تخصص أكبر داخل هذه الفروع.
الكيمياء التحليليةهي تحليل عينات من المادة لمعرفة التركيب الكيميائى لها وكيفية بنائها.الكيمياء الحيويةهي دراسة المواد الكيميائية، والتفاعلات الكيميائية التي تحدث في الكائنات الحية.الكيمياء غير العضويةهي دراسة خواص وتفاعلات المركبات غير العضوية. ولا يوجد هناك حد واضح للتفريق بين الكيمياء العضوية وغير العضوية، كما أن هناك تداخل كبير بينهما, ويكون أهمه في فرع آخر يسمى كيمياء الفلزات العضوية.كيمياء عضويةهي دراسة تركيب، وخواص، وتفاعلات المركبات العضوية.الكيمياء الفيزيائيةهي دراسة الأصل الفيزيائى للتفاعلات والأنظمة الكيميائية. ولمزيد من التحديد فإنها تدرس تغييريات حالات الطاقة في التفاعلات الكيميائية. ومن الفروع التي تهم الكيميائيين المتخصصين في الكيمياء الحرارية، الكيمياء الحركية،كيمياء الكم، الميكانيكا الإحصائية، علم الأطياف.
سلمى المسدي
قوانين الكيمياء
تخضع التفاعلات الكيميائية لقوانين محددة، والتي أصبحت مفاهيم أساسية في الكيمياء، وهذه بعض القوانين:
- قانون أفوجادرو
- قانون بير لامبرت
- قانون شارل
- قانون فيك للانتشار
- قانون جاي لوساك
- مبدأ لو شاتيليه
- قانون هنري
- قانون هس
- قانون بقاء الطاقة الذي أدى إلى اكتشاف مفاهيم مهمة مثل التوازن والديناميكا الحرارية والحركية الكيميائية.
- قانون بقاء المادة
- قانون النسب الثابتة
- قانون النسب المتضاعفة
- قانون راؤول
سلمى المسدي
الروابط الكيميائية
الرابطة الكيميائية هي القوة التي تربط الذرات في الجزيء أو في البلورة. في مركبات بسيطة عديدة, نظرية التكافؤ ومبدأ عدد التأكسد يمكن استخدامهما للتنبؤ بالتركيب الجزيئي. وبالمثل, فإن النظريات الفيزياء الكلاسيكية يمكن استخدامها للتنبؤ بتركيب مركبات أيونية عديدة. أما المركبات ذات التركيب المعقد، مثل السبائك المعدنية، فإن نظرية التكافؤ لا تستطيع تفسير تركيبها, وهنا تظهر أهمية استخدام نظريات الميكانيكا الكمية مثل نظرية المدار الجزيئي.
بعض أنواع الروابط الكيميائية:
- رابطة أيونية
- رابطة تساهمية
- رابطه قطبيه
- رابطة فلزية
- رابطة تناسقية
والرابطة التناسقية تنساق تحت الرابطة التساهمية تقريبا وتوجد رابطة أخرى وهي الرابطة الهيدروجينية وتتكون عن طريق اتحاد جزيئين بحيث يكون بكل جزئ ذرة هيدروجين وذرة أخرى ذات سالبيه كهربيه عاليه والذي يؤدى إلى وقوع ذرة الهيدروجين بين ذرتين ذات سالبيه كهربيه عاليه عند الاتحاد.
الرابطة الأيونية : تتكون غالباً بين الفلزات واللافلزات حيث تكون :
الفلزات : ذراتها حجمها كبير - جهد تأينها صغير (فيسهل فقد الكترونات المستوى الأخير) فيتكون أيون موجب ليصل لأقرب غاز خامل.
اللافلزات : صغيرة الحجم - ميلها الإلكتروني كبير (فيسهل اكتساب إلكترونات) فتصبح أيون سالب لتصل لأقرب غاز خامل (نبيل).
والربطة الأيونية هي : انجذاب كهربائي بين الأيون الموجب والسالب (وليس لها وجود مادي).
سلمى المسدي
المادة
المادة الكيميائية هي نوع من المادة له تركيب معلوم ومجموعة من الخواص.[22] ولكن وبشكل دقيق لا يعد مزيج من المركبات أو العناصر أو المركبات والعناصر مادة كيميائية. تعد الكثير من المواد التي نراها في حياتنا اليومية نوعاً من أنواع الأمزجة، مثل: الهواء، السبائك، والكتل الحيوية.
سلمى المسدي
المركب
المركب الكيميائي هو مادة تتكون من نسبة معينة من العناصر وتحدد تركيب المركب والمجموعة التي يقع فيها هذا المركب والتي تحدد بالتالى خواص هذا المركب. فمثلاً الماء هو مركب يحتوى على الهيدروجين الأكسجين بنسبة 2 إلى 1، حيث تكون ذرة الأكسجين محاطة بزوج من ذرات الهيدروجين وبزاوية قياسها 104.5 درجة. تتكون المركبات وتتحول عن طريق التفاعلات الكيميائية.
سلمى المسدي
العنصر
العنصر هو المادة المتكونة من نوع واحد من الذرات، ويمتلك العنصر الكيميائي عدداً ثابتاً ومحدداً من البروتونات في نواة ذرته، ويعرف هذا العدد بالعدد الذري للعنصر. فمثلاً جميع الذرات التي تمتلك 6 بروتونات في أنويتها هي ذرات عنصر الكربون، وجميع الذارت التي تمتلك 92 بروتوناً في أنويتها هي ذرات عنصر اليورانيوم. وهنالك 94 عنصراً متوفراً في الطبيعة بالإضافة إلى 18 عنصراً تم تصنيعها.
على الرغم من احتواء جميع ذرات العنصر الواحد على نفس عدد البروتونات فإن ليس من اللازم احتواءها على نفس عدد النيترونات، تسمى مثل هذه الذرات بالنظائر ويمكن أن يمتلك العنصر الواحد أكثر من نظير واحد.
أفضل تمثيل للعناصر الكيميائية هو الجدول الدوري والذي يرتب العناصر حسب عددها الذري، وتتشارك زمر ودورات العناصر في الجدول الدوري في بعض الخصائص أو تتبع نمطاً معيناً للخصائص، مثل قطر الذرة، والسالبية الكهربية، وغيرها
سلمى المسدي
الذرة
الذرة هي الوحدة الأساسية في الكيمياء، وتتكون من النواة موجبة الشحنة والتي تحتوي على البروتونات والنيترونات وتحتوي أيضاً عدداً من الإلكترونات التي تعمل على معادلة الشحنة الموجبة في النواة. كما أن الذرة هي أصغر وحدة يمكن تصورها والتي تكون قادرة على المحافظة على الخواص الكيميائية للعنصر، مثل السالبية الكهربية وطاقة التأين، حالات الأكسدة المفضلة، عدد التساند وعدد الروابط التي يفضل تشكيلها. (مثل الفلزية والأيونية والتساهمية).
سلمى المسدي
الكيمياء الحديثة
أنطوان لافوازييه عالم كيمياء فرنسي ، و معروف بأنه أبو الكيمياء الحديثة
يرجع تاريخ الكيمياء الحديثة إلى القرن السابع عشر الميلادي بأبحاث (بويل) الذي قسم الأجسام إلى مواد أولية(عناصر ومركبات ومخاليط) وتلت أبحاث (بلاك، ولافوازييه)عن الاحتراق والتأكسد ثم(برتلي) الذي اكتشف الأكسجين في الهواء، ثم(كافندش) الذي اكتشف تكوين الماء ثم (دالتون) الذي وضع النظرية الذرية عن تكون المادة وتعرّف الكيمياء الحديثة بأنها:- علم طبيعي في تكوين المادة والتغييرات التي تحدث فيها تحت تغييرات مختلفة تفقد الجسم مظهره الخاص وصفاته التي يتميز بها، إذ تتبدل مادته بأخرى ذات خواص وصفات جديدة وتوصف مظاهر المواد وسلوكها بالخواص الكيميائية، أي تعرّف بذلك وتبين تلك الخواص الكيميائية إبان التفاعلات بالمعادلات.
سلمى المسدي
تاريخ الكيمياء
الكيمياء هي إحدى العلوم الطبيعية التي عرفها الإنسان ومارسها منذ وقت بعيد لا تعرف له بداية، وقد ارتبط هذا الفن منذ الحضارات القديمة بالمعادن والتعدين وصناعة الألوان والطب والدواء وبعض الصناعات الفنية كدبغ الجلود وصبغ القماش وصناعة الزجاج، وحتى طبخ الطعام قد يصاحبه تغيرات كيميائية معينة مثل نبات الكاسافا الذي زرعه الأميرنديون في فنزويلا منذ آلاف السنين قبل الميلاد، وتحتوي جذور هذا النبات على حمض الهيدروسيانيك القاتل، وقد عرف الهنود الأمريكيون القدامى هذه المادة السامة وقاموا بالتخلص منها بالتسخين الذي يحول هذا الحمض إلى مواد غير سامة. واستخدم الإنسان منذ أكثر من ثلاثة آلاف سنة قبل الميلاد محلول الشب وبعض الصبغات المحضرة من العفص ولحاء بعض ثمار الأشجار وأوراق نبات السماق في تلوين الجلود والقماش. وما زال استخدام الصبغة المحضرة من أوراق وثمار نبات السماق موجوداً حتى اليوم للغرض نفسه في شمال العراق والشام وتركيا وغيرها. وقد نشأت الكيمياء كغيرها من العلوم في أروقة المعابد، وكانت من الفنون الخاصة جداً، وكانت حكراً على طائفة دون غيرها هم الكهنة.[6]
سلمى المسدي
النظرية
تبدأ الكيمياء التقليدية بدراسة الجسيمات الأولية والذرات والجزيئات والمواد الكيميائية والبلورات وأشكال التجمعات الأخرى للمادة وفي الحالة الصلبة والسائلة والغازية معزولة عن بعضها أو متحدة مع بعضها. تنتج التآثرات والتفاعلات والتحولات التي تدرسها الكيمياء من التآثر بين مواد كيميائية مختلفة أو بين المادة والطاقة. يدرس هذا السلوك في المختبروباستخدام أشكال مختلفة من الأدوات المختبرية.
مختبر في قسم الكيمياء الحيوية، جامعة كولونيا
التفاعل الكيميائي هو تحول بعض المواد إلى مادة أخرى أو أكثر.[5] ويمكن استخدام الرموز للتعبير عنه بواسطة معادلة كيميائية. غالباً ما يكون عدد الذرات في طرفي المعادلة متساوياً، وتكون طبيعة التفاعلات الكيميائية والتغيرات في الطاقة التي تحدث نتيجة لهذه التفاعلات محكومة بقوانين تسمى القوانين الكيميائية، وتعد ملاحظة الطاقة والإنتروبيا من الأمور المهمة في أغلب الدراسات الكيميائية.
تصنف المواد الكيميائية حسب بنيتها، والطور بالإضافة إلى تركيبها الكيميائي. ويمكن تحليلها باستخدام أدوات التحليل الكيميائي، مثل المطيافية والاستشراب.
سلمى المسدي
كيمياء
الكيمياء علم المادة، وبخاصة خواصها، بنيتها، تركيبها، سلوكها، تفاعلاتها، وتداخلاتها التي تحدثها.[1][2]
تسمى الكيمياء أحياناً بـ (العلم المركزي) لأنها تربط الفيزياء مع العلوم الطبيعية مثل علم الفلك والجيولوجيا وعلم الأحياء.[1][2] و يُعد تاريخ صناعة الكيمياء له أثرًا بالغًا في مجال الكيمياء بشكل عام.
تدرس الفيزياء المادة أيضاً ولكنها تدرس كميات الفضاء والمادة، والقوانين التي تحكمها، والكيمياء فرع من العلوم الفيزيائية ولكنها لا تتفرع عن الفيزياء.[3
سلمى المسدي
اشعة المهبط
أشعة المهبط أو أشعة الكاثود هي سيل من الأشعة غير المنظورة تنبعث من كاثود أنبوبة تفريغ كهربي ضغط الغاز فيها منخفض يتراوح بين 01. : 001. مم زئبق وفرق الجهدبين قطبي المصدر الكهربي يصل إلى 10000 فولت.
خواصها[عدل]
اروى الصافي
خواصها[عدل]
- تسير في خطوط مستقيمة من المهبط (الكاثود) إلى المصعد (الأنود) تبسيطاً بشكل موازٍ للحقل الكهربائي المطبق بين المصعد والمهبط.
- لها تأثير حراري حيث أنها تحدث توهج على جدار أنبوب التفريغ.
- تتكون من دقائق مادية صغيرة. أي ان لها كتلة
- تتأثر بالمجال المغناطيسي والكهربائي بطريقة تدل على أن شحنتها سالبة.
- لا تتغير بتغير نوع مادة المهبط أو نوع الغاز المخلخل مما يدل على انها تدخل في تركيب جميع المواد.
- تسير هذه الاشعة داخل الأنبوبة في خطوط مستقيمة تبسيطاً بشكل موازٍ للحقل الكهربائي المطبق بين المصعد والمهبط أي عمودياً على سطح المهبط (الكاثود). وكذلك لو نظرنا إلى أحد خصائص الضوء سنجدها تحمل صفة الاستقامة مثل أشعة الكاثود، بحيث لو أننا وضعنا جسماً معيناً في ضوء الشمس سيتكون ظل لهذا الجسم.
- عند اصطدام هذه الأشعة بسطح معدني رقيق فإنها ترفع درجة حرارته حتى التوهج (أي أنها تحمل طاقة حركية)، كذلك الضوء يحمل هذه الصفة، حيث لو أننا لمسنا مصباح سيارة مثلا بعد مشوار طويل في الليل سنجد أنه ساخن أي يحمل طاقة حرارية فهذه الطاقة تحولت من الطاقة الضوئية.
- تحرك عجلة خفيفة عند اصطدامها بها أي أن لها كمية حركة (أو كتلة)، ولكن لونظرنا إلى الضوء سنجد أنه لا يحمل هذه الصفة، حيث لو أننا سلطنا مصباح على مروحة قابلة للدوران حول محور لن تدور هذه المروحة ولكن سيحدث العكس عند أشعة الكاثود (أي ستدور المروحة).
- تنحرف هذه الأشعة عند دخولها مجالاً مغناطيسياً عمودياً على اتجاهها (أي أنها تمتلك شحنات كهربائية سالبة)، ولكن لو سلطنا ضوء مصباح على المولد الكهربائي سنجد أن الضوء يسير بلا انحراف أو تكسر أو حيود فهذا يفسر أن الضوء لا يحمل هذه الصفة ولا يتأثر بالمجال المغناطيسي.
اروى الصافي
تفاعلات كيميائية مذهلة وغريبة
اروى الصافي
الأوزون هو غاز ذو لون ازرق | يتكون من ثلاث ذرات من الأكسجين صيغته الكيميائية O3 ،ونسبته في الغلاف الجوى ضئيلة قد لا تتجاوز في بعض المناطق واحد في المليون وهو غاز سام.
مكان الأوزون اين يوجد الاوزون.
يوجد الأوزون طبيعياً في طبقة الستراتوسفير ويرجع وجودة إلى سلسلة من التفاعلات بين الأكسجين الجزئى والذرى ولايبقى الأوزون المتكون لفترة وجيزه ثم يتفكك بفعل ضوء الشمس إلى جزئي أكسجين ثم يتكون وفى النهاية نحصل على شكل يبقى دائماً على طبقة من الأوزون في منطقة الستراتوسفير متوازنة وهذا التوازون يعتمد على سرعة تكوينه وسرعة تفكك الأوزون. وعندما يحدث تداخل لبعض المواد مع هذة السرعة يحدث خللا في الاتزان، إما بزيادة تركيز الأوزون أو بالعكس تحلل الأوزون من منطقة الستراتوسفير
هل غاز الأوزون في طبقات الجو السفلى
على العكس من طبقات الجو العليا فان تواجد الاوزون في طبقات الجو السفلى يسبب اضرار كبيرة. فاستنشاق جزء يسير من الاوزون مع الهواء يسبب صداع واثار صحية غير محمودة. كما أنه يؤثر على الريئتين ويضعف مقاومتها للبكتريا وقد يسبب تحطما للخلايا. كما أنه يدمر المطاط والبوليمرات ويجعل عمرها اقصر وخصوصا اطارات السيارات. والسبب الرئيسي لتكون الاوزون في الطبقات السفلى هو عادم السيارات.
ماهو تأثير الأوزون على الحياة
وجود الأوزون في الغلاف الجوي يعمل كحاجب طبيعي يقوم بعملية تنظيف أو تعقيم البيئة بالإضافة إلى حماية الأرض من الأشعة فوق البنفسجية التي تصلنا من الشمس والتي يتولى الأوزون امتصاص أكثرمن 99% منها، وبذلك يحمى أشكال الحياة المعروفة على سطح الأرض.
اروى الصافي
مكان الأوزون اين يوجد الاوزون.
يوجد الأوزون طبيعياً في طبقة الستراتوسفير ويرجع وجودة إلى سلسلة من التفاعلات بين الأكسجين الجزئى والذرى ولايبقى الأوزون المتكون لفترة وجيزه ثم يتفكك بفعل ضوء الشمس إلى جزئي أكسجين ثم يتكون وفى النهاية نحصل على شكل يبقى دائماً على طبقة من الأوزون في منطقة الستراتوسفير متوازنة وهذا التوازون يعتمد على سرعة تكوينه وسرعة تفكك الأوزون. وعندما يحدث تداخل لبعض المواد مع هذة السرعة يحدث خللا في الاتزان، إما بزيادة تركيز الأوزون أو بالعكس تحلل الأوزون من منطقة الستراتوسفير
هل غاز الأوزون في طبقات الجو السفلى
على العكس من طبقات الجو العليا فان تواجد الاوزون في طبقات الجو السفلى يسبب اضرار كبيرة. فاستنشاق جزء يسير من الاوزون مع الهواء يسبب صداع واثار صحية غير محمودة. كما أنه يؤثر على الريئتين ويضعف مقاومتها للبكتريا وقد يسبب تحطما للخلايا. كما أنه يدمر المطاط والبوليمرات ويجعل عمرها اقصر وخصوصا اطارات السيارات. والسبب الرئيسي لتكون الاوزون في الطبقات السفلى هو عادم السيارات.
ماهو تأثير الأوزون على الحياة
وجود الأوزون في الغلاف الجوي يعمل كحاجب طبيعي يقوم بعملية تنظيف أو تعقيم البيئة بالإضافة إلى حماية الأرض من الأشعة فوق البنفسجية التي تصلنا من الشمس والتي يتولى الأوزون امتصاص أكثرمن 99% منها، وبذلك يحمى أشكال الحياة المعروفة على سطح الأرض.
اروى الصافي
اكتشاف الذرة
وابدا في تعريف الذرة
حيث تعرف بانها اصغر بناء في العنصر وتتكون من نواة بها بروتون موجبة الشحنة ونيترون متعادلة الشحنة ويدور حوله في مدارات خارجية الكترون سالبة الشحنة
وتبدا قصتنا بالعالم جوزيف جون طومسن : الذي ولد عام 1856 ميلادي بالقرب من مانشستر بانجلترا وتوفي عام 1940 ميلادي حيث شغل عدة مناصب منها استاذ كافندش للفيزياء بجامعة كامبرج و منصب لاستاذ في الفيزياء بالمعهد الملكي بلندن وحصل علي جائزة نوبل للفيزياء عام 1906 ميلادي .
حيث اكتشف طومسن نموذجه للذرة عام 1897 حيث اعتبرت اول نموذج يتم اكتشافه للذرة والذي ينص علي ان الذرة عبارة عن نواة موجبة الشحنة كرة الشكل مرصعة بلالكترونات سالبة الشحنة
ولكن سرعان ما بطل هاذة النموذج بعدة تجربة روذرفورد علي ذره الهليوم
وهذه معلومات موجزة عن شخصيتنا الثانية :
حيث ولد روذرفورد عام 1871 ميلادي بالقرب من نيلسون بنيوزيلندا وتوفي عام 1937 ميلادي بعد شغل منصب الاساتذة في جامعة ماكجيل بمونتريال بكندا قبل الانتقال الي جامعة مانشيستر عام 1907 ميلادي وفي عام 1919 ميلادي خلف طومسن في كرسي كافندش بجامعة كامبرج وقد تسلم جائزة نوبل في الفيزياء عام 1908 ميلادي .
حيث قام روذرفورد بتجربته الشهيرة ( انحراف جسيمات الفا عن نواة ذرة الهليوم )
حيث لاحظ روذرفورد ان الجسيمات عندما تكون بعيدة عن النواة فانها لاتنحرف فتبقي علي ذالك السلوك حتي تصل الي بعد معين فيظهر الانحراف وهاذ يعني ان هناك فراغ بين الجسيمات السالبة والجسيمات الموجبة حيث ان جسيمة الفا موجبة الشحنة فلذلك لا تعاني اي انحراف عندما تمر باقرب من الجسيمات السالبة وتنحرف عندما تقترب من الجسيمات الموجبة وهذا يدلا علي ان النواة ليست مرصعة بالاكترونات كما ذكر طومسن ولكنها موجودة خارج النواة
ويبقى السوال الذي يطرح نفسه .
ماهو وضع سلوك الاكترونات خارج النواة ؟
وقد جاوب العالم نيلز هينريك بوهر وهذه بعض المعلومات الموجزة عليه
حيث ولد بوهر عام 1885 ميلادي في كوبنهاجن بالدينمارك وتوفي عام 1962 ميلادي بعد ان درس في جامعة كوبنهاجن انتقل الي مانشستر ليعمل مع روذرفورد في عام 1912 ميلادي ونشر بحثه الشهير في تركيب الذرة
و في عام 1916 ميلادي اصبح استاذ للطبيعة النظرية في جامعة كوبنهاجن واصبح معهده للفيزياء النظرية ( المؤسس عام 1921 ميلادي )
حيث اكتشف بوهر نموذجه عام 1912 ميلادي الذي نص علي هيئة فرضيتين وهما :
الفرضية الاولى : تدور الالكترونات حول النواة في مسارات بيضاوية الشكل ثابتة غير مستمرة تسمى بمستويات الطاقة ولتي يحددها الزخم الزاوي للالكترون والذي يجب ان تساوى اعداد ثابتة من ثابت بلانك
الفرضية الثانية : يمكن للالكترون ان ينتقل من مدار لاخر بفقد او اكتساب طاقة ولتي عبارة عن الفرق بين طاقة المستويين
واصبح هذا النموذج هو المعتمد بالنسبة للذرة حتي اليوم مع بعض التعديلات التي اجراها كل من باولي وديبروري وهايزنبرغ وشرودنجر
ويعتبرون هاؤلاء العلماء هم رواد الفيزياء الكمية التي تختلف اختلاف كبيرا عن الفيزياء الكلاسيكية
اروى الصافي
حيث تعرف بانها اصغر بناء في العنصر وتتكون من نواة بها بروتون موجبة الشحنة ونيترون متعادلة الشحنة ويدور حوله في مدارات خارجية الكترون سالبة الشحنة
وتبدا قصتنا بالعالم جوزيف جون طومسن : الذي ولد عام 1856 ميلادي بالقرب من مانشستر بانجلترا وتوفي عام 1940 ميلادي حيث شغل عدة مناصب منها استاذ كافندش للفيزياء بجامعة كامبرج و منصب لاستاذ في الفيزياء بالمعهد الملكي بلندن وحصل علي جائزة نوبل للفيزياء عام 1906 ميلادي .
حيث اكتشف طومسن نموذجه للذرة عام 1897 حيث اعتبرت اول نموذج يتم اكتشافه للذرة والذي ينص علي ان الذرة عبارة عن نواة موجبة الشحنة كرة الشكل مرصعة بلالكترونات سالبة الشحنة
ولكن سرعان ما بطل هاذة النموذج بعدة تجربة روذرفورد علي ذره الهليوم
وهذه معلومات موجزة عن شخصيتنا الثانية :
حيث ولد روذرفورد عام 1871 ميلادي بالقرب من نيلسون بنيوزيلندا وتوفي عام 1937 ميلادي بعد شغل منصب الاساتذة في جامعة ماكجيل بمونتريال بكندا قبل الانتقال الي جامعة مانشيستر عام 1907 ميلادي وفي عام 1919 ميلادي خلف طومسن في كرسي كافندش بجامعة كامبرج وقد تسلم جائزة نوبل في الفيزياء عام 1908 ميلادي .
حيث قام روذرفورد بتجربته الشهيرة ( انحراف جسيمات الفا عن نواة ذرة الهليوم )
حيث لاحظ روذرفورد ان الجسيمات عندما تكون بعيدة عن النواة فانها لاتنحرف فتبقي علي ذالك السلوك حتي تصل الي بعد معين فيظهر الانحراف وهاذ يعني ان هناك فراغ بين الجسيمات السالبة والجسيمات الموجبة حيث ان جسيمة الفا موجبة الشحنة فلذلك لا تعاني اي انحراف عندما تمر باقرب من الجسيمات السالبة وتنحرف عندما تقترب من الجسيمات الموجبة وهذا يدلا علي ان النواة ليست مرصعة بالاكترونات كما ذكر طومسن ولكنها موجودة خارج النواة
ويبقى السوال الذي يطرح نفسه .
ماهو وضع سلوك الاكترونات خارج النواة ؟
وقد جاوب العالم نيلز هينريك بوهر وهذه بعض المعلومات الموجزة عليه
حيث ولد بوهر عام 1885 ميلادي في كوبنهاجن بالدينمارك وتوفي عام 1962 ميلادي بعد ان درس في جامعة كوبنهاجن انتقل الي مانشستر ليعمل مع روذرفورد في عام 1912 ميلادي ونشر بحثه الشهير في تركيب الذرة
و في عام 1916 ميلادي اصبح استاذ للطبيعة النظرية في جامعة كوبنهاجن واصبح معهده للفيزياء النظرية ( المؤسس عام 1921 ميلادي )
حيث اكتشف بوهر نموذجه عام 1912 ميلادي الذي نص علي هيئة فرضيتين وهما :
الفرضية الاولى : تدور الالكترونات حول النواة في مسارات بيضاوية الشكل ثابتة غير مستمرة تسمى بمستويات الطاقة ولتي يحددها الزخم الزاوي للالكترون والذي يجب ان تساوى اعداد ثابتة من ثابت بلانك
الفرضية الثانية : يمكن للالكترون ان ينتقل من مدار لاخر بفقد او اكتساب طاقة ولتي عبارة عن الفرق بين طاقة المستويين
واصبح هذا النموذج هو المعتمد بالنسبة للذرة حتي اليوم مع بعض التعديلات التي اجراها كل من باولي وديبروري وهايزنبرغ وشرودنجر
ويعتبرون هاؤلاء العلماء هم رواد الفيزياء الكمية التي تختلف اختلاف كبيرا عن الفيزياء الكلاسيكية
اروى الصافي
الكيمياء الدوائية
لكيمياء الصيدلانية أو الكيمياء الدوائية هو تخصص علمي يجمع بين الكيمياء والصيدلة بهذف تصميم المركبات الدوائية الجديدة وتطويرها. تقوم الكيمياء الصيدلانية بتمييز وتصنيع وتطوير المركبات الكيميائية الجديدة لتناسب الإستخدامات العلاجية: بمعنى زيادة التأثير العلاجي لها وإنقاص الآثار الجانبي. من أجل ذلك تستخدم الكثير من التقنيات الكيميائية والتقنية وأيضا تطبيقات الكيمياء الحاسوبية الجديدة لدراسة الأدوية المستخدمة وتأثيراتها الحيوية، من أهم هذه التقنيات علاقة البنية-تأثير (سار) وعلاقة بنية-تأثير الكمية (كيوسار).
وهي فرع من الكيمياء يدرس المركبات الدوائية وخواصها كما يدرس طرق معايرتها وتحديد ذاتيتها تنقسم لفرع عضوي وقسم لا عضوي. ان الكتب المرجعية لهذا العلم يجب ان تتضمن تصنيفا شاملا للاعداد الهائلة من الأدوية المتوفرة في السوق التجارية بحسب زمر فارماكوجية او كيميائية تبرز ما يطلق عليه علاقة البنية-التأثير لأفراد كل زمرة بعينها ويجب ان توفر هذه المراجع معلومات مثل الخواص الفيزيائية و الكيميائية والاستعمال والتاثيرات الجانبية والمقدار الدوائي وفيما عدا هذه المعلومات ثمة اختلافات واسعة بين كل كتاب مرجعي وأخر في مجال الكيمياء الصيدلية اذ ان بعضها يذهب الى الاهتمام بدراسة الأدوية من حيث الانحلال و الارتباط بالبروتينات والامتصاص والأطراح وبعضها يذهب الى الاهتمام بدراسة الطرق التحليلية لهذه الادوية
وقد اختلفت النظرة الى الكيمياء الصيدلية بأختلاف التوجهات الحديثة في تدريس الصيدلة وأول هذه التوجهات انطلقت من مفهوم الاهتمام بالدواء الى الاهتمام بمصير الدواء لدى المريض الى الاهتمام بدواء الحالة السريريةالى الاهتمام بتخليق وتصنيع الدواء من منشأ بيولوجي .وغيرها من التوجهات التي تعتمدها مدارس الصيدلة في مختلف أنحاء العالم
عملية اكتشاف الأدويةاكتشاف الأدويةالمقالة الرئيسية: اكتشاف الأدوية
في مجالات الطب ، التكنولوجيا الحيوية وعلم الدواء ، اكتشاف الأدوية هي العملية التي يتم من خلالها اكتشاف الأدوية و/أو تصميمها. في الماضي كانت أكثر الأدوية التى تم اكتشاف إما عن طريق تحديد العنصر النشط منالعلاجات التقليدية أو عن طريق الصدفة. وثمة نهج جديد لفهم كيف أن المرض و العدوى يتم ضبطهما بمستوى جزيئي وفسيولوجي واستهداف كيانات معينة على أساس هذه المعرفة.
التحسينوهنالك خطوة أخرى في اكتشاف الدواء تشمل تعديلات كيميائية إضافية لتحسين الخصائص البيولوجية والفيزيوكيميائية لجمهرة المركبات المرشحة، ويمكن أن تحسن التعديلات الكيميائية من هندسة التعرف والإرتباط geometries (pharmacophores للمركبات المقصودة ودرجة ألفتها وحرائكها الدوائية أو بالحقيقة تفاعليتها وثباتها خلال تدركها الاستقلابي، وقد ساهمت عدة طرق في توقع السلوك الاستقلابي المحسوب كمياً ومن الأملثلة الحديثة SPORCalc[1].
علاقة بنية-تأثير الكمية (كيوسار) quantitative structure-activity relationship QSAR لفاماكفور pharmacophore لها دور هام في الحصول على المركب الرائد lead compound الذي يبدي أشد الفعالية وأكثر الانتقائية وأفضل الحرائك الدوائية وأقل السمية. الكيوسار يشمل استخدام الكيمياء الفيزيائية وأدوات التحكم بالجزيئات molecular docking tools (CoMFA and CoMSIA) التي تعطينا بيانات مجدولة ومعادلات من الرتبة الأولى والثانية. وتوجد كثير من النظريات منها تحليل هانش Hansch's analysis ويشمل متثابتات (بارميترات) هاميت Hammett الإلكترونية ومتثابتات steric ومتثابتات logP(lipophilicity)
اروى الصافي
وهي فرع من الكيمياء يدرس المركبات الدوائية وخواصها كما يدرس طرق معايرتها وتحديد ذاتيتها تنقسم لفرع عضوي وقسم لا عضوي. ان الكتب المرجعية لهذا العلم يجب ان تتضمن تصنيفا شاملا للاعداد الهائلة من الأدوية المتوفرة في السوق التجارية بحسب زمر فارماكوجية او كيميائية تبرز ما يطلق عليه علاقة البنية-التأثير لأفراد كل زمرة بعينها ويجب ان توفر هذه المراجع معلومات مثل الخواص الفيزيائية و الكيميائية والاستعمال والتاثيرات الجانبية والمقدار الدوائي وفيما عدا هذه المعلومات ثمة اختلافات واسعة بين كل كتاب مرجعي وأخر في مجال الكيمياء الصيدلية اذ ان بعضها يذهب الى الاهتمام بدراسة الأدوية من حيث الانحلال و الارتباط بالبروتينات والامتصاص والأطراح وبعضها يذهب الى الاهتمام بدراسة الطرق التحليلية لهذه الادوية
وقد اختلفت النظرة الى الكيمياء الصيدلية بأختلاف التوجهات الحديثة في تدريس الصيدلة وأول هذه التوجهات انطلقت من مفهوم الاهتمام بالدواء الى الاهتمام بمصير الدواء لدى المريض الى الاهتمام بدواء الحالة السريريةالى الاهتمام بتخليق وتصنيع الدواء من منشأ بيولوجي .وغيرها من التوجهات التي تعتمدها مدارس الصيدلة في مختلف أنحاء العالم
عملية اكتشاف الأدويةاكتشاف الأدويةالمقالة الرئيسية: اكتشاف الأدوية
في مجالات الطب ، التكنولوجيا الحيوية وعلم الدواء ، اكتشاف الأدوية هي العملية التي يتم من خلالها اكتشاف الأدوية و/أو تصميمها. في الماضي كانت أكثر الأدوية التى تم اكتشاف إما عن طريق تحديد العنصر النشط منالعلاجات التقليدية أو عن طريق الصدفة. وثمة نهج جديد لفهم كيف أن المرض و العدوى يتم ضبطهما بمستوى جزيئي وفسيولوجي واستهداف كيانات معينة على أساس هذه المعرفة.
التحسينوهنالك خطوة أخرى في اكتشاف الدواء تشمل تعديلات كيميائية إضافية لتحسين الخصائص البيولوجية والفيزيوكيميائية لجمهرة المركبات المرشحة، ويمكن أن تحسن التعديلات الكيميائية من هندسة التعرف والإرتباط geometries (pharmacophores للمركبات المقصودة ودرجة ألفتها وحرائكها الدوائية أو بالحقيقة تفاعليتها وثباتها خلال تدركها الاستقلابي، وقد ساهمت عدة طرق في توقع السلوك الاستقلابي المحسوب كمياً ومن الأملثلة الحديثة SPORCalc[1].
علاقة بنية-تأثير الكمية (كيوسار) quantitative structure-activity relationship QSAR لفاماكفور pharmacophore لها دور هام في الحصول على المركب الرائد lead compound الذي يبدي أشد الفعالية وأكثر الانتقائية وأفضل الحرائك الدوائية وأقل السمية. الكيوسار يشمل استخدام الكيمياء الفيزيائية وأدوات التحكم بالجزيئات molecular docking tools (CoMFA and CoMSIA) التي تعطينا بيانات مجدولة ومعادلات من الرتبة الأولى والثانية. وتوجد كثير من النظريات منها تحليل هانش Hansch's analysis ويشمل متثابتات (بارميترات) هاميت Hammett الإلكترونية ومتثابتات steric ومتثابتات logP(lipophilicity)
اروى الصافي
دور الكيمياء في حياتنا
تلعب الكيمياء دورًا هامًا في حياتنا، إذ نجدها تدخل في الصناعة والزراعة والطب، وقد مرت بمراحل عديدة إلى أن وصلت لما هي عليه الآن. كانت أول تلك المراحل مرحلة علم الصنعة والتي زعم وقتها إمكانية تحويل المعادن الرخيصة إلى معادن ثمينة، ثم كانت المرحلة الثانية وهى مرحلة الكيمياء التي اتجهت إلى الطب، ففي هذه المرحلة تم تحضير وتصنيع بعض الأدوية الهامة التي تساعد في علاج المرضى، وكان جابر بن حيان وابن سينا وأبو بكر الرازي أشهر العلماء المسلمين اللذين تركوا بصمة في هذا المجال. وتأتى مرحلة هامة من تلك المراحل وهى مرحلة نظرية الفلوجستون والتي أقرت أن هناك عنصر يساعد المادة على الاشتعال ويتحد معها مكونا أكسيد المادة و أسموه الكالكس وقد بقيت النظرية سائدة حتى أتى العالم الفرنسي لافوازيه عام 1778م وأثبت خطأ هذه النظرية عندما سخن الزئبق وبرهن أن عملية الاحتراق عبارة عن اتحاد أكسجين الهواء بالمادة (تأكسد) وليس كما قالت نظرية فلوجستون. المرحلة الرابعة والأخيرة هي علم الكيمياء الحديثة التي بدأت في أواخر القرن الثامن عشر، والتي تشعبت لتصل إلى أكثر من فرع مثل الكيمياء التحليلية، الكيمياء الحيوية، كيمياء بيئية، الكيمياء اللاعضوية، الكيمياء الطبية، الكيمياء النووية، الكيمياء العضوية، الكيمياء الدوائية، الكيمياء الفيزيائية.
الكيمياء والصناعة تدخل الكيمياء فى الكثير من عمليات التصنيع مثل صناعة البلاستيك والاسمنت وكل مواد البناء وصناعة الزجاج، و إنتاج البتروكيماويات، الدواء البوليمرات ، الطلاءات ، الزيوت، ويتم استخدام علوم الكيمياء والتفاعلات الكيميائية لإنتاج مواد جديدة ، أو فصل المواد من بعضها باستخدام طرق كيميائية خاصة. مثال..كيفية تصنيع البلاستيك البلاستيك مواد يمكن تشكيلها بسهولة، أصلها مركبات كيميائية يتم الحصول عليها من النفط، يتركب البلاستيك من مركبات ذات سلاسل طويلة تسمى بالبلمرات(polymers) ، الترتيب المميز لتلك المركبات يمنح البلاستيك مزايا متعددة، إن البلاستيك الصلب يستبدل المعادن في كثير من الأدوات ،أما البلاستيك الطري فيدخل في صناعة الخيوط والجلود وحتى الفرو .البلاستيك من المكونات الطبيعية. في عام 1862م صنع الكيميائي ألكسندر باركز Alexander Parkes أول شكل للبلاستيك من مادة نترات السيلولوز. شاهده الناس في معرض لندنLondon exhibition ثم طور هذا الشكل على يد الأمريكي جون وبسلي ، الذي سماها بالسليليود Celluloid فيما بعد، ومع أن السيليلود كان هشاً ويتغير لونه عند التعرض للضوء الشديد، فقد استعمل في صناعة كرات البلياردو والأسنان الصناعية والأفلام الفوتوغرافية.
صناعة الأسمنت تعد من الصناعات الهامة لكونها ترتبط مباشرة بأعمال الإنشاء والتعمير. ويستخدم الأسمنت كمادة رابطة هيدروليكية من مكونات المونة أو الخرسانة.وهي مع ذلك صناعة بسيطة مقارنة بالصناعات الكبرى،وتعتمد على توفر المواد الخام اللازمة لذلك. يتكون الأسمنت من خليط من الطفل (Clay) والحجر الجيري (Limestone)، والذي يسخن في درجة حرارة كافية لإحداث التفاعل بينهما لإنتاج سليكات الكالسيوم (Calcium Silicate). وتختلف الملوثات الناتجة عن مصانع الأسمنت من حيث المكونات والكمية، تبعاً لاختلاف عمليات التشغيل من مصنع لآخر وإجراءات النظافة العامة المتبعة، وعوامل أخرى متنوعة.وتعتمد فكرة التصنيع على طريقتين يعرفان بعملية الترطيب والتجفيف (Wet & Dry Processes)، في العمليات الرطبة تطحن المواد الخام وتخلط بالمياه، ثم يفصل الناتج المعلق (Slurry) إلى الفرن، أما في العمليات الجافة فيتم تجفيف المواد الخام قبل أو أثناء الطحن أي قبل إدخالها إلى الفرن. وقد تدخل بعض المواد الكيميائية الأخرى في اختبارات تحليل الجودة والتحكم فيها، مثلا الزيوت تستخدم لصيانة الآلات، والغاز الطبيعي والمازوت لتوليد غازات الاحتراق المستخدمة في الأفران، وتكون الأفران مجهزة بحيث تستطيع حرق أكثر من نوع واحد من أنواع الوقود.
صناعة الزجاجتعد صناعة الزجاج من الصناعات السهلة، من الصناعات القديمة التي اعتمدت علي المهارة اليدوية الفائقة حيث أبدع القدماء في تشكيل الزجاج وتكوينه ونقشه. مواد التصنيع :
1- الرمل أو السيليكا: يشكل حمض السيليكون المادة الأساسية التي يصنع منها الزجاج العادي ونحصل عليه من الرمل ولا يستخدم رمل الكوارتز نظرا للصعوبات وارتفاع تكلفة التحضير للصناعة.ويشترط في الرمل المستخدم أن يحتوي على نسبة عالية من أكسيد السيليكون تصل إلى 80% وأن تكون نسبة الشوائب قليلة خاصة الملونة مثل مركبات الحديد .
2- مركبات الصوديوم: حيث يعمل أكسيد الصوديوم على تقليل درجة الانصهار ويساعد في تشكيل الزجاج.
3- الكالسيوم والدولوميت: حيث يساعد أكسيد الكالسيوم على تصليب الزجاج.
4- الفلدسبار: يستخدم بشكل كبير لوجوده بشكل نقي كما انه رخيص الثمن وينصهر بسهولة.
5- البوراكس: يحتوي على أكسيدي الصوديوم والبورون حيث أن هذه المادة تنصهر بشكل جيد وتقلل من معامل تمدد الزجاج . ولذلك نجد أن الزجاج الحاوي نسبة كبيرة من أكسيد البورون لا ينكسر إذا سخن أو برد فجأة. مواد
أخرى:وتضم المواد التي تضاف لتحسين نوعية الزجاج كالمواد الملونة ومسرعات الانصهار والشفافية مثل أكسيد الرصاص وأكسيد التيتانيوم وأكسيد الباريوم.
اروى الصافي
الكيمياء والصناعة تدخل الكيمياء فى الكثير من عمليات التصنيع مثل صناعة البلاستيك والاسمنت وكل مواد البناء وصناعة الزجاج، و إنتاج البتروكيماويات، الدواء البوليمرات ، الطلاءات ، الزيوت، ويتم استخدام علوم الكيمياء والتفاعلات الكيميائية لإنتاج مواد جديدة ، أو فصل المواد من بعضها باستخدام طرق كيميائية خاصة. مثال..كيفية تصنيع البلاستيك البلاستيك مواد يمكن تشكيلها بسهولة، أصلها مركبات كيميائية يتم الحصول عليها من النفط، يتركب البلاستيك من مركبات ذات سلاسل طويلة تسمى بالبلمرات(polymers) ، الترتيب المميز لتلك المركبات يمنح البلاستيك مزايا متعددة، إن البلاستيك الصلب يستبدل المعادن في كثير من الأدوات ،أما البلاستيك الطري فيدخل في صناعة الخيوط والجلود وحتى الفرو .البلاستيك من المكونات الطبيعية. في عام 1862م صنع الكيميائي ألكسندر باركز Alexander Parkes أول شكل للبلاستيك من مادة نترات السيلولوز. شاهده الناس في معرض لندنLondon exhibition ثم طور هذا الشكل على يد الأمريكي جون وبسلي ، الذي سماها بالسليليود Celluloid فيما بعد، ومع أن السيليلود كان هشاً ويتغير لونه عند التعرض للضوء الشديد، فقد استعمل في صناعة كرات البلياردو والأسنان الصناعية والأفلام الفوتوغرافية.
صناعة الأسمنت تعد من الصناعات الهامة لكونها ترتبط مباشرة بأعمال الإنشاء والتعمير. ويستخدم الأسمنت كمادة رابطة هيدروليكية من مكونات المونة أو الخرسانة.وهي مع ذلك صناعة بسيطة مقارنة بالصناعات الكبرى،وتعتمد على توفر المواد الخام اللازمة لذلك. يتكون الأسمنت من خليط من الطفل (Clay) والحجر الجيري (Limestone)، والذي يسخن في درجة حرارة كافية لإحداث التفاعل بينهما لإنتاج سليكات الكالسيوم (Calcium Silicate). وتختلف الملوثات الناتجة عن مصانع الأسمنت من حيث المكونات والكمية، تبعاً لاختلاف عمليات التشغيل من مصنع لآخر وإجراءات النظافة العامة المتبعة، وعوامل أخرى متنوعة.وتعتمد فكرة التصنيع على طريقتين يعرفان بعملية الترطيب والتجفيف (Wet & Dry Processes)، في العمليات الرطبة تطحن المواد الخام وتخلط بالمياه، ثم يفصل الناتج المعلق (Slurry) إلى الفرن، أما في العمليات الجافة فيتم تجفيف المواد الخام قبل أو أثناء الطحن أي قبل إدخالها إلى الفرن. وقد تدخل بعض المواد الكيميائية الأخرى في اختبارات تحليل الجودة والتحكم فيها، مثلا الزيوت تستخدم لصيانة الآلات، والغاز الطبيعي والمازوت لتوليد غازات الاحتراق المستخدمة في الأفران، وتكون الأفران مجهزة بحيث تستطيع حرق أكثر من نوع واحد من أنواع الوقود.
صناعة الزجاجتعد صناعة الزجاج من الصناعات السهلة، من الصناعات القديمة التي اعتمدت علي المهارة اليدوية الفائقة حيث أبدع القدماء في تشكيل الزجاج وتكوينه ونقشه. مواد التصنيع :
1- الرمل أو السيليكا: يشكل حمض السيليكون المادة الأساسية التي يصنع منها الزجاج العادي ونحصل عليه من الرمل ولا يستخدم رمل الكوارتز نظرا للصعوبات وارتفاع تكلفة التحضير للصناعة.ويشترط في الرمل المستخدم أن يحتوي على نسبة عالية من أكسيد السيليكون تصل إلى 80% وأن تكون نسبة الشوائب قليلة خاصة الملونة مثل مركبات الحديد .
2- مركبات الصوديوم: حيث يعمل أكسيد الصوديوم على تقليل درجة الانصهار ويساعد في تشكيل الزجاج.
3- الكالسيوم والدولوميت: حيث يساعد أكسيد الكالسيوم على تصليب الزجاج.
4- الفلدسبار: يستخدم بشكل كبير لوجوده بشكل نقي كما انه رخيص الثمن وينصهر بسهولة.
5- البوراكس: يحتوي على أكسيدي الصوديوم والبورون حيث أن هذه المادة تنصهر بشكل جيد وتقلل من معامل تمدد الزجاج . ولذلك نجد أن الزجاج الحاوي نسبة كبيرة من أكسيد البورون لا ينكسر إذا سخن أو برد فجأة. مواد
أخرى:وتضم المواد التي تضاف لتحسين نوعية الزجاج كالمواد الملونة ومسرعات الانصهار والشفافية مثل أكسيد الرصاص وأكسيد التيتانيوم وأكسيد الباريوم.
اروى الصافي
الانوية الغير مستقره والتحلل الاشعاعي
النشاط الإشعاعي : الأشعة والجسيمات المنبعثة من المواد المشعة.
التفاعل النووي : تغير في نواة الذرة.
التحلل الإشعاعي : عملية تفقد خلالها الأنوية غير المستقرة طاقة بإصدار إشعاعات في عملية تلقائية تسمى التحلل الإشعاعي.أنواع الإشعاع توجد ثلاثة أنواع من الإشعاع النشط: جسيمات ألفا، وكان بكويريل أول من تعرف عليها؛ وجسيمات بيتا التي تعرف عليها النيوزيلندي إرنست رذرفورد؛ وأشعة جاما التي تعرف عليها الزوجان الفرنسيان ماري وبيير كوري.
جسيمات ألفا. تحمل شحنات كهربائية موجبة. ويتركب جسيم ألفا من بروتونين ونيوترونين، أي أنه يماثل نواة ذرة الهيليوم. تنطلق جسيمات ألفا بطاقات عالية، ولكنها سرعان ما تفقدها عند مرورها في المادة. وبمقدور ورقتين من أوراق هذه الموسوعة إيقافها.
جسيمات بيتا. وهي إلكترونات. تطلق بعض النوي المشعة إلكترونات عادية تحمل شحنات كهربائية سالبة. لكن البعض الآخر يطلق بوزيترونات وهي إلكترونات ذات شحنة موجبة. وتنتقل جسيمات بيتا بسرعة تقارب سرعة الضوء ويستطيع بعضها أن ينفذ خلال 13ملم من الخشب.
أشعة جاما. أشعة غير مشحونة كهربائيًا. وتشبه هذه الأشعة الأشعة السينية، إلا أنها تكون في الغالب ذات طولٍ موجي أصغر. وهذه الأشعة هي فوتونات (جسيمات الإشعاع الكهرومغنطيسي)، وتنتقل بسرعة الضوء. تخترق أشعة جاما الأجسام بدرجةٍ أكبر من جسيمات ألفا أو بيتا.
نجلة محمد قستي
الذرة
هي أصغر جزء من العنصر الكيميائي الذي يحتفظ بالخصائص الكيميائية لذلك العنصر. يرجع أصل الكلمة الإنجليزية (بالإنجليزية: Atom) إلى الكلمة الإغريقية أتوموس، وتعني غير القابل للانقسام؛ إذ كان يعتقد أنه ليس ثمة ما هو أصغر من الذرة. تتكون الذرة من سحابة من الشحنات السالبة (الإلكترونات) تحوم حول نواة موجبة الشحنة صغيرة جدا في الوسط. تتكون النواة الموجبة هذه من بروتونات موجبة الشحنة، ونيوترونات متعادلة. الذرة هي أصغر جزء من العنصر يمكن أن يتميز به عن بقية العناصر؛ إذ كلما غصنا أكثر في المادة لنلاقي البنى الأصغر لن يعود هناك فرق بين عنصر وآخر. فمثلاً، لا فرق بين بروتون في ذرة حديد وبروتون آخر في ذرة يورانيوم مثلاً، أو ذرة أي عنصر آخر. الذرة، بما تحمله من خصائص؛ عدد بروتوناتها، كتلتها، توزيعها الإلكتروني...، تصنع الفروقات بين العناصر المختلفة، وبين الصور المختلفة للعنصر نفسه (المسماة بالنظائر)، وحتى بين كون هذا العنصر قادراً على خوض تفاعل كيميائي ما أم لا.
ظل تركيب الذرة وما يجري في هذا العالم البالغ الصغر، ظل وما زال يشغل العلماء ويدفعهم إلى اكتشاف المزيد. ومن هنا أخذت تظهر فروع جديدة في العلم حاملة معها مبادئها ونظرياتها الخاصة بها، بدءاً بمبدأ عدم التأكد (اللاثقة)، مروراً بنظريات التوحيد الكبرى، وانتهاءً بنظرية الأوتار الفائقة.
نجلة محمد قستي#
الكيمياء ” النظريات القديمة للمادة – أفكار الفلاسفة الإغريقا
- افكار الفلاسفة الإغريق حول المادة :
* ديمقريطس Democritus ( ٣٧٠-٤٦٠ ) ق.م :
- تتكون المادة من ذرات تتحرك في الفراغ .
- الذرات الصلبة ، متجانسة ، لاتتحطم ولاتتجزأ .
- الأنواع المختلفة من الذرات لها أحجام وأشكال مختلفة .
- حجم الذرات وشكلها وحركتها يحدد خواص المادة .
* أرسطو Aristotl ( ٣٢٢-٣٤٨ ) ق.م :
- لا وجود للفراغ .
- الماده مكونة من التراب ، والنار ، والهواء ، والماء .
* جون دالتون John Dalton ( ١٧٦٦-١٨٤٤ ) م :
- الذرات لاتتجزأ ولاتتكسر.
- تختلف ذرات أي عنصر عن ذرات العناصر الأخرى .
- في التفاعلات الكميائية : تنفصل الذرات ، أو تتحد ، أو يعاد ترتيبها .
نجلة محمد قستي
المخاليط والمركبات
ما هي المخاليط ؟
المخاليط هي : مزيج مكون من مادتين نقيتين او اكثر مع
احتفاظ كل من هذي المواد بخواصها الاصليه.
وتنقسم المخاليط الى قسمين هما :-
1-المخلوط الغير متجانس . مثال:-
سلطة الخضار والماء مع التراب و الملح مع السكر
ويمكن فصلها بطرقه سهله.
2-المخاليط المتجانسه . مثال:-
الشاهي و السكر في الماء و ملح الطعام في الماء
----------------------------------------------
باختصار
المخاليط الغير متجانسه:-
لا تذوب في المحلول بل تضهر على شكلها الاصلي ولا تفقد خواصها
المخاليط المتجانسه
تذوب وتختفي في الملحول لكنها لا تفقد خواصها بل تحتفظ بها
---------------------------------------------
فصل المخاليط ؟
هل يمكن فصل المخاليط ؟
نعم يمكن وبعدة طرق وهي
1-الترشيح
2-التقطير
3-التبلور
4-التسامي
5-الكروماتوجرافيا
سنشرحها في موضوع مستقل ^^
انتهينا من المخاليط .
نبدأ في المركبات
ما هي المركبات ؟
المركب هو عباره عن عنصرين او اكثر متحدين معا اتحادا كيميائياً
من خواص المركبات
1- تختلف خواص العنصر عند اتحاده مع عنصر اخر مثال:-
ملح الطعام بكون من كلوريد وهي ماده سامه + الصوديوم وهي ايضا ماده سامه
وكونت ملح الطعام ماده نقيه ليست سامه مثل عناصرها
2-يصعب فصل العناصر المركبه الا بالطرق كيميائيه صعبه سنشرحها في موضوع مستقل
للطالبة : نجلة محمد قستي
تغيرات المادة
المادة هي : كل شيء يشغل حيزاً من الفراغ وله ثقل .
المادة عرضة للتغير نتيجة تعرضها لظروف معينة كالحرارة والضغط أو تفاعلها مع مواد أخرى وهناك نوعين من التغيرات التي يمكن أن تطرأ على المادة في حالاتها وأشكالها المختلفة :
التغير الكيميائي : هو أي تغير يحدث على مادة أو مجموعة مواد مؤدياً إلى تغييرها وإنتاج مادة أو مواد من نوع جديد (تغيرات تطرأ على المادة فتنتج مواد جديدة مختلفة في خواصها عن المادة الأصلية.
مثل: احتراق الفحم، فساد الحليب، تحلل الماء كهربياً ).
التغير الفيزيائي : هي تغيرات تحدث في حالة المادة من حيث الشكل والمظهر الخارجي مرتبط بتغير درجة الحرارة أي هو تغير في نوع المادة فقط دون حدوث أي تغير في خواصها الأخرى ( تغيرات تطرأ على المادة وتظل المادة محتفظة بهويتها مثل: كسر الزجاج، تبخر الماء، ذوبان السكر في الماء).
أشكال المادة
العنصر
مادة أولية لا يمكن تحليلها إلى مواد أبسط منها لا بالطرق الفيزيائية ولا بالطرق الكيميائية .
مثل الأكسجين ، الكربون ، الحديد
المركب
مادة ناتجة من اتحاد عنصرين أو أكثر اتحاداً كيميائياً .
مثل الماء ، الملح ، السكر .
المخلوط
مادتين أو أكثر مجتمعة مع بعضها دون اتحاد كيميائي .
مثل الهواء ، الأكسجين في الماء ، ملح وسكر .
طرق فصل المواد
يمكن فصل المواد المختلطة أو المتحدة مع بعضها البعض بطرق مختلفة، ويمكن تصنيف هذه الطرق بشكل عام تحت طريقتين رئيستين:
طرق فصل فيزيائية
وهي طرق يتم من خلالها فصل المواد عن بعضها البعض دون التأثير في تركيب المادة.
مثل: عملية التسخين، عملية الترشيح ،استخدام المغناطيس
طرق فصل كيميائية
وهي طرق يتم من خلالها فصل المواد عن بعضها البعض عن طريق التأثير في تركيب المادة.
مثل: عملية التسخين، عملية التحليل الكهربي.
بعض التغيرات نافع وبعضها ضار
التغيرات النافعة
تحولات المـــاء – ذوبان السكـر – ذوبان المــلح
احتراق الفحـــم – احتراق الغــــذاء
التغيرات الضارة
تسوس الأسنان – صدأ الحديد – حرائق الغابات
احتراق السكــر– عفن المواد الغذائية
تحولات المـــاء
الماء مركب كيميائي مكون من ذرتي هيدروجين وذرة من الاكسجين. ينتشر الماء على الأرض بأشكاله المختلفة، السائل و الصلب و الغازي .
يستطيع الماء التحول الى ثلاث حالات في الطبيعة هي الصلبة والسائلة والغازية:
الحالة الصلبة: يكون فيها الماء على شكل جليد أو ثلج أبيض اللون ناصع ، يوجد على هذه الحالة عندما تكون درجة حرارة الماء أقل من الصفر المئوي.
الحالة السائلة: يكون فيها الماء سائلا شفافا، وهي الحالة الأكثر شيوعا للماء. ويوجد الماء على صورته السائلة في درجات الحرارة ما بين الصفر المئوي، ودرجة الغليان، وهي 100 درجة مئوية.
وتوجد عدة طرق لتحويل الماء الى الحالة الغازية منها :
الغليان
يتبخر الماء عند غليه بدرجة 100 مئوية
التبخر
عملية تبخر الماء لاتحتاج لدرجات حرارة عالية بل يمكن أن يتبخر الماء عند 30درجة مئوية وتزداد سرعة التبخر بزيادة درجة الحرارة وهذا ما يفسر جفاف الملابس وتبخر مياه البحر الذي يكون السحب حيث ان مياه البحار لا تغلى لكنها تتبخر وتنتج بخار الماء بالاضافة الحالات الثلاثة توجد حالتان هما التكاثف والتسامي
التكاثف
هو تحول الماء من الحالة الغازية إلى الحالة السائلة نتيجة تبريد بخار الماء وأوضح مثال هو السحب والضباب بالاضافة الى قطرات الندى الذي تتكون على على السيارات صباحا وعلى نظارة الشخص عند خروجه من مكان حار إلى بارد والعكس
التسامي
هو تحول الماء من الحالة الصلبة الى الحالةالغازية
مثال ذلك هو تبخر الثلج الموجود على الشوارع في الدول ذات الطقس البارد والجاف جدا
الحالة الغازية : هي الحالة التي يتحول فيها الماء من سائل الى غاز ويكون فيها الماء على شكل بخار، ويكون الماء بالحالة الغازية بدرجات حرارة مختلفة.
لماذا لا تتجمد المحيطات في فصل الشتاء حتى القاع؟
لماذا يكون التجمد على السطح فحسب؟
في الجواب حكمة ربانية وهي ان الماء عندما تنخفض حرارته وتبلغ 4 درجات مئوية فإن سطحه يتجمد ويزداد حجمه ،على العكس من كل السوائل والجوامد الاخرى، وبالتالي ينخفض وزنه ويطفو على السطح ويصبح بينه وبين الماء عازل هو الهواء وهذا ما يحافظ على حياة الكائنات البحرية ويحميها من التجمد
التغيرات الحيو كيميائية
تعريفها:
هي تغير في مظهر المادة وتركيبها الداخلي وحدوث تغير كيميائي ينتج عنه مواد جديدة بفعل خمائر تفرزها الكائنات الحية داخل الجسم أو خارجه.
بعض الأمثلة على التغيرات الحيو كيميائية :
مثل :( التنفس ـ الهضم ـ البناء الضوئي ـ تعفن الخبز والفاكهة ـ فساد الأطعمة ـ تحمض الحليب ) .
سبب حدوث فساد الطعام:
يفسد الطعام بسبب :وجودة في مناطق حارة ورطبة .
بعض طرق حفظ الطعام :
من طرق حفظ الأطعمة :( التجفيف ــ البرودة الشديدة ــ إضافة كميات من الملح- الغليان والتبخر - التعليب )
كيفية نتخلص من البكتيريا والفطريات :
يتم التخلص من البكتيريا والفطريات عن طريق : الغليان والتبخر ــ التعليب في جو معقم ــ تخفيض درجة الحرارة
تخثر الدم : هو تحول الدم من الحالة السائلة إلى الحالة الصلبة .
كيفية تخثر الدم
تحتوي بلازما الدم على البروتين الشفاف ذائب في ماء البلازما ويتحول هذا البروتين بفعل خمائر ( إنزيمات) إلى بروتين آخر صلب .
فوائد تخثر الدم:
1-وقف نزف الدم 2 -منع تسرب الجراثيم إلى داخل الجسم .
سبب حدوث التغيرات الحيوكيميائية :
1-وجود كائنات حية دقيقة منتشرة حولنا مثل البكتيريا والفطريات .
2-وجود درجة حرارة مناسبة ورطوبة عالية .
كيفية حدوث التغيرات الحيوكيميائية :
تفرز هذه الكائنات الدقيقة أنواعاً مختلفة من الخمائر التي تساعد على تحلل المواد النباتية والحيوانية وتغير تركيبها الكيميائي .
بعض فوائد حدوث التغيرات الحيو كيميائية:
1.يستفاد منها في صناعة الأغذية
2.توجد أنواع من البكتيريا المفيدة في الجسم والتي تساعد في عملية الهضم
3.توجد أنواع مفيدة البكتيريا في التربة تزيد من خصوبتها
4.توجد أنواع من البكتيريا تساعد في تكوين النفط
5.صناعة الأدوية: فقد استطاع العالم الانجليزي الكسندر فلمنج استخلاص دواء البنسلين من أحد أنواع الفطريات.
مميزات التغيرات الحيو كيميائية .
1-تتحكم بهذه التغيرات خمائر تفرزها الكائنات الحية .
2-هذه التغيرات أكثر تعقيداً من التغيرات الكيميائية .
3-لا تحصل بالسرعة نفسها التي تحصل فيها التغيرات الكيميائية فهي بطيئة نسبياً
للطالبة : نجلة محمد قستي
خواص المادة
خواص المادة هي سمات مميزة لكل مادة، وتعرف بأنها غير مقدارية (لا تختلف باختلاف مقدار المادة) ويمكن غالبا وصفها كميا، وذلك من خلال وحدات للقياس تمكننا من المقارنة بين المواد وترتيبها حسب كل خاصية مما يساعد في اختيار المادة حسب المواصفات المطلوبة.فمثلا الكثافة ووحدتها كيلوجرام/مترمكعب هي خاصية غير مقدارية للمادة حيث أنها ثابتة أينما أخذنا العينة من المادة الموجودة . وكذلك حرارة نوعية ووحدتها جول/مول أيضا خاصية غير مقدارية حيث أنها تنطبق على أي مول من المادة . تسمى تلك الخاصيتان وأشباههما في الترموديناميكا "خاصية مكثفة".
وقد تكون خواص المادة رقما ثابتا وقد تتغير حسب متغير (مثل الحرارة) أو أكثر من متغير. وقد تتغير قيمة خواص المادة تبعا لاتجاه القياس وهو ما يعرف بـ تباينية الخواص. مثال على ذلك أن مغناطيسية بلورة في اتجاه المحور السيني قد تختلف عن مغناطيسيتها في اتجاه المحور الصادي.
وبالنسبة للخواص التي تربط بين ظاهرتين طبيعيتين فهي تتغير بشكل خطي أو شبه
خطي خلال نطاق معين، فهي تعتبر قيمة ثابتة خلال هذا النطاق.
تقسم الى:
الطالبة : نجلة محمد قستي
خواص العناصر
1-الفلزات (المعادن)Metals :
أ- خواصها الفيزيائية(الطبيعية) : - اللمعان والبريق. - موصلة جيدة للحرارة والكهرباء. - كثافتها عالية. - درجة انصهارها عالية. - يمكن سحبها لأسلاك. - يمكن طرقها لألواح. - جميعها صلبة ما عدا الزئبق سائل
ب- خواصها الكيميائية : - تفقد ألكترونات بسهولة. - تتآكل بسرعة. فالحديد يصدأ والفضة تطوس.
2-اللافلزات (اللامعادن) Nonmetals :
أ- خواصها الفيزيائية(الطبيعية) : صفاتها عكس المعادن - لا تلمع وبدون بريق. - رديئة التوصيل للحرارة ووالكهرباء، - هشه تتهشم بسهولة. - لا تسحب لسلاك. - لا تطرق لألواح. - كثافتها قليلة. - درجة الانصهار منخفضة.
ب- الخواص الكيماوية : - تميل لاكتساب إلكترونات وحيث أن المعادن تميل لفقدان الكترونات واللامعادن تميل لاكتساب الكترونات. لهذا المعادن واللا معادن يميلان لتكوين مركبات منهما. وهذه المركبات يطلق عليها مركبات أيونية (متاينة) ionic compounds. وعندما يتحد اثنان أو أكثر من اللامعادن تكون مركبات متحدة الذرات a covalent compound.
3-أشباه الفلزات (المعادن) Metalloids : لها خواص المعادن واللامعادن
أ- خواصها الفيزيائية (الطبيعية): - صلبة - لامعة أو غير لامعة. - يمكن سحبها لأسلاك. - يمكن طرقها لألواح.
- توصل الحرارة والكهرباء لكن ليس بكفاءة المعادن.
سلمى المسدي
استعمالات الجدول
يعتبر الجدول الدوري للعناصر له أهميته للعلماء وطلاب الكيمياء لدراسة العناصر والخواص الكيميائية والفيزيائية، وكيفية اختلافها بكل مجموعة به. فمن خلال الجدول يمكن الحدس بخواص عنصر ما، وكيفية التفاعل مع عنصر آخر. فلو أراد دارس معرفة خواص عنصر كالفرانشيوم francium مثلا، فيمكنه التعرف عليه من خلال خواص المجموعة 1. فسيعرف أنه معدن لين يتفاعل بشدة مع الماء أكثر من العنصر الذي فوقه. ولو أراد معرفة مركبات التلليريم tellurium مع الهيدروجين hydrogen.فان العنصرين سيكونان مركب H2Te لأن بقية العناصر في مجموعة التلليريم تكون مركبات مع الهيدروجين كالماء H2Oوكبريتيد الهيدروجين H2S و H2Se.وأخيرا كان تنظيم جدول مندليف يعتمد علي الوزن الذري في الترتيب التصاعدي والجدول الدوري الحديث يعتمد علي العدد الذري التصاعدي ولكل عنصر عدده الذري ولا يتكرر مع عنصر آخر. لأن العدد الذري هو عدد البروتونات في نواته. وأصبح لكل عنصر رمزه الكيماوي. فالكربون رمزه C والأكسجين رمزه O والكبريت رمزه s والهيدروجين رمزه H والكربون نجد ان عدده الذري 6ووزنه الذري حوالي 12.
سلمى المسدي
النظرية الذريه
حتي نهاية القرن 19 كانت الذرة تعتبر ككرة صلبة صغيرة. عندما اكتشف طومسون الإلكترون عام 1897.فلقد كان العلماء بعرفون أن التيار الكهربائي لو مر في أنبوبة مفرغة، فيمكن رؤية تيارا على هيئة مادة متوهجة. ولم يكن يعرف لها تفسيرا. فلاحظ طومسون أن التبار المتوهج الغامض يتجه للوح الكهربائي الموجب.فوجد أن التيار المتوهج مكون من جسيمات صغيرة وأجزاء من الذرات تحمل شحنات سالبة سميت بالإلكترونات. وقال ايوجين جولدشتين عام 1886 أن الذرات بها شحنات موجبة. وفي سنة 1911 كانت النظرية الذرية لرذرفورد، عندما قال أن الذرة تتكون من قلب مكثف له شحنة موجبة من البروتونات protons حوله طوق من الإلكترونات السالبة تدور حول النواة.وفي سنة 1932اكتشف جيمس كادويك نوعا ثالثا من جسيمات الذرة أطلق عليه نيترونات. Neutrons. وأن النترونات تقلل تنافر البروتوناتى النتشابعى الشحتة الكهربائيى بالنواة المتماسكة. والنترونات حجمها نفي حجم البروتونات بالنواة. ولاتحمل شحنات كهربائية لأنها. متعادلة الشحنات.والذرة متعادلة الشحنة لأن عدد البروتونات الموجبة يعادل عدد الإلكترونات السالبة داخلها. وأصغر ذرة ذرة الهيدروجين. ومعظم الفراغ بالذرة فارغ. لأن الإلكترونات تدور في مدارات بعيدة نسبيا من النواة. وكل عنصر من العناصر المختلفة تتميز عن غبرها من العناصر بعدد ثابت من البروتونات. ولكل ذرة عتصر ما، وزنها الذري الذي يعين حسب عدد البروتونات والنترونات بنواتها. ويجب أن نعرف أن حجم الذرة ضئيل جدا. فذرة الهيدروجين قطرها (5 x 10–8 mm). فلو وضعنا 20 مليون ذرة هيدروجين فتشكل خطا طوله واحد ملليمتر. وذرة الهيدروجين تتكون من بروتون واحد والكترون واحد. وذرة الهيليوم بها 2 بروتون يدور حولها 2الكترون. وبصفة عامة نجد أن كل ذرة لها قلب يسمي النواة a nucleus التي تشكل كتلة الذرة تقريبا، إلا أنها تشغل حيزا صغيرا من حجم الذرة نفسها.لأن معظم الذرة فراغ حول النواة. وبالنواة يوجد جسيمات أصغر هي البروتونات protonsموجبة الشحنات والنترونات neutrons متعادلة الشحنات. ويدور بالفراغ حول النواة جسيمات خفبفة جدا تسمي الإلكترونات electrons.وكل عنصر بذرته عدد ثابت ومتشابه من البروتونات بالنواة. فعنصر الأكسجين بنواته 8 بروتونات. والنترونات لاتجمل شحنات كهروبائية. وليس بالضرورة ذرة كل عنصر تجمل عددا ثابتا من البروتونات. فلو ذرات عنصر ما تحمل عددا مختلفا من النيترونات يطلق عليها نظائر مشعة isotopes من العنصر الواحد. والإلكترونات جسبمات سلبية الكهربائية ندور في الفراغ حول النواة. وكتلة الإلكترون تعادل 1/2000 كتلة البروتون أو النيترون.كتلة نيترون واحد تعادل كتلة بروتون ونيترون معا, والتفاعل أو الإتحاد بين ذرات العناصر تتم بين ترابط الإلكترونات لتكوين الجزيئات أو المركبات الكيماوية. لهذا نجد العدد الذري لكل ذرة يدل علي عدد البروتونات بنواة ذرة العنصر.فالأكسجين عدده الذري 8. وهذا معناه أن ذرة الأكسجين تتكون من 8 بروتونات والرقم الذري للنحاس 29 وهذا معناه أن ذرة عنصر النحاس نواتها بها29 بروتون. وكتلة الذرة نجدها مجموع عدد البروتونات والنترونات بالنواة. لأن 99،99% من كتلة الذرة في النواة. فأمكن التعرف من خلال التعرف علي مكنونات الذرة علي تفسيرات للنماذج المتكررة بالجدول الدوري. فوجد العلماء أن العناصر في مجموعة واحدة من الجدول تمتلك نفس العدد من الإلكترونات الخارجية بمدارات الذرة.وكانت الجسيمات لم تكن قد اكتشفت عندما وضع العلماء الجداول الدورية الأولي. وحدسثنا السابق كان حول الذرة المتعادلة الشحنات كهربائيا.لكن في الحقيقة الذرات يمكنها فقدان أو اكتساب الكتلاونات سالبة. لكن عدد البروتونات لاتتغير بالنواة. فلو اكتسبت الذرة الكترونات تصبح الذرة سالبة الشحنة لأن عدد الإلكتلاونات تزيد علي عدد البروتونات بالنواة..ولو فقدت الذرة الكترونات تصبح الذرة موجبة الشحنة لأن عدد البروتوناتبالنواة يزيد علي عدد الإلكترونات. وكل ذرة لها شجنة تسمي ايون an ion فالهيدروجين الموجب الشجنة يسمي ايون الهيدروجين الموجب وتوضع فوق رمزه علامة (+) ويكتب هكذا H+ ولو كان أيون ذرة الهيدروجين سالب الشحنة يكتب هكذا(H-) ولو كانت الذرة متعادلة تكتب بدون علامة(+ أو -) وتكتب الذرة هكذا(H).وفي الحالات الثلاثة للذرة نجد أن العدد الذري والوزن الذري ثابت. وفي النظائر isotopes للعنصر نجد أن عدد النيترونات تتغير حسب نظير العنصر. لهذا نجد أن نظير العنصر يتغير في الوزن الذري الذي هو مجموع عدد البروتونات والنترونات، وليس في العدد الذري الذي هو عدد البروتونا ت. فالنظير لعنصر نجده ثابت في العدد الذري ومختلف في الوزن الذري.فالهيدروجين عدده الذري 1 ووزنه الذري 1 والديتريم Deuterium نظير الهيدروجين نجد عدده الذري 1 ووزنه الذري 2
سلمى المسدي
: تاريخ الجدول الدوري
كان أرسطو عام 330 قبل الميلاد يعتبر العناصر أربعة عناصر.هي الأرض والهواء والنار والماء. وفي عام 1770صنف لافوازييه 33 عنصر.وفرق بين الفلزات (المعادن) واللافلزات. وفي عام 1828 صنع جدولا للعناصر وأوزانها الذرية ووضع للعناصر رموزها الكيماوية. وفي عام 1829 وضع دوبرينر ثلاثة جداول بها ثلاثة مجموعات كل مجموعة تضم 3 عناصر متشابهة الخواص. المجموعة الأولي تضم الليثيوم والصوديوم والبوتاسيوم والثانية تضم الكالسيوم والإسترونشيوم والباريوم. والثالثة تضم الكلورين والبرومين واليود. وفي عام 1864 رتب جون نيولاندز John Newlands 60 عنصرا حسب الأوزان الذرية ووجد تشابها ما بين العنصر الأول والعنصر التاسع والعنصر الثاني والعنصر العاشر إلي آخره من الترتيب. فاقترح قانون اوكتاف the 'Law of Octaves'.وكان ديمتري مندليف Dmitri Mendeleev - عالم كيميائي روسي ولد بمدينة توبوليسك بسيبيريا عام 1834 - عرف بانه أبو الجدول الدوري للعناصر the periodic table of the elements.وهذا الجدول له أهميته لدراسة الكيمياء وفهم وتبسيط التفاعلات الكيميائية حتي المعقدة منها. ولم يكن مندليف قد رتب الجدول الدوري للعناصر فقط، بل كتب مجلدين بعنوان مبادئ الكيمياء Principles of Chemistry. مات 20 يناير 1907.
تم اقتراح الجدول الدوري الأصلي بدون معرفة التركيب الداخلي للذرات، فلو تم ترتيب العناصر طبقا للكتلة الذرية، ثم تم وضع الخواص الأخرى فيمكن ملاحظة التكرارية التي تحدث للخواص عند تمثيلها مقابل الكتلة الذرية. أول من أدرك تلك التكرارية هو الكيميائي الألماني جوهان فولف جانج دوبرينير والذي لاحظ عام 1829 وجود ثلاثيات من العناصر تتقارب في صفاتها.
سلمى المسدي
جدول دوري
الجدول الدوري للعناصر الكيميائية, والذي يعرف أيضا بـ (جدول مندليف، الجدول الدوري للعناصر، أو فقط الجدول الدوري) وهو عرض جدولي للعناصر الكيميائية المعروفة. على الرغم من وجود جداول سبقت جدول مندلييف إلا أن بناء هذا الجدول يعزى بشكل عام إلى الكيميائي الروسي ديمتري مندليف, حيث قام في عام 1869 بترتيب العناصر بالاعتماد على السلوك (الدوري) للخصائص الكيميائية للعناصر، ثم قام هنري موزلي عام 1911 بإعادة ترتيب العناصر بحسب العدد الذري، أي عدد البروتونات الموجودة بكل عنصر. ومع مرور الوقت تم تعديل مخطط الجدول مرات عديدة، حيث أضيفت عناصر جديدة مكتشفة، كما أضيفت نماذج نظرية طورت لتفسير سلوك العناصر الكيميائية.
أصبح الجدول الدوري في عصرنا هذا معتمداً في جميع المناحي الأكاديمية الكيميائية، موفراً إطاراً مفيداً جداً لتصنيف وتنظيم ومقارنة جميع الأشكال المختلفة للخصائص الكيميائية. وللجدول الدوري تطبيقات متعددة وواسعة في الكيمياءوالفيزياء وعلم الأحياء والهندسة خاصة الهندسة الكيميائية.
يحتوي الجدول الدوري الحالي على 118 عنصراً (العناصر 1 - 118)، مع ضرورة الإشارة إلى أن العناصر 113 و115 و117 و118 لا تزال بحاجة إلى تأكيد من الوسط العلمي. أغلب العناصر من 1 إلى 98 متوفرة في الطبيعة بشكل أو بآخر، في حين أن العناصر من 99 إلى 118 مصطنعة فقط في المختبر.
سلمى المسدي
الانوية غير المستقرة والتحلل الاشعاعي
قياس العمر إشعاعياً هو طريقة لتقدير عمر المواد و(منها المستحاثات أيضا) وتسمى بالإنكليزية ب Radiometric dating وتعني تحديد العمر بالطريقة الراديومترية (الاشعاعية), هذه الطريقة تعتمد على النشاط الاشعاعي للنظائر الطبيعية. هنالك طرق عديدة مختلفة للقيام بذلك وكل طريقة تستعمل نظام نظائري مختلف عن الأخرى وكل طريقة تختلف عن الأخرى في مستوى الدقة واتكاليف والمدة الزمنية التي يجب أن نرجع إلى الوراء لمعرفة عمر المادة.
محتويات
النظرية التي تستند عليها[عدل]النظائر[عدل]ذرات العنصر الكيمياوي يحتوي في نواتها على بروتونات، عدد هذه البروتونات يسمى بالعدد الذري، وتحتوي نواة الذرة أيضا على النيوترونات التي تحدد الكتلة الذرية للعنصر وأعدادها تختلف من ذرة لأخرى لنفس العنصر الكيمياويوتسمى هذه الذرات بالنظائر الكيمياوية لنفس العنصر وأصل كلمة نظير يعني نفس المكان كناية إلى أن النظائر المختلفة لعنصر معين تشغل نفس المكان في الجدول الدوري.
أي أن عدد البروتونات متساوية للنظائر المختلفة لعنصر معين وتختلف العناصر فقط في عدد النيوترونات.
النشاط الاشعاعي[عدل]كل نظير من نظائر العنصر الواحد لديه كتلة واستقرارية مختلفتين. بعض النظائر غير مستقرة أي انها في حالة مضطربه وفي اية لحظة يمكن أن تتحلل عن طريق السقوط الاشعاعي (تحرير الاشعاع). والنشاط الاشعاعي للعناصر تكون غالبا متكونا من دقائق ألفا (2 بروتون مع 2 نيوترون معاً) وكذلك من دقائق بيتا. تتكون المادة من عدد هائل جدا من الذرات وهناك اعداد معينة من أنوية الذرات تتحلل اشعاعيا وتوقيت حصول ذلك يمكن أن يحدث في اية لحظة. الذرات النشطة الموجودة في المادة تكون بعد مرور زمن معين قد اصابها التحلل الاشعاعي. وهذا يعتمد على مدى قلقية (عدم استقرارية) تلك الذرات. وهذه الاستقرارية يمكن تعريفها وقياسها تحت مفهوم [نصف العمر] لنظائر العناصر. ونصف العمر هو الوقت اللازم لكي يتحلل نصف المادة اشعاعيا. وكل نظير من نظائر العناصر المختلفة له نصف العمر ثابت طبيعي معروف. معظم النظائر المشعة يتحلل في عدة خطوات (سلسلة متتابعة من التحلل) إلى عناصر مستقرة تسمى بعنصر البنت بينما النظائر الأصلية قبل التحلل تسمى بعناصر الأم. أي نظير يُستخدم في تحديد العمر الاشعاعي يجب أن يتراوح نصف العمر له من بضعة آلاف سنة إلى بضعة مليارات من السنين.
النظائر عبارة عن ساعات دقيقة[عدل]في أغلب الحالات يكون نصف العمر للنظائر معتمدا على خصائص الذرات المكونة لها والعوامل الخارجية لا تؤثر عليها مثل درجة الحرارة والضغط والوسط الكيمياوي المتواجد فيه والحقول المغناطيسية والكهربية. بالإضافة إلى ذلك فاننصف العمر للنظائر لا يتغير حسب الوقت بل هو قيمة ثابتة طبيعيا. لكن النشاط الاشعاعي الذري يمكن أن يؤثر على نصف العمر للنظائر لكن لحسن الحظ لو حصل ذلك لعرفنا ذلك بسهولة لأن ذلك يترك وراءه أثر الاشعاع. لذلك الزمن اللازم لتحول عنصر الأم إلى عنصر البنت يمكن اعتباره ساعة ذرية دقيقة. وهو الزمن العابر عندما تشكل عنصر الأم في المادة المعينة إلى وقتنا الحالي.
وجود النظائر في المواد[عدل]عندما تتون مادة معينة فانها تتشكل فقط من عناصر الأم فليس فيها عناصر البنت. وعندما نفحص المواد لمعرفة عمرها نرى فيها عناصر بنت وأم، فعناصر البنت قد تشكلت من عناصر الام بعد حصول التحلل الاشعاعي كما وضحت أعلاه. عندما تتشكل مادة ما فأنها تمنع عناصر البنت من التسرب إليها نتيجة حصول تسخن كبير جدا لها وعناصر البنت التي تتشكل على مر الزمن سوف تتلاشى بواسطة الانتشار بسبب فرق التركيز Diffusion عندها تكون الساعة النووية قد تم تصفيرها. ودرجة الحرارة التي عندها تحصل هذه العملية تسمى بدرجة الحرارة الكابحة. ودرجة الحرارة هذه تختلف باختلاف المادة.
معادلة حساب العمر[عدل]عندما تتحلل عناصر الأم غير المستقرة إلى عناصر البنت المستقرة فأن معادلة حساب العمر يربط التحلل الاشعاعي بالزمن الجيولوجي:
وفيها
t= عمر المادة
D= تركيز نظائر البنت
P= تركيز نظائر الأم
λ = ثابت التحلل لنظير الأم
ln= اللوغاريثم الطبيعي
ثابت التحلل λ هو ذلك الجزء من ذرات عنصر الأم التي تتحلل في وحدة الزمن ويتناسب عكسيا مع عمر النصف
وفيها
عمر النصف لعنصر الأم.
التقنية[عدل]شروط ينبغي توفرها للحصول على تحديد عمر جيد[عدل]ليس في كل الحالات تستطيع المادة عند تكوينها أن تأخذ عناصر الأم لوحدها فعادة تأخذ أيضا بعض عناصر البنت وفي هذه الحالة يجب علينا أن نفرض مسبقا قيمة نسبة تركيز عناصر البنت إلى تركيز عناصر الأم عندما تكوّنت المادة. يجب أن تكون عناصر البنت غير غازية لأنها تتسرب من المادة بسهولة, وعناصر البنت يجب أن تكون مستقرة بشكل يكفي لنا أن نقيس تراكيز عالية منها في المادة. بالإضافة إلى ذلك يجب على عناصر البنت والأم أن لا تكوّنا مواد فعّآلة كيماوية والتي تتفاعل بشكل نشط جدا داخل المادة. وكذلك يجب أن لا تحتوي المادة على كمية كبيرة من عناصر بنت أخرى نشأت من التحلل الاشعاعي لعناصر أم أخرى. وأخيرا يجب أن تكون طريقة عزل وفحص وتحليل التراكيز واضحة وموثوقة بها. عند استعمال طريقة التماثل الزمني Isochron (وهي من أبسط الطرق لتحديد العمر اشعاعيا) فاننا لسنا بحاجة إلى معرفة نسبة تركيز عناصر البنت إلى تركيز عناصر الأم عنما تكوّنت المادة المراد قياس عمرها الآن.
جهاز قياس الطيف الكتلي[عدل]مطيافية الكتلة (بالإنجليزية: Mass spectrometry) هذا الجهاز يستعمل في تحديد شكل ونوعية وماهية النظائر والجزيئات وخلائط الكيمياوية والبيولوجية والتي تكون بمقادير صغيرة جدا قد تصل إلى جزء واحد من المليار للغرام الواحد.
الجهاز الذي يستعمل هذه الطريقة تم اختراعه في أربعينيات القرن الماضي، ومنذ خمسينيات القرن الماضي يُستعمل هذا الجهاز لتحديد عمر المواد اشعاعيا. يقوم هذا الجهاز بواسطة السخونة الشديدة بشحن مجموعة من الذرات بالأيونات ويتم استخلاص هذه الذرات المتأينة من النموذج ويتم فصل الكتلة والشحنة الكهربائية عن بعضها، عندها يتم قياس الأيونات بواسطة مجسات خاصة تسمى بكؤوس الفاراداي (بالإنجليزية: Faraday cup)، عندما تتعرض هذه الكؤوس للأيونات هذه فان ذلك يؤدي إلى توليد كهربائية ضعيفة ويتم قياس هذه الكهربائية بدقة وعندها وبواسطة هذه القيم المقاسة يتم معرفة كمية تراكيز العناصر أو النظائر المختلفة (عناصر الأم والبنت).
نسبة الخطأ أو الدقة في تحديد العمر اشعاعيا[عدل]على الرغم من أن طريقة تحديد العمر اشعاعيا هي طريقة دقيقة إلا أن هذه الدقة تعتمد أساساً على التكنولوجيا والطريقة المستعملة في القياس.
من الممكن ان تؤثر النقاط أدناه على دقة النتائج المحصلة:
يمكن أن نرفع دقة قياس العمر بالاشعاع عن طريق أخذ عينات من أماكن مختلفة من النموذج المراد تقدير قِدَمه (عُمْره) لأنه إذا فرضنا أن جميع أجزاء العينة له نفس العمر فيجب منطقيا تعطي كافة القياسات نفس الزمن (العمر) isochron. يمكن مقارنة نتائج فحص نظامين نظائريين مع بعضهما في حالة تواجدهما معا في نفس العينة وذلك للتأكد من دقة القياسات.
دقة القياسات تعتمد أيضا على عمر النصف لعنصر الأم. فمثلا نظير كاربون المشع 14C لها عمر نصف أقل من 6000 سنة فليس من المعقول أن نستعمل 14C في تحديد عمر شيء يرجع قِدمه إلى 600 ألف سنة مثلا. لذلك في هذه الحالة يجب استمال أنظمة نظائرية أخرى. أن استعمال نظائر الكربون لتحديد أعمار أشياء ترجع إلى فترة من 1000 سنة إلى 50 ألف سنة قبل الآن يمكن أن يعطي نتائج دقيقة نسبيا.
الطرق المستعملة في تحديد العمر إشعاعياً[عدل]من أقدم الطرق المستعملة هي طريقة يورانيوم - رصاص لتحديد العمر، يُستعمل هذه الطريقة لتحديد عمر معدن الزركون (سليكات الزركونيوم) الذي عند تكوّنه يستبعد أخذ الرصاص بينما يأخذ تراكيز كبيرة من اليورانيوم. استعمال هذه الطريقة الآن يعطي نتائج فيها عدم دقة تصل إلى زائد ناقص 2 مليون سنة لشيء عمره 3 مليارات من السنين، هذه الطريقة تستعمل بكثرة في الداسات والفحوصات الجيولوجية. بما أن 235U تتحلل اشعاعيا إلى 207Pb وفي نفس الوقت238U تتحلل إلى 206Pb فأن هذه الطريقة لها ميزة جيدة جدا باننا نحصل على نتيجتين يمكننا مقارنتهما مع بعض لمعرفة مدى دقة القياسات المأخوذة.
طريقة بوتاسيم - أرغون لتحديد العمر تستعمل طريقة تحلّل 40K إلى 40Ar. فنظير بوتاسيم المشع أربعين 40K له عمر نصف كبير جدا وتتواجد بكثرة في المايكات Mica وفيلدسبارات Feldspar وفي هورنبليندات Hornblende لكن من أهم مساويء هذه الطريقة هي أن ل 40K درجة حرارة كابحة منخفضة جداً.
طريقة روبيديوم - سترونتيوم لتحديد العمر اشعاعيا تستعمل تحلّل 87Rb إلى 87Sr الذي له عمر نصف كبير جدا ودرجة حرارة الكابحة لهذه الطريقة هي كبيرة نسبياً، لكن لأنّ عمر النصف له كبير جدا فأن القياسات تكون غير دقيقة.
طريقة تحديد العمر بواسطة الكربون اشعاعيا تستعمل تحلل 14C اشعاعيا الذي له نصف عمر قليل نسبيا لذلك نرى بأن هذه الطريقة من أشهر الطرق في تحديد عمر المواد في علم الآثار Archaeology.
طريقة أخرى لها أيضا عمر نصف قليل نسبيا هي طريقة يورانيوم - ثوريوم لتحديد العمر اشعاعيا وفيها تستعمل تحلّل 238U إلى 230Th وكذلك 235U إلى 231Pa (Protactinium).
طرق أخرى لتحديد عمرالمواد اشعاعياً:
تسربت الكثير من 36Cl في طبقة الأتموسفير للكرة الأرضية نتيجة التجارب الأسلحة النووية في خمسينيات القرن المنصرم ولأن 36Cl له عمر نصف قصير جداً فأنها تستعمل لمعرفة المسافات التي تقطعها تكتلات المياه الجوفية لكن هذه الطريقة لا تدخل ضمن مفهوم تحديد العمر اشعاعيا.
تحديد الأعمار في التطبيقات الفلكية بواسطة النظائر المفقودة (المتحلّلة)[عدل]عندما كان كوننا يافعا كان مليئا بنظائر مشعة ذات عمر قصير جدا مثل النظائر 26Al و60Fe و53Mn و129I، هذه النظائر المنقرضة ربما تم إنتاجها خلال عملية الأنفجار العظيم، هذه النظائر المتحللة يمكن لحد الآن قياسها من خلال النيازك التي تسقط على الأرض ومن خلال هذه القياسات يتم معرفة تسلسل الأحداث خلال عملية تكوين المجرات.
المصادر
malaak jabr
محتويات
- 1 النظرية التي تستند عليها
- 2 التقنية
- 3 الطرق المستعملة في تحديد العمر إشعاعياً
- 4 تحديد الأعمار في التطبيقات الفلكية بواسطة النظائر المفقودة (المتحلّلة)
- 5 المصادر
- 6 اقرأ أيضا
النظرية التي تستند عليها[عدل]النظائر[عدل]ذرات العنصر الكيمياوي يحتوي في نواتها على بروتونات، عدد هذه البروتونات يسمى بالعدد الذري، وتحتوي نواة الذرة أيضا على النيوترونات التي تحدد الكتلة الذرية للعنصر وأعدادها تختلف من ذرة لأخرى لنفس العنصر الكيمياويوتسمى هذه الذرات بالنظائر الكيمياوية لنفس العنصر وأصل كلمة نظير يعني نفس المكان كناية إلى أن النظائر المختلفة لعنصر معين تشغل نفس المكان في الجدول الدوري.
أي أن عدد البروتونات متساوية للنظائر المختلفة لعنصر معين وتختلف العناصر فقط في عدد النيوترونات.
النشاط الاشعاعي[عدل]كل نظير من نظائر العنصر الواحد لديه كتلة واستقرارية مختلفتين. بعض النظائر غير مستقرة أي انها في حالة مضطربه وفي اية لحظة يمكن أن تتحلل عن طريق السقوط الاشعاعي (تحرير الاشعاع). والنشاط الاشعاعي للعناصر تكون غالبا متكونا من دقائق ألفا (2 بروتون مع 2 نيوترون معاً) وكذلك من دقائق بيتا. تتكون المادة من عدد هائل جدا من الذرات وهناك اعداد معينة من أنوية الذرات تتحلل اشعاعيا وتوقيت حصول ذلك يمكن أن يحدث في اية لحظة. الذرات النشطة الموجودة في المادة تكون بعد مرور زمن معين قد اصابها التحلل الاشعاعي. وهذا يعتمد على مدى قلقية (عدم استقرارية) تلك الذرات. وهذه الاستقرارية يمكن تعريفها وقياسها تحت مفهوم [نصف العمر] لنظائر العناصر. ونصف العمر هو الوقت اللازم لكي يتحلل نصف المادة اشعاعيا. وكل نظير من نظائر العناصر المختلفة له نصف العمر ثابت طبيعي معروف. معظم النظائر المشعة يتحلل في عدة خطوات (سلسلة متتابعة من التحلل) إلى عناصر مستقرة تسمى بعنصر البنت بينما النظائر الأصلية قبل التحلل تسمى بعناصر الأم. أي نظير يُستخدم في تحديد العمر الاشعاعي يجب أن يتراوح نصف العمر له من بضعة آلاف سنة إلى بضعة مليارات من السنين.
النظائر عبارة عن ساعات دقيقة[عدل]في أغلب الحالات يكون نصف العمر للنظائر معتمدا على خصائص الذرات المكونة لها والعوامل الخارجية لا تؤثر عليها مثل درجة الحرارة والضغط والوسط الكيمياوي المتواجد فيه والحقول المغناطيسية والكهربية. بالإضافة إلى ذلك فاننصف العمر للنظائر لا يتغير حسب الوقت بل هو قيمة ثابتة طبيعيا. لكن النشاط الاشعاعي الذري يمكن أن يؤثر على نصف العمر للنظائر لكن لحسن الحظ لو حصل ذلك لعرفنا ذلك بسهولة لأن ذلك يترك وراءه أثر الاشعاع. لذلك الزمن اللازم لتحول عنصر الأم إلى عنصر البنت يمكن اعتباره ساعة ذرية دقيقة. وهو الزمن العابر عندما تشكل عنصر الأم في المادة المعينة إلى وقتنا الحالي.
وجود النظائر في المواد[عدل]عندما تتون مادة معينة فانها تتشكل فقط من عناصر الأم فليس فيها عناصر البنت. وعندما نفحص المواد لمعرفة عمرها نرى فيها عناصر بنت وأم، فعناصر البنت قد تشكلت من عناصر الام بعد حصول التحلل الاشعاعي كما وضحت أعلاه. عندما تتشكل مادة ما فأنها تمنع عناصر البنت من التسرب إليها نتيجة حصول تسخن كبير جدا لها وعناصر البنت التي تتشكل على مر الزمن سوف تتلاشى بواسطة الانتشار بسبب فرق التركيز Diffusion عندها تكون الساعة النووية قد تم تصفيرها. ودرجة الحرارة التي عندها تحصل هذه العملية تسمى بدرجة الحرارة الكابحة. ودرجة الحرارة هذه تختلف باختلاف المادة.
معادلة حساب العمر[عدل]عندما تتحلل عناصر الأم غير المستقرة إلى عناصر البنت المستقرة فأن معادلة حساب العمر يربط التحلل الاشعاعي بالزمن الجيولوجي:
وفيها
t= عمر المادة
D= تركيز نظائر البنت
P= تركيز نظائر الأم
λ = ثابت التحلل لنظير الأم
ln= اللوغاريثم الطبيعي
ثابت التحلل λ هو ذلك الجزء من ذرات عنصر الأم التي تتحلل في وحدة الزمن ويتناسب عكسيا مع عمر النصف
وفيها
عمر النصف لعنصر الأم.
التقنية[عدل]شروط ينبغي توفرها للحصول على تحديد عمر جيد[عدل]ليس في كل الحالات تستطيع المادة عند تكوينها أن تأخذ عناصر الأم لوحدها فعادة تأخذ أيضا بعض عناصر البنت وفي هذه الحالة يجب علينا أن نفرض مسبقا قيمة نسبة تركيز عناصر البنت إلى تركيز عناصر الأم عندما تكوّنت المادة. يجب أن تكون عناصر البنت غير غازية لأنها تتسرب من المادة بسهولة, وعناصر البنت يجب أن تكون مستقرة بشكل يكفي لنا أن نقيس تراكيز عالية منها في المادة. بالإضافة إلى ذلك يجب على عناصر البنت والأم أن لا تكوّنا مواد فعّآلة كيماوية والتي تتفاعل بشكل نشط جدا داخل المادة. وكذلك يجب أن لا تحتوي المادة على كمية كبيرة من عناصر بنت أخرى نشأت من التحلل الاشعاعي لعناصر أم أخرى. وأخيرا يجب أن تكون طريقة عزل وفحص وتحليل التراكيز واضحة وموثوقة بها. عند استعمال طريقة التماثل الزمني Isochron (وهي من أبسط الطرق لتحديد العمر اشعاعيا) فاننا لسنا بحاجة إلى معرفة نسبة تركيز عناصر البنت إلى تركيز عناصر الأم عنما تكوّنت المادة المراد قياس عمرها الآن.
جهاز قياس الطيف الكتلي[عدل]مطيافية الكتلة (بالإنجليزية: Mass spectrometry) هذا الجهاز يستعمل في تحديد شكل ونوعية وماهية النظائر والجزيئات وخلائط الكيمياوية والبيولوجية والتي تكون بمقادير صغيرة جدا قد تصل إلى جزء واحد من المليار للغرام الواحد.
الجهاز الذي يستعمل هذه الطريقة تم اختراعه في أربعينيات القرن الماضي، ومنذ خمسينيات القرن الماضي يُستعمل هذا الجهاز لتحديد عمر المواد اشعاعيا. يقوم هذا الجهاز بواسطة السخونة الشديدة بشحن مجموعة من الذرات بالأيونات ويتم استخلاص هذه الذرات المتأينة من النموذج ويتم فصل الكتلة والشحنة الكهربائية عن بعضها، عندها يتم قياس الأيونات بواسطة مجسات خاصة تسمى بكؤوس الفاراداي (بالإنجليزية: Faraday cup)، عندما تتعرض هذه الكؤوس للأيونات هذه فان ذلك يؤدي إلى توليد كهربائية ضعيفة ويتم قياس هذه الكهربائية بدقة وعندها وبواسطة هذه القيم المقاسة يتم معرفة كمية تراكيز العناصر أو النظائر المختلفة (عناصر الأم والبنت).
نسبة الخطأ أو الدقة في تحديد العمر اشعاعيا[عدل]على الرغم من أن طريقة تحديد العمر اشعاعيا هي طريقة دقيقة إلا أن هذه الدقة تعتمد أساساً على التكنولوجيا والطريقة المستعملة في القياس.
من الممكن ان تؤثر النقاط أدناه على دقة النتائج المحصلة:
- تراكيز عناصر الأم والبنت عندما كانت المادة في مرحلة التكوّن؛
- كمية عناصر الأم أو البنت التي تسربت من المادة، أو حتى التي أضيفت إلى المادة خلال عمرها؛
- وجود نظائر معينة في النموذج والتي لها عدد الكتلي مساوي للعدد الكتلي لنظائر الأم والبنت يؤثر على دقة القياسات في جهاز قياس الطيف الكتلوي الآنف الذكر. في هذه الحالة يجب أن تُصحَح القياسات المأخوذة لتقليل تأثير العناصر الأخرى التي لها نفس الوزن (عدد الكتلة).
- كذلك يمكن أن يتعرض جهاز قياس الطيف الكتلي للكثير من التأثيرات العرضية. هذا الجهاز يجب أن يكون مفرغا من الهواء vacuum أن جودة ونوعية التفريغ من أهم العوامل التي تؤثر على القياسات. إذا كان الفراغ vacuum في الجهاز غير كامل (وجود غازات) فأن الذرات المتأينة تُستقبل من قبل جزيئات هذه الغازات بدلاً من أن تستقبل في كؤوس فاراداي لقياسها.
يمكن أن نرفع دقة قياس العمر بالاشعاع عن طريق أخذ عينات من أماكن مختلفة من النموذج المراد تقدير قِدَمه (عُمْره) لأنه إذا فرضنا أن جميع أجزاء العينة له نفس العمر فيجب منطقيا تعطي كافة القياسات نفس الزمن (العمر) isochron. يمكن مقارنة نتائج فحص نظامين نظائريين مع بعضهما في حالة تواجدهما معا في نفس العينة وذلك للتأكد من دقة القياسات.
دقة القياسات تعتمد أيضا على عمر النصف لعنصر الأم. فمثلا نظير كاربون المشع 14C لها عمر نصف أقل من 6000 سنة فليس من المعقول أن نستعمل 14C في تحديد عمر شيء يرجع قِدمه إلى 600 ألف سنة مثلا. لذلك في هذه الحالة يجب استمال أنظمة نظائرية أخرى. أن استعمال نظائر الكربون لتحديد أعمار أشياء ترجع إلى فترة من 1000 سنة إلى 50 ألف سنة قبل الآن يمكن أن يعطي نتائج دقيقة نسبيا.
الطرق المستعملة في تحديد العمر إشعاعياً[عدل]من أقدم الطرق المستعملة هي طريقة يورانيوم - رصاص لتحديد العمر، يُستعمل هذه الطريقة لتحديد عمر معدن الزركون (سليكات الزركونيوم) الذي عند تكوّنه يستبعد أخذ الرصاص بينما يأخذ تراكيز كبيرة من اليورانيوم. استعمال هذه الطريقة الآن يعطي نتائج فيها عدم دقة تصل إلى زائد ناقص 2 مليون سنة لشيء عمره 3 مليارات من السنين، هذه الطريقة تستعمل بكثرة في الداسات والفحوصات الجيولوجية. بما أن 235U تتحلل اشعاعيا إلى 207Pb وفي نفس الوقت238U تتحلل إلى 206Pb فأن هذه الطريقة لها ميزة جيدة جدا باننا نحصل على نتيجتين يمكننا مقارنتهما مع بعض لمعرفة مدى دقة القياسات المأخوذة.
طريقة بوتاسيم - أرغون لتحديد العمر تستعمل طريقة تحلّل 40K إلى 40Ar. فنظير بوتاسيم المشع أربعين 40K له عمر نصف كبير جدا وتتواجد بكثرة في المايكات Mica وفيلدسبارات Feldspar وفي هورنبليندات Hornblende لكن من أهم مساويء هذه الطريقة هي أن ل 40K درجة حرارة كابحة منخفضة جداً.
طريقة روبيديوم - سترونتيوم لتحديد العمر اشعاعيا تستعمل تحلّل 87Rb إلى 87Sr الذي له عمر نصف كبير جدا ودرجة حرارة الكابحة لهذه الطريقة هي كبيرة نسبياً، لكن لأنّ عمر النصف له كبير جدا فأن القياسات تكون غير دقيقة.
طريقة تحديد العمر بواسطة الكربون اشعاعيا تستعمل تحلل 14C اشعاعيا الذي له نصف عمر قليل نسبيا لذلك نرى بأن هذه الطريقة من أشهر الطرق في تحديد عمر المواد في علم الآثار Archaeology.
طريقة أخرى لها أيضا عمر نصف قليل نسبيا هي طريقة يورانيوم - ثوريوم لتحديد العمر اشعاعيا وفيها تستعمل تحلّل 238U إلى 230Th وكذلك 235U إلى 231Pa (Protactinium).
طرق أخرى لتحديد عمرالمواد اشعاعياً:
- ساماريوم - نيودايميوم؛
- لوتيتيوم - هافنيوم؛
- أرغون - أرغون؛
- هيليوم؛
- يورانيوم - يورانيوم؛
- رصاص - رصاص؛
- رهينيوم - ئوسميوم؛
- يوديوم - كسينون؛
- لانثانوم - باريوم.
تسربت الكثير من 36Cl في طبقة الأتموسفير للكرة الأرضية نتيجة التجارب الأسلحة النووية في خمسينيات القرن المنصرم ولأن 36Cl له عمر نصف قصير جداً فأنها تستعمل لمعرفة المسافات التي تقطعها تكتلات المياه الجوفية لكن هذه الطريقة لا تدخل ضمن مفهوم تحديد العمر اشعاعيا.
تحديد الأعمار في التطبيقات الفلكية بواسطة النظائر المفقودة (المتحلّلة)[عدل]عندما كان كوننا يافعا كان مليئا بنظائر مشعة ذات عمر قصير جدا مثل النظائر 26Al و60Fe و53Mn و129I، هذه النظائر المنقرضة ربما تم إنتاجها خلال عملية الأنفجار العظيم، هذه النظائر المتحللة يمكن لحد الآن قياسها من خلال النيازك التي تسقط على الأرض ومن خلال هذه القياسات يتم معرفة تسلسل الأحداث خلال عملية تكوين المجرات.
المصادر
malaak jabr
كيف تختلف الذرات
لذره:هي دقائق صغيره جداً لا ترى بالعين المجرده وتكون الماده. ويتكون العنصر الواحد من نوع واحد من الذرات المتشابهه بالشكل والحجم واللون وتختلف الذرات من عنصر الى اخر. العنصر: ماده تتألف من نوع واحد من الذرات . والمركب: يتألف من نوعين أو أكثر من الذرات. الجزيئ: أصغر جزء في الماده ويتكون من ذرتين أو أكثر ويكونون ملتصقين . مكونات الذره: 1-النواه: وهي جزء صغير جداً لا يرى بالعين المجرده يوجد في مركز الذره ويحتوي على
A- بروتونات
B- نيوترونات وكتلتهما متساوية.
البروتونات: جسيمات صغيرة جداً لا ترى بالعين المجرده و شحنتها موجبة.
النيوترونات: هي جسيمات صغيرة جداً لا ترى بالعين المجرده وهي غير مشحونه.
2-الإلكترونات : جسيمات تدور حول النواه شحنتها سالبه وكتلتها صغيره جداً. خصائص الذره: العدد الذري: هو عدد البروتونات في نواه الذره والعدد الذري مساوي لعدد الالكترونات ويعد هويه العنصر ولا يوجد عنصران متشابهان في العددالذري. العدد الكتلي : و هو عدد البروتونات اضافةً الى عدد النيوترونات في الذره واهملنا عدد الالكترونات لان كتلتها صغيرة جداً.
الجزيء :هو أصغر جسيم من المادة الكيميائية النقية يحتفظ بتركيبها الكيميائي وخواصها. علم دراسة الجزيئات يسمى كيمياء جزيئية أو فيزياء جزيئية ، تبعاً لمجال الرؤية المعين. تهتم الكيمياء الجزيئية بالقوانين التي تحكم التفاعلات بين الجزيئات التي ينتج عنها تكون أو تكسير للروابط الكيميائية، بينما تهتم الفيزياء الجزيئية بالقوانين التي تحكم بناء الجزيئات. وبصفة عامة، فإن الفرق بينها قد يكون غامضاً وصعب التحديد إلى حد ما.
يمكن للجزيء أن يتكوّن من ذرة واحدة (كما في الغازات النبيلة) أو من أكثر من ذرة مرتبطة معاً. يتم استخدام تصور الجزيء وحيد الذرة حصريا في نظرية الحركة للغازت. في علم الجزيئات يتكون الجزيء من نظام ثابت (حالة ترابط) يستوعب ذرتين أو أكثر. والمصطلح جزيء غير ثابت يستخدم للأنواع النشطة، أي الجسيمات التي لها عمر قصير (لها رنين) في الإلكترونات والذرات، مثل الجذور "Radicals", الجزيئات الأيونية, جزيء رايدبيرج (شاهد ذرة رايدبيرج), الحالات الانتقالية، متراكبات فان ريد فال، أو الأنظمة التي يحدث فيها تجمع للذرات في تكاثف بوس-أينيشتين. كما يستخدم المصطلح جزيء بصفة خاصة كمرادف "للرابطة التساهمية"، وهذا نتيجة للحقيقة التي تنص على أن المركبات غير التساهمية, المركبات الأيونية لا تنتج ما يمكن تعريفه بدقة على أنه "الجسيمات الدقيقة" التي يمن أن تتلائم مع التعريفات السابقة. كما يعرف أن المسامات الجزيئية هي الفراغات التي بين جزيئات المادة. ويتناسب حجم المسامات عكسيا مع قوى التجاذب بين الجزيئات. فتكون المسامات كبيرة بين جزيئات المادة الغازية ومتوسطة في المادة السائلة وصغيرة في المواد الصلبة. وتقدم المسامات الجزيئية تفسيرا واضحا لاختراق المواد لبعضها البعض. و رغم أن مصطلح الجزيء تم استخدامه لأول مرة في عام 1811 عن طريق أفوجادرو، كان المصطلح مادة مفتوحة للنقاش في مجتمع الكيمياء حتى ظهور نتائج أبحاث بيرن في عام 1911. كما أن النظرية الحديثة للجزيئات قد استفادت كثيرا من التقنيات المستخدمة في الكيمياء الحسابية. حجم الجزيء معظم الجزيئات صغيرة للغاية حتى يمكن رؤيتها بالعين المجردة، ولكن يوجد بعض الاستثناءات، فمثلا الجزيئات الكبيرة مثل جزيء DNA يمكن أن يصل للحجم المجهري. أصغر الجزيئات حجما هو جزيء الهيدروجين. المسافة بين الذرية له تكون 1.5 Å. ولكن يصعب تحديد السحابة الإلكترونية بدقة. وتحت الظروف العادية يكون للجزيء بعد يتراوح من عدة إلى عدة عشرات من Å. وقد يوجد روابط أخرى مثل الرابطة المشتركة حيث الرابطة المشتركة تتكون من ثلاثة أقسام احادية ثنايئية ثلاثية والرابطة التساهمية المعادلة الكيميائية: "المعادلة الكيميائية" تعكس الرقم الدقيق لعدد الذرات التي تكون الجزيء. ويتم حساب الكتلة الجزيئية من المعادلة الكيميائية في وحدات تساوى 12/1 من كتلة نظير ذرة C 12. هندسة الجزيء: الجزيئات لها حالة تعادل ثابتة بطول رابطة وزاوية بين الروابط معينين. وتتكون المادة النقية من جزيئات لها نفس البناء الفراغي. ويكون المعادلة الكيميائية وبناء الجزيء دور هام في تحديد خواص الجزيء, وخاصة نشاطيته. الأيزومرات تتشارك في نفس شكل المعادلة الكيميائية, ولكن يكون لكل منها خواص مختلفة تماما نظرا لاختلاف بنائها. الأيزومرات الفراغية، نوع خاص من الأيزومرات, ويمكن أن يكون لها خواص فيزوكيميائية متشابهه ولكن في نفس الوقت تختلف تماما في نشاطها الحيوي
malaak jabr
A- بروتونات
B- نيوترونات وكتلتهما متساوية.
البروتونات: جسيمات صغيرة جداً لا ترى بالعين المجرده و شحنتها موجبة.
النيوترونات: هي جسيمات صغيرة جداً لا ترى بالعين المجرده وهي غير مشحونه.
2-الإلكترونات : جسيمات تدور حول النواه شحنتها سالبه وكتلتها صغيره جداً. خصائص الذره: العدد الذري: هو عدد البروتونات في نواه الذره والعدد الذري مساوي لعدد الالكترونات ويعد هويه العنصر ولا يوجد عنصران متشابهان في العددالذري. العدد الكتلي : و هو عدد البروتونات اضافةً الى عدد النيوترونات في الذره واهملنا عدد الالكترونات لان كتلتها صغيرة جداً.
الجزيء :هو أصغر جسيم من المادة الكيميائية النقية يحتفظ بتركيبها الكيميائي وخواصها. علم دراسة الجزيئات يسمى كيمياء جزيئية أو فيزياء جزيئية ، تبعاً لمجال الرؤية المعين. تهتم الكيمياء الجزيئية بالقوانين التي تحكم التفاعلات بين الجزيئات التي ينتج عنها تكون أو تكسير للروابط الكيميائية، بينما تهتم الفيزياء الجزيئية بالقوانين التي تحكم بناء الجزيئات. وبصفة عامة، فإن الفرق بينها قد يكون غامضاً وصعب التحديد إلى حد ما.
يمكن للجزيء أن يتكوّن من ذرة واحدة (كما في الغازات النبيلة) أو من أكثر من ذرة مرتبطة معاً. يتم استخدام تصور الجزيء وحيد الذرة حصريا في نظرية الحركة للغازت. في علم الجزيئات يتكون الجزيء من نظام ثابت (حالة ترابط) يستوعب ذرتين أو أكثر. والمصطلح جزيء غير ثابت يستخدم للأنواع النشطة، أي الجسيمات التي لها عمر قصير (لها رنين) في الإلكترونات والذرات، مثل الجذور "Radicals", الجزيئات الأيونية, جزيء رايدبيرج (شاهد ذرة رايدبيرج), الحالات الانتقالية، متراكبات فان ريد فال، أو الأنظمة التي يحدث فيها تجمع للذرات في تكاثف بوس-أينيشتين. كما يستخدم المصطلح جزيء بصفة خاصة كمرادف "للرابطة التساهمية"، وهذا نتيجة للحقيقة التي تنص على أن المركبات غير التساهمية, المركبات الأيونية لا تنتج ما يمكن تعريفه بدقة على أنه "الجسيمات الدقيقة" التي يمن أن تتلائم مع التعريفات السابقة. كما يعرف أن المسامات الجزيئية هي الفراغات التي بين جزيئات المادة. ويتناسب حجم المسامات عكسيا مع قوى التجاذب بين الجزيئات. فتكون المسامات كبيرة بين جزيئات المادة الغازية ومتوسطة في المادة السائلة وصغيرة في المواد الصلبة. وتقدم المسامات الجزيئية تفسيرا واضحا لاختراق المواد لبعضها البعض. و رغم أن مصطلح الجزيء تم استخدامه لأول مرة في عام 1811 عن طريق أفوجادرو، كان المصطلح مادة مفتوحة للنقاش في مجتمع الكيمياء حتى ظهور نتائج أبحاث بيرن في عام 1911. كما أن النظرية الحديثة للجزيئات قد استفادت كثيرا من التقنيات المستخدمة في الكيمياء الحسابية. حجم الجزيء معظم الجزيئات صغيرة للغاية حتى يمكن رؤيتها بالعين المجردة، ولكن يوجد بعض الاستثناءات، فمثلا الجزيئات الكبيرة مثل جزيء DNA يمكن أن يصل للحجم المجهري. أصغر الجزيئات حجما هو جزيء الهيدروجين. المسافة بين الذرية له تكون 1.5 Å. ولكن يصعب تحديد السحابة الإلكترونية بدقة. وتحت الظروف العادية يكون للجزيء بعد يتراوح من عدة إلى عدة عشرات من Å. وقد يوجد روابط أخرى مثل الرابطة المشتركة حيث الرابطة المشتركة تتكون من ثلاثة أقسام احادية ثنايئية ثلاثية والرابطة التساهمية المعادلة الكيميائية: "المعادلة الكيميائية" تعكس الرقم الدقيق لعدد الذرات التي تكون الجزيء. ويتم حساب الكتلة الجزيئية من المعادلة الكيميائية في وحدات تساوى 12/1 من كتلة نظير ذرة C 12. هندسة الجزيء: الجزيئات لها حالة تعادل ثابتة بطول رابطة وزاوية بين الروابط معينين. وتتكون المادة النقية من جزيئات لها نفس البناء الفراغي. ويكون المعادلة الكيميائية وبناء الجزيء دور هام في تحديد خواص الجزيء, وخاصة نشاطيته. الأيزومرات تتشارك في نفس شكل المعادلة الكيميائية, ولكن يكون لكل منها خواص مختلفة تماما نظرا لاختلاف بنائها. الأيزومرات الفراغية، نوع خاص من الأيزومرات, ويمكن أن يكون لها خواص فيزوكيميائية متشابهه ولكن في نفس الوقت تختلف تماما في نشاطها الحيوي
malaak jabr
تعريف لـــــــــــــــــذرة
ـالذرة هي تركيب مجهري يوجد في اية مادة عادية من حولنا. تتكون الذرات من ثلاثة أنواع من الجزيئات الذرية الفرعية هي :
· الألكترونات - ولها شحنة سالبة.
· البروتونات - ولها شحنة موجبة.
· النيوترون - ليس له شحنة (محايد).
الذرات هي كتل البناء الأساسية للكيمياء، ومحفوظة في التفاعلات الكيمياوية، وهي الجزيء الأصغر للعنصر الكيميائي ؛ عندما تنقسم ذرة عنصر معين يتوقف عن كونه ذلك العنصر، اي يتحول الى عنصر اخر، وقد حدد عدد 91 عنصر وجدت طبيعيا على الأرض.
كل عنصر فريد بعدد البروتونات في كل ذرة ذلك العنصر، كل ذرة لها عدد من الألكترونات يساوي عددها من البروتونات؛ إذا حدث عدم توازن تدعى الذرة في هذه الحالة آيون او ذرة متأينة. ذرات نفس العنصر يمكن أن تأخذ أعداد مختلفة من النيوترونات طالما عدد البروتونات أو الألكترونات لا تتغيران، والذرات ذوات الأعداد المختلفة من النيوترون تدعو نظائر مشعة للعنصر الكيميائي.
العناصر الأخرى خلقت بشكل إصطناعي، لكنها عناصر غير مستقرة عادة وتلقائيا تغيير إلى العناصر الكيميائية الطبيعية المستقرة بعمليات التحلل الإشعاعي.
مع ذلك 91 عنصر فقط موجود بصورة طبيعية، ذرات هذه العناصر قادرة على الإلتصاق بالجزيئات والأنواع الأخرى من المركبات الكيميائية. الجزيئات تتكون من الذرات المتعددة؛ على سبيل المثال جزيء الماء يتكون من اتحاد ذرتين من الهيدروجين وذرة أوكسجين واحدة.
التركيب
النموذج المقبول على نحو واسع هو نموذج الموجه، وهو مستند على نموذج بوهر، لكن يأخذ في الحسبان التطورات الحديثة والإكتشافات في ميكانيك الكم.
الذرات تتكون من جزيئات فرعية (بروتونات، ألكترونات، ونيوترون)، حجم الفراغ كبير في الذرة، مركز الذرة صغير جدا، النواة ذات شحنة موجبة وتتألف من بروتونات ونيوترون، وحجم النواة ثمثل اصغر من 100,000 مرة من حجم الذرة.
عندما تنضم إلكترونات إلى ذرة معينة، تستقر في القشرة الاقل طاقة، ذلك هو المدار الأقرب إلى النواة، ويسمى (القشرة الأولى). اما الألكترونات في المدار الأبعد (قشرة التكافؤ) فهي التي تكون جاهزة للإلتصاق الذري.
حجم الذرة
حجم الذرة لا تحدد بسهولة حيث ان مدار الإلكترون تتحرم الصفر بشكل تدريجي حسب الزيادات في المسافة عن النواة. للذرات التي يمكن أن تشكل بلورات صلبة، المسافة بين النوى المجاورة يمكن أن تعطي تقدير لحجم الذرّة. للذرات التي لا تشكل بلورات الصلبة الأخرى نستعمل تكنيك أخر، يدخل في ذلك الحسابات النظرية. كمثال، حجم ذرة الهيدروجين تقدر تقريبا بـ 1.2 × 10-10 . قارن هذا إلى حجم البروتون الذي هو جزيء في نواة ذرة الهيدروجين التي هي تقريبا 0.87 × 10-15 m. هكذا النسبة بين الأحجام في ذرة الهيدروجين إلى نواتها يساوي تقريبا 100,000. ذرات العناصر المختلفة تتفاوت في الحجم، لكن الأحجام تقريبا نفسها. إن السبب لهذا يرجع الى تلك العناصر ذات شحنة موجبة كبيرة في النواة تجذب الألكترونات إلى مركز الذرة بقوة أكثر.
العناصر والنظائر المشعة
الذرات تصنف عموما بعددها الذري، الذي يقابل عدد البروتونات في الذرة. يحدد العدد الذري لاي عنصر تنتمي تلك الذرة. على سبيل المثال، ذرات الكربون تحتوي على ستة بروتونات، كل الذرات التي بنفس هذا العدد الذري تشارك في تشكيلة منوعة من الخواص الفزيائية وتظهر نفس السلوك الكيميائي.
رقم الكتلة، العدد الذري للكتلة، أو العدد النيكلوني لعنصر هو العدد الكلي للبروتونات والنيوترون في ذرة ذلك العنصر، لأن كل بروتون أو نيوترون اساسا له كتلة من 1 amu. عدد النيوترون في ذرة ليس له تأثير على نوع العنصر. كل عنصر يمكن أن يتخذ ذرات مختلفة عديدة لكن بنفس عدد البروتونات والألكترونات، لكن أعداد مختلفة من النيوترون. كل من له نفس العدد الذري لكن رقم كتلة مختلف، هذه تدعى النظائر المشعة لعنصر ما. عند كتابة اسم نظير مشع، اسم العنصر يتبع بالرقم الكتلة. على سبيل المثال، كربون 14 يحتوي على ستة بروتونات وثمانية نيوترونات في كل ذرّة، ليكون رقم الكتلة الكلي من 14.
إنّ ذرة الهيدروجين هي ابسط الذرات، لها عدد ذري 1 وتشمل بروتون واحد وإلكترون واحد. نظائر الهيدروجين المشعة التي تحتوي نيوترون واحد تدعى الديوتوريم Deuterium أو هيدروجين2 ؛ إما نظائر الهيدروجين المشعة التي تحتوي على إثنان نيوترون تدعى تريتيم Tritium أو هيدروجين 3.
إن الكتلة الذرية التي أدرجت لكل عنصر في الجدول الدوري هي معدل كتلة النظير المشع الموجود في الطبيعة مرجحا بدرجة وفرتهم.
التكافؤ والتراكيب
إن السلوك الكيميائي للذرات يعود بشكل كبير بسبب التفاعلات بين الألكترونات. ألكترونات ذرّة معينة يجب أن تبقى ضمن الترتيبات الالكترون المتوقّعة والمحددة. تسقط الألكترونات إلى القشور مستندة على مسافتهم النسبية من النواة (يرجع لتركيب الذرة للمزيد من التفاصيل). الألكترونات في القشرة الأبعد، تمسى إلكترونات التكافؤ، لها التأثير الأكبر على السلوك الكيميائي. إلكترونات المركز (تلك ليست في القشرة الخارجية) تلعب دورا، لكنه عادة ذا تأثير ثانوي بسبب حاجز الشحنة الموجبة في نواة الذرة.
كل غلاف، مرقم من الأقرب إلى النواة، يمكن أن يمسك عدد محدد من الإلكترونات يعود ذلك حسب اختلاف عدد ونوعه المدار.
الغلاف 1: 2 ألكترونات
الغلاف 2: 8 ألكترونات
الغلاف 3: 8 أو 18 ألكترون (إعتمادا على العنصر)
تملأ الألكترونات المدارات من الداخل الى الخارج، يبدآن بغلاف واحد. تجد الاغلفة ذات الارقام الأعلى توجد فقط عند الضرورة وتحدد بعدد الألكترونات. أي غلاف موجود خارجيا هو غلاف التكافؤ، حتى ولو كان ذا إلكترون واحد فقط.
السبب الذي ملئ الأغلفة بالترتيب بأن مستويات طاقة الألكترونات في الأغلفة الأعمق أقل جدا من مستويات طاقة الألكترونات في الأغلفة الخارجية. إذن لو أن الأغلفة الداخلية لم تكن ممتلئة تماما، الألكترون في الغلاف الخارجي يسقط بسرعة إلى الغلاف الداخلي (بإشعاع الفوتون الذي يحمل الإختلاف في مستويات الطاقة.
الذرات في الكون والعالم من حولنا
بإستعمال نظرية التوسع، عدد الذرات في الكون الملاحظ يمكن توقعه بأن يكون بين 4x1078 و6x1079 . وبسبب الطبيعة اللانهائية للكون، فإن العدد الكلي للذرات في كامل الكون قد يكون أكثر بكثير أو لانهائي. هذا لا يغير من العدد المتوقع للذرات في الكون الملاحظ ضمن حوالي 14 بليون سنة ضوئية - الذي كل مايمكن أن نلاحظه فقط هو بعمر 14 بليون سنة.
malaak jabr
· الألكترونات - ولها شحنة سالبة.
· البروتونات - ولها شحنة موجبة.
· النيوترون - ليس له شحنة (محايد).
الذرات هي كتل البناء الأساسية للكيمياء، ومحفوظة في التفاعلات الكيمياوية، وهي الجزيء الأصغر للعنصر الكيميائي ؛ عندما تنقسم ذرة عنصر معين يتوقف عن كونه ذلك العنصر، اي يتحول الى عنصر اخر، وقد حدد عدد 91 عنصر وجدت طبيعيا على الأرض.
كل عنصر فريد بعدد البروتونات في كل ذرة ذلك العنصر، كل ذرة لها عدد من الألكترونات يساوي عددها من البروتونات؛ إذا حدث عدم توازن تدعى الذرة في هذه الحالة آيون او ذرة متأينة. ذرات نفس العنصر يمكن أن تأخذ أعداد مختلفة من النيوترونات طالما عدد البروتونات أو الألكترونات لا تتغيران، والذرات ذوات الأعداد المختلفة من النيوترون تدعو نظائر مشعة للعنصر الكيميائي.
العناصر الأخرى خلقت بشكل إصطناعي، لكنها عناصر غير مستقرة عادة وتلقائيا تغيير إلى العناصر الكيميائية الطبيعية المستقرة بعمليات التحلل الإشعاعي.
مع ذلك 91 عنصر فقط موجود بصورة طبيعية، ذرات هذه العناصر قادرة على الإلتصاق بالجزيئات والأنواع الأخرى من المركبات الكيميائية. الجزيئات تتكون من الذرات المتعددة؛ على سبيل المثال جزيء الماء يتكون من اتحاد ذرتين من الهيدروجين وذرة أوكسجين واحدة.
التركيب
النموذج المقبول على نحو واسع هو نموذج الموجه، وهو مستند على نموذج بوهر، لكن يأخذ في الحسبان التطورات الحديثة والإكتشافات في ميكانيك الكم.
الذرات تتكون من جزيئات فرعية (بروتونات، ألكترونات، ونيوترون)، حجم الفراغ كبير في الذرة، مركز الذرة صغير جدا، النواة ذات شحنة موجبة وتتألف من بروتونات ونيوترون، وحجم النواة ثمثل اصغر من 100,000 مرة من حجم الذرة.
عندما تنضم إلكترونات إلى ذرة معينة، تستقر في القشرة الاقل طاقة، ذلك هو المدار الأقرب إلى النواة، ويسمى (القشرة الأولى). اما الألكترونات في المدار الأبعد (قشرة التكافؤ) فهي التي تكون جاهزة للإلتصاق الذري.
حجم الذرة
حجم الذرة لا تحدد بسهولة حيث ان مدار الإلكترون تتحرم الصفر بشكل تدريجي حسب الزيادات في المسافة عن النواة. للذرات التي يمكن أن تشكل بلورات صلبة، المسافة بين النوى المجاورة يمكن أن تعطي تقدير لحجم الذرّة. للذرات التي لا تشكل بلورات الصلبة الأخرى نستعمل تكنيك أخر، يدخل في ذلك الحسابات النظرية. كمثال، حجم ذرة الهيدروجين تقدر تقريبا بـ 1.2 × 10-10 . قارن هذا إلى حجم البروتون الذي هو جزيء في نواة ذرة الهيدروجين التي هي تقريبا 0.87 × 10-15 m. هكذا النسبة بين الأحجام في ذرة الهيدروجين إلى نواتها يساوي تقريبا 100,000. ذرات العناصر المختلفة تتفاوت في الحجم، لكن الأحجام تقريبا نفسها. إن السبب لهذا يرجع الى تلك العناصر ذات شحنة موجبة كبيرة في النواة تجذب الألكترونات إلى مركز الذرة بقوة أكثر.
العناصر والنظائر المشعة
الذرات تصنف عموما بعددها الذري، الذي يقابل عدد البروتونات في الذرة. يحدد العدد الذري لاي عنصر تنتمي تلك الذرة. على سبيل المثال، ذرات الكربون تحتوي على ستة بروتونات، كل الذرات التي بنفس هذا العدد الذري تشارك في تشكيلة منوعة من الخواص الفزيائية وتظهر نفس السلوك الكيميائي.
رقم الكتلة، العدد الذري للكتلة، أو العدد النيكلوني لعنصر هو العدد الكلي للبروتونات والنيوترون في ذرة ذلك العنصر، لأن كل بروتون أو نيوترون اساسا له كتلة من 1 amu. عدد النيوترون في ذرة ليس له تأثير على نوع العنصر. كل عنصر يمكن أن يتخذ ذرات مختلفة عديدة لكن بنفس عدد البروتونات والألكترونات، لكن أعداد مختلفة من النيوترون. كل من له نفس العدد الذري لكن رقم كتلة مختلف، هذه تدعى النظائر المشعة لعنصر ما. عند كتابة اسم نظير مشع، اسم العنصر يتبع بالرقم الكتلة. على سبيل المثال، كربون 14 يحتوي على ستة بروتونات وثمانية نيوترونات في كل ذرّة، ليكون رقم الكتلة الكلي من 14.
إنّ ذرة الهيدروجين هي ابسط الذرات، لها عدد ذري 1 وتشمل بروتون واحد وإلكترون واحد. نظائر الهيدروجين المشعة التي تحتوي نيوترون واحد تدعى الديوتوريم Deuterium أو هيدروجين2 ؛ إما نظائر الهيدروجين المشعة التي تحتوي على إثنان نيوترون تدعى تريتيم Tritium أو هيدروجين 3.
إن الكتلة الذرية التي أدرجت لكل عنصر في الجدول الدوري هي معدل كتلة النظير المشع الموجود في الطبيعة مرجحا بدرجة وفرتهم.
التكافؤ والتراكيب
إن السلوك الكيميائي للذرات يعود بشكل كبير بسبب التفاعلات بين الألكترونات. ألكترونات ذرّة معينة يجب أن تبقى ضمن الترتيبات الالكترون المتوقّعة والمحددة. تسقط الألكترونات إلى القشور مستندة على مسافتهم النسبية من النواة (يرجع لتركيب الذرة للمزيد من التفاصيل). الألكترونات في القشرة الأبعد، تمسى إلكترونات التكافؤ، لها التأثير الأكبر على السلوك الكيميائي. إلكترونات المركز (تلك ليست في القشرة الخارجية) تلعب دورا، لكنه عادة ذا تأثير ثانوي بسبب حاجز الشحنة الموجبة في نواة الذرة.
كل غلاف، مرقم من الأقرب إلى النواة، يمكن أن يمسك عدد محدد من الإلكترونات يعود ذلك حسب اختلاف عدد ونوعه المدار.
الغلاف 1: 2 ألكترونات
الغلاف 2: 8 ألكترونات
الغلاف 3: 8 أو 18 ألكترون (إعتمادا على العنصر)
تملأ الألكترونات المدارات من الداخل الى الخارج، يبدآن بغلاف واحد. تجد الاغلفة ذات الارقام الأعلى توجد فقط عند الضرورة وتحدد بعدد الألكترونات. أي غلاف موجود خارجيا هو غلاف التكافؤ، حتى ولو كان ذا إلكترون واحد فقط.
السبب الذي ملئ الأغلفة بالترتيب بأن مستويات طاقة الألكترونات في الأغلفة الأعمق أقل جدا من مستويات طاقة الألكترونات في الأغلفة الخارجية. إذن لو أن الأغلفة الداخلية لم تكن ممتلئة تماما، الألكترون في الغلاف الخارجي يسقط بسرعة إلى الغلاف الداخلي (بإشعاع الفوتون الذي يحمل الإختلاف في مستويات الطاقة.
الذرات في الكون والعالم من حولنا
بإستعمال نظرية التوسع، عدد الذرات في الكون الملاحظ يمكن توقعه بأن يكون بين 4x1078 و6x1079 . وبسبب الطبيعة اللانهائية للكون، فإن العدد الكلي للذرات في كامل الكون قد يكون أكثر بكثير أو لانهائي. هذا لا يغير من العدد المتوقع للذرات في الكون الملاحظ ضمن حوالي 14 بليون سنة ضوئية - الذي كل مايمكن أن نلاحظه فقط هو بعمر 14 بليون سنة.
malaak jabr
النظريات القديمة للمادة – أفكار الفلاسفة الإغريق .- افكار الفلاسفة الإغريق حول المادة
* ديمقريطس Democritus ( ٣٧٠-٤٦٠ ) ق.م :
- تتكون المادة من ذرات تتحرك في الفراغ .
- الذرات الصلبة ، متجانسة ، لاتتحطم ولاتتجزأ .
- الأنواع المختلفة من الذرات لها أحجام وأشكال مختلفة .
- حجم الذرات وشكلها وحركتها يحدد خواص المادة .
* أرسطو Aristotl ( ٣٢٢-٣٤٨ ) ق.م :
- لا وجود للفراغ .
- الماده مكونة من التراب ، والنار ، والهواء ، والماء .
* جون دالتون John Dalton ( ١٧٦٦-١٨٤٤ ) م :
- الذرات لاتتجزأ ولاتتكسر.
- تختلف ذرات أي عنصر عن ذرات العناصر الأخرى .
- في التفاعلات الكميائية : تنفصل الذرات ، أو تتحد ، أو يعاد ترتيبها .
- malaak jabr
قانون النسب المتضاعفة
قانون النسب المتضاعفة هو أحد القوانين الأساسية في قياس اتحادية العناصر واكتشفه الكيميائي الأنكليزي جون دالتون سنة 1803. ينص القانون على أنه عند اتحاد عنصران كيميائيان، وتكوين أكثر من مركب واحد، فإن النسبة بين الكتل المختلفة من أحد العنصرين التي تتحد مع كتلة ثابتة من العنصر الآخر تكون نسبة عددية صحيحة وبسيطة. مثلا يتفاعل الأكسجين والكربون ليشكلا أول أكسيد الكربون (CO) أو ثاني أكسيد الكربون (CO2)، ولكن لا يمكن تشكيل CO1.3.
بالإضافة إلى أنه ينص على أنه إذا شكل العنصران الكيميائيان المتفإعلان أكثر من مركب كيميائي واحد، فإن نسب الكتل للعنصر الثاني إلى الكتلة الثابتة للعنصر الأول ستكون أيضا نسبة عددية صحيحة وبسيطة.
التاريخ[عدل]ان أول من أوجد قانون النسب المتضاعفة هو العالم الإنجليزي جون دالتون حيث فسرت نظريته (النظرية الذرية)التي أوجدها حوالي عام 1803 قانون النسب المتضاعفة.وبعده جاء العالم جاك لوسك ليطبق النظرية بقانون رياضي عملي.
أمثلة[عدل]عند يكوين مركبين مختلفين من نفس العنصرين فان كتلتي أحد العنصرين اللتين تتفإعلان مع كتلة ثابتة من العنصر الآخر تكونان في شكل نسبة عددين بسيطين وصحيحين.
ضغط الغاز / درجة الحراة المطلقة = مقدار ثابت ويمكن كتابة العلاقة بالشكل التالي : p1/T1 = p2/T2.
وبناءً على هذا القانون تكون حجوم الغازات الداخلة في التفاعل والناتجة عنه مرتبطة بنسب مكوّنة من أعداد صحيحة وبسيطة عند نفس الظروف من الضغط ودرجة الحرارة.وفي معادلة الماء مثلا:
O2 + 2H2 = 2H2O. في هذا التفاعل وغيره من التفاعلات نرى أن الغازات تتفاعل بنسب حجمية ثابتة مكوّنة من أعداد صحيحة وصغيرة عند ثبوت الضغط ودرجة الحرارة.
وترتبط الغازات بالنسب الحجمية التالية : حجم واحد من O2 : حجمين من H2 : حجمين من بخار الماء H2O. بمعنى لو تفاعل لترين من غازالأكسجين فإنّه سيتفاعل 4 لترات من غاز الهيدروجين وينتج 4 لترات من بخار الماء.ولو تفاعل 10 لترات من غاز الأكسجين فإنّه سيتفاعل 20 لتر من غاز الهيدروجين وينتج 20 لتر من بخار الماء. الجدول الأول
جدول 1: العلاقات الرياضية للهيدروجين والنيتروجين ومركبات الأكسجينمجمعجدول التفاعلاتالهدروجينكتلة النيتروجينكتلة الأوكسجينمجمع التفاعلات الرياضيةالهيدروجين النيتروجيناكسيد النيتريك15.0 g-7.0 g8.0 g-7.08.0الأمونيا8.5 g1.5 g7.0 g-1.57.0-الماء9.0 g1.0 g-8.0 g1.0-8.0المراجع[عدل]
malaak jabr
بالإضافة إلى أنه ينص على أنه إذا شكل العنصران الكيميائيان المتفإعلان أكثر من مركب كيميائي واحد، فإن نسب الكتل للعنصر الثاني إلى الكتلة الثابتة للعنصر الأول ستكون أيضا نسبة عددية صحيحة وبسيطة.
التاريخ[عدل]ان أول من أوجد قانون النسب المتضاعفة هو العالم الإنجليزي جون دالتون حيث فسرت نظريته (النظرية الذرية)التي أوجدها حوالي عام 1803 قانون النسب المتضاعفة.وبعده جاء العالم جاك لوسك ليطبق النظرية بقانون رياضي عملي.
أمثلة[عدل]عند يكوين مركبين مختلفين من نفس العنصرين فان كتلتي أحد العنصرين اللتين تتفإعلان مع كتلة ثابتة من العنصر الآخر تكونان في شكل نسبة عددين بسيطين وصحيحين.
ضغط الغاز / درجة الحراة المطلقة = مقدار ثابت ويمكن كتابة العلاقة بالشكل التالي : p1/T1 = p2/T2.
وبناءً على هذا القانون تكون حجوم الغازات الداخلة في التفاعل والناتجة عنه مرتبطة بنسب مكوّنة من أعداد صحيحة وبسيطة عند نفس الظروف من الضغط ودرجة الحرارة.وفي معادلة الماء مثلا:
O2 + 2H2 = 2H2O. في هذا التفاعل وغيره من التفاعلات نرى أن الغازات تتفاعل بنسب حجمية ثابتة مكوّنة من أعداد صحيحة وصغيرة عند ثبوت الضغط ودرجة الحرارة.
وترتبط الغازات بالنسب الحجمية التالية : حجم واحد من O2 : حجمين من H2 : حجمين من بخار الماء H2O. بمعنى لو تفاعل لترين من غازالأكسجين فإنّه سيتفاعل 4 لترات من غاز الهيدروجين وينتج 4 لترات من بخار الماء.ولو تفاعل 10 لترات من غاز الأكسجين فإنّه سيتفاعل 20 لتر من غاز الهيدروجين وينتج 20 لتر من بخار الماء. الجدول الأول
جدول 1: العلاقات الرياضية للهيدروجين والنيتروجين ومركبات الأكسجينمجمعجدول التفاعلاتالهدروجينكتلة النيتروجينكتلة الأوكسجينمجمع التفاعلات الرياضيةالهيدروجين النيتروجيناكسيد النيتريك15.0 g-7.0 g8.0 g-7.08.0الأمونيا8.5 g1.5 g7.0 g-1.57.0-الماء9.0 g1.0 g-8.0 g1.0-8.0المراجع[عدل]
- This article incorporates text from the Connexions article "About: The Atomic Molecular Theory" by author John S. Hutchinson, which was released under the Creative Commons - Attribution (CC-by) 1.0 license. This statement is included in accordance with the license attribution requirements
malaak jabr
المخاليط
العنصر : مادة تتكون من نفسها فقط ولايمكن تبسيطها أكثر من ذلك
مثل جميع عناصر الجدول الدوري
المخلوط : خليط أو مزيج من مادتين أو أكثر ويمكن فصلها بطريقة بسيطة مثل
( الترشيح – التقطير – قمع الفصل – المغناطيس ) وغيرها
من المخاليط مزيج من أكثر من مادة غير متفاعلة و
ماءورمل - رمل وبرادة حديد - ماء وملح - الهواء الجوي )وغيرها
المركب : مادة تتكون من عنصرين أو أكثر ومتحدة معا لايمكن فصلها إلا بالتفاعلات الكيمائية
من المركبات
الاحماض ( حمض الكبريتيك – حمض اهيدروكلوريك ) وغيرها
– الاكاسيد - ( اكسيد الحديد – اكسيد النحاس –أكسيد الفضة ) وغيرها
الاملاح ( نترات الفضة – كلوريد الصوديوم – كبريتات النحاس ) وغيرها
صنف المواد التالية في الجدول التالي
ورق الشجر - ذهب - ملح الطعام المنزلي - ثاني أوكسيد الكربون - أرز - بخار الماء - النيتروجين - التراب الدم الإنساني. – البطاطا- هيدروجين – يوديد البوتاسيوم - نترات الكالسيوم – اكسيد الزئبق–الهواء الجوي – المغنسيوم –الكبريت- ماء البحر – السلطة
عناصر مخاليط مركبات
فصل المخاليط Analyzes
مستعينا بالوسائل التالية بين كيف يمكن فصل المخاليط التالية إلى مكوناتها
(( الترشيح – التقطير – قمع الفصل – الملعقة – اليد – المنخل – المصفاة – المغناطيس ))
المخلوط mixture طريقة الفصلseparation
الرمل والماء
الارز والماء
الملح والماء
الكرات الزجاجية والرمل والماء
ملح الطعام والرمل
الرمل وبرادة الحديد
الزيت والماء
المكسرات
امامك مجموعة من المواد سواء المركبات أو المخاليط بين مكونات كل منها
المادة Matter المكونات Analyze العناصر المكونة
ملح الطعام (كلوريد الصوديوم ) .
الماء
اكسيد الماغنسيوم
مخلوط الكبريت وبرادة الحديد
ثاني اكسيد الكربون
كلوريد الهيدروجين
اكسيد النحاس
malaak jabr
خواص المواد
خواص المادة هي سمات مميزة لكل مادة، وتعرف بأنها غير مقدارية (لا تختلف باختلاف مقدار المادة) ويمكن غالبا وصفها كميا، وذلك من خلال وحدات للقياس تمكننا من المقارنة بين المواد وترتيبها حسب كل خاصية مما يساعد في اختيار المادة حسب المواصفات المطلوبة.فمثلا الكثافة ووحدتها كيلوجرام/مترمكعب هي خاصية غير مقدارية للمادة حيث أنها ثابتة أينما أخذنا العينة من المادة الموجودة . وكذلك حرارة نوعية ووحدتها جول/مول أيضا خاصية غير مقدارية حيث أنها تنطبق على أي مول من المادة . تسمى تلك الخاصيتان وأشباههما في الترموديناميكا "خاصية مكثفة".
وقد تكون خواص المادة رقما ثابتا وقد تتغير حسب متغير (مثل الحرارة) أو أكثر من متغير. وقد تتغير قيمة خواص المادة تبعا لاتجاه القياس وهو ما يعرف بـ تباينية الخواص. مثال على ذلك أن مغناطيسية بلورة في اتجاه المحور السيني قد تختلف عن مغناطيسيتها في اتجاه المحور الصادي.
وبالنسبة للخواص التي تربط بين ظاهرتين طبيعيتين فهي تتغير بشكل خطي أو شبه خطي خلال نطاق معين، فهي تعتبر قيمة ثابتة خلال هذا النطاق.
محتويات [أخف]
خواص فيزيائية[عدل]خواص ميكانيكية[عدل]معامل يونج (بالإنجليزية: Young's Modulus)
معامل المرونة النوعي (بالإنجليزية: Specific Modulus)
مقاومة الشد (بالإنجليزية: tensile strength)
مقاومة الانضغاط (بالإنجليزية: Compressive Strength)
مقاومة القص (بالإنجليزية: Shear Strength)
مقاومة الخضوع (بالإنجليزية: YIELD Strength)
المطيلية (بالإنجليزية: Ductility)
قابلية الطرق (بالإنجليزية: Malleability)
الانفعال عند الانهيار (بالإنجليزية: Strain at failure)
مؤشر التصليد بالانفعال (بالإنجليزية: Strain hardening INDEX)
الصلادة (بالإنجليزية: Hardness)
المتانة (بالإنجليزية: Toughness)
شدة تحمل صدمة (بالإنجليزية: Impact Toughness)
نسبة بواسون (بالإنجليزية: Poisson's ratio)
التصليدية (للمعادن) (بالإنجليزية: Hardenability)
قابلية اللحام (بالإنجليزية: Weldability)
حد الكلال أو حد التعب (بالإنجليزية: Fatigue Limit)
الكثافة (بالإنجليزية: Densiy)
اللزوجة (بالإنجليزية: Viscosity)
النفاذية (بالإنجليزية: Permeability)
المسامية (بالإنجليزية: Porosity)
السرعة الانفجارية (بالإنجليزية: Explosive Velocity)
مؤشر السريان عند الانصهار (بالإنجليزية: Melt Flow INDEX)
الثوابت الكهرضغطية (بالإنجليزية: Piezoelectric constants)
الرجوعية (بالإنجليزية: Resilience)
خواص كهربية[عدل]الموصلية الكهربائية أو الناقلية الكهربائية (بالإنجليزية: Electrical Conductivity)
السماحية (بالإنجليزية: Permitivity)
ثابت العازل (بالإنجليزية: Dielectric Constant)
شدة العزل (بالإنجليزية: Dielectric Strength)
الثوابت الكهرضغطية (بالإنجليزية: Piezoelectric Constants)
معامل سيبيك (بالإنجليزية: Seebeck coefficient)
خواص حرارية[عدل]الموصلية الحرارية (بالإنجليزية: Thermal Conductivity)
معامل الانتشار (بالإنجليزية: Diffusivity)
معامل سيبيك (بالإنجليزية: Seebeck Coeffecient)
الانبعاثية (بالإنجليزية: Emissivity)
معامل التمدد الحراري (بالإنجليزية: Coeffecient of Thermal Expansion)
الحرارة النوعية (بالإنجليزية: Specific Heat)
حرارة التبخر (بالإنجليزية: Heat of Vaporization)
حرارة الانصهار (بالإنجليزية: Heat of Fusion)
تلقائية الاشتعال (بالإنجليزية: Pyrophoricity)
اشتعالية (بالإنجليزية: Flammability)
ضغط البخار (بالإنجليزية: Vapor Pressure)
درجة حرارة الاشتعال الذاتي (بالإنجليزية: Autoignition Temperature)
درجة الحرارة الحرجة (بالإنجليزية: Critical temperature)
درجة حرارة انتقال زجاجية (بالإنجليزية: Glass transition temperature)
مخطط اتزان الأطوار (بالإنجليزية: Phase diagram)
مخطط اتزان الأطوار الثنائي (بالإنجليزية: BINARY phase diagrams)
نقطة التصلد الحرج (بالإنجليزية: Eutectic point)
نقطة انصهار (بالإنجليزية: Melting point)
malaak jabr
وقد تكون خواص المادة رقما ثابتا وقد تتغير حسب متغير (مثل الحرارة) أو أكثر من متغير. وقد تتغير قيمة خواص المادة تبعا لاتجاه القياس وهو ما يعرف بـ تباينية الخواص. مثال على ذلك أن مغناطيسية بلورة في اتجاه المحور السيني قد تختلف عن مغناطيسيتها في اتجاه المحور الصادي.
وبالنسبة للخواص التي تربط بين ظاهرتين طبيعيتين فهي تتغير بشكل خطي أو شبه خطي خلال نطاق معين، فهي تعتبر قيمة ثابتة خلال هذا النطاق.
محتويات [أخف]
خواص فيزيائية[عدل]خواص ميكانيكية[عدل]معامل يونج (بالإنجليزية: Young's Modulus)
معامل المرونة النوعي (بالإنجليزية: Specific Modulus)
مقاومة الشد (بالإنجليزية: tensile strength)
مقاومة الانضغاط (بالإنجليزية: Compressive Strength)
مقاومة القص (بالإنجليزية: Shear Strength)
مقاومة الخضوع (بالإنجليزية: YIELD Strength)
المطيلية (بالإنجليزية: Ductility)
قابلية الطرق (بالإنجليزية: Malleability)
الانفعال عند الانهيار (بالإنجليزية: Strain at failure)
مؤشر التصليد بالانفعال (بالإنجليزية: Strain hardening INDEX)
الصلادة (بالإنجليزية: Hardness)
المتانة (بالإنجليزية: Toughness)
شدة تحمل صدمة (بالإنجليزية: Impact Toughness)
نسبة بواسون (بالإنجليزية: Poisson's ratio)
التصليدية (للمعادن) (بالإنجليزية: Hardenability)
قابلية اللحام (بالإنجليزية: Weldability)
حد الكلال أو حد التعب (بالإنجليزية: Fatigue Limit)
الكثافة (بالإنجليزية: Densiy)
اللزوجة (بالإنجليزية: Viscosity)
النفاذية (بالإنجليزية: Permeability)
المسامية (بالإنجليزية: Porosity)
السرعة الانفجارية (بالإنجليزية: Explosive Velocity)
مؤشر السريان عند الانصهار (بالإنجليزية: Melt Flow INDEX)
الثوابت الكهرضغطية (بالإنجليزية: Piezoelectric constants)
الرجوعية (بالإنجليزية: Resilience)
خواص كهربية[عدل]الموصلية الكهربائية أو الناقلية الكهربائية (بالإنجليزية: Electrical Conductivity)
السماحية (بالإنجليزية: Permitivity)
ثابت العازل (بالإنجليزية: Dielectric Constant)
شدة العزل (بالإنجليزية: Dielectric Strength)
الثوابت الكهرضغطية (بالإنجليزية: Piezoelectric Constants)
معامل سيبيك (بالإنجليزية: Seebeck coefficient)
خواص حرارية[عدل]الموصلية الحرارية (بالإنجليزية: Thermal Conductivity)
معامل الانتشار (بالإنجليزية: Diffusivity)
معامل سيبيك (بالإنجليزية: Seebeck Coeffecient)
الانبعاثية (بالإنجليزية: Emissivity)
معامل التمدد الحراري (بالإنجليزية: Coeffecient of Thermal Expansion)
الحرارة النوعية (بالإنجليزية: Specific Heat)
حرارة التبخر (بالإنجليزية: Heat of Vaporization)
حرارة الانصهار (بالإنجليزية: Heat of Fusion)
تلقائية الاشتعال (بالإنجليزية: Pyrophoricity)
اشتعالية (بالإنجليزية: Flammability)
ضغط البخار (بالإنجليزية: Vapor Pressure)
درجة حرارة الاشتعال الذاتي (بالإنجليزية: Autoignition Temperature)
درجة الحرارة الحرجة (بالإنجليزية: Critical temperature)
درجة حرارة انتقال زجاجية (بالإنجليزية: Glass transition temperature)
مخطط اتزان الأطوار (بالإنجليزية: Phase diagram)
مخطط اتزان الأطوار الثنائي (بالإنجليزية: BINARY phase diagrams)
نقطة التصلد الحرج (بالإنجليزية: Eutectic point)
نقطة انصهار (بالإنجليزية: Melting point)
malaak jabr
تغيرات المادة
خواص المادة وتغيراتها
يستغل الكيميائيون الخواص التي تميز المواد للتفريق بينها، فيمكن التفريق بين مجموعات المادة الواحدة بواسطة هذه الخواص. ويمكن استخدامها أيضا لتصنيف مادة مجهولة ضمن مجموعة من المواد. هناك خواص تعتمد على كمية المادة الموجودة كخواص الحجم والكتلة وكمية الطاقة، بينما هناك خواص لا تعتمد على كمية المادة الموجودة كدرجة الانصهار والغليان والكثافة والقدرة على توصيل الكهرباء والحرارة.
الخواص والتغيرات الفيزيائية للمادة
الخواص الفيزيائية هي صفات التي ترى وتقاس دون أن يحدث تغيير في هوية المادة، أي انها الصفات التي تتصف بها المادة نفسها وليس كيفية تحولها إلى مواد أخرى. التغيير الفيزيائي يكون في خواص المادة الفيزيائية دون أن يحولها إلى مادة أخرى، أي لا تغير في هوية المادة، إذ تبقى المادة كما هي. التغير في الحالة هو تغير فيزيائي يجعل المادة تتحول من حالة إلى أخرى.
الحالات الشائعة للمادة:
1. الحالة الصلبة.
2. الحالة السائلة.
3. الحالة الغازية.
الحالة الصلبة: الجسيمات التي تكونها تكون قريبة من بعضها مما يجعلها تتسم بحجم وشكل محددين. وبينما السبب الذي يجعلها ثابتة و تتذبذب فقط حول نقطة ثابتة هو أن قوى تجاذب الجسيمات قوية جدا
الحالة السائلة: تتسم فيها المادة بحجم محدد لكنها تفتقر إلى شكل محدد حيث أنها تتخذ شكل الوعاء إلى توضع فيه، وتتصف المادة السائلة بهذه الخواص لأن الجسيمات التي تكونها متقاربة، لكنها أكثر حركة من جسيمات المادة الصلبة.
الحالة الغازية: تفتقر المادة إلى شكل أو حجم محددين. وتتصف المادة بهذه الخواص نظرا إلى تباعد جسيمات حيث أن قوى التجاذب ضعيفة جدا.
أما الحالة الرابعة للمادة فهي البلازما: وهي الحالة الفيزيائية التي تنتج عن درجات الحرارة العالية، حيث تفقد الذرات إلكتروناتها.
#malaakjabr
ثقب الاوزون ومركبات ال CFCs |
malaak jabr
|
طبقة الأوزون[عدل]من ويكيبيديا، الموسوعة الحرة
صورة توضح دورة حياة الأوزون والأكسجين في طبقة الأوزون
طبقة الأوزون (Ozone layer) أو (Ozonsphere layer) هي جزء من الغلاف الجوي لكوكب الأرض والذي يحتوي بشكل مكثف غاز الأوزون. وهي متمركزة بشكل كبير في الجزء السفلي من طبقة الستراتوسفير من الغلاف الجوي للأرض وهي ذات لون أزرق.
يتحول فيها جزء من غاز الأوكسجين إلى غاز الأوزون بفعل الأشعة فوق البنفسجية القوية التي تصدرها الشمس وتؤثر في هذا الجزء من الغلاف الجوي نظرا لعدم وجود طبقات سميكة من الهواء فوقه لوقايته. ولهذه الطبقة أهمية حيوية بالنسبة لنا فهي تحول دون وصول الموجات فوق البنفسجية القصيرة بتركيز كبير إلى سطح الأرض.
اكتشف كل من شارل فابري وهنري بويسون طبقة الأوزون في 1913 وتم معرفة التفاصيل عنها من خلال غوردون دوبسون الذي قام بتطوير جهاز لقياس الأوزون الموجود في طبقة الستراتوسفير من سطح الأرض.
بين سنة 1928 و1958 قام دوبسون بعمل شبكة عالمية لمراقبة الأوزون والتي ما زالت تعمل حتى وقتنا هذا. وحدة قياس دوبسون, هي وحدة لقياس مجموع الأوزون في العامود، تم تسميتها تكريماً له.
الأشعة الفوق بنفسجية والأوزون[عدل]
رسم بياني يوضح مستويات الأوزون عند ارتفاعات مختلفة ومنع الأشعة فوق البنفسجية
دور طبقــة الأوزون: على الرغم من أن تركيز الأوزون في طبقة الأوزون قليل, إلا انه مهم بشكل كبير للحياة على الأرض, حيث انها تتسرب الأشعة فوق البنفسجية الضارة (UV) التي تطلقها الشمس. تم تصنيفها على حسب طول موجاتها إلى UV-A و UV-B و UV-C حيث تعتبر الأخيرة خطيرة جداً على البشر ويتم تنقيتها بشكل كامل من خلال الأوزون على ارتفاع 35 كيلومتر. مع ذلك يعتبر غاز الأوزون سام على ارتفاعات منخفضة حيث يسبب النزيف وغيرها.
من الممكن ان يؤدي تعرض الجلد لأشعة UV-B لاحتراقه (يظهر على شكل احمرار شديد); والتعرض الشديد له قد يؤدي إلى تغير في الشفرة الوراثية والتي تنتج عنها سرطان الجلد. مع ان طبقة الأوزون تمنع وصول الأشعة UV-B الا انه يصل بعضاً منها لسطح الأرض. معظم أشعة UV-A تصل الأرض وهي لا تضر بشكل كبير إلا انها من الممكن ان تسبب تغيير في الشفرة الوراثية أيضاً.
استنزاف طبقة الأوزون يسمح للأشعة فوق البنفسجية وتحديداً الأشعة ذات الموجات الأكثر ضررا أن تصل إلى سطح الأرض مما يؤدي إلى زيادة في احتمال حدوث تغييرات بالجينات الوراثية للأحياء على الأرض.
حساسية الحمض النووي للأشعة فوق البنفسجية[عدل]
مستويات طاقة الأشعة فوق البنفسجية عند ارتفاعات مختلفة, الخط الأزرق يوضح حساسية الحمض النووي (DNA). اللون الأحمر يوضح مستوى الطاقة عند انخفاض 10% بنسبة الاوزون
لتقدير أهمية الوقاية من الأشعة فوق البنفسجية, نستطيع خصائص الضرر من التعرض للإشعاع في طيف ضوئي (action spectrum), حيث يبين لنا تأثير الإشعاع البيولوجي حسب طول الموجات. من الممكن ان يكون التأثير حروق الجلد, تغير في نمو النبات أو تغيير في الحمض النووي (DNA). يتغير الضرر من التعرض للإشعاع على حسب طول الموجات. لحسن الحظ, يتغير تركيب الحمض النووي (DNA) بالموجات الأقل من 290 نانومتر والتي تقوم طبقة الأوزون بحجبها بشكل كبير. وفي الموجات الأطول التي يحجبها الاوزون بشكل بسيط لا يتضرر الحمض النووي بشكل كبير. لو قل الأوزون بنسبة 10%, سيتم التغيير بنسبة 22% في الحمض النووي من تأثير الأشعة الفوق بنفسجية. للعلم التغيير في الحمض النووي يؤدي الى أمراض مثل سرطان الجلد, وهذا يوضح أهمية طبقة الاوزون على حياتنا.
أيــن يتوزع الأوزون[عدل]
المتوسط الشهري العالمي لكمية الأوزون الإجمالية
سماكة الأوزون هي الكمية الإجمالية في عامود رأسي من الهواء وهي تختلف لأسباب كثيرة, حيث تكون اقل عند خط الاستواء وأكبر مع المرور عند القطبين. وهي تختلف أيضاً في المواسم, حيث تكون أكثر سماكة في فصل الربيع وأقل سماكة في فصل الخريف. والأسباب لذلك معقدة, يتضمن ذلك دورة الغلاف الجوي وقوة الشمس.
بما أن الأوزون الموجود في طبقة الستراتوسفير تنتج بسبب الأشعة الفوق البنفسجية الصادرة من اشعة الشمس, لذلك من المتوقع ان تكون أعلى مستويات الأوزون عند خط الاستواء وأقلها عن القطبين ولنفس السبب من الممكن الاستنتاج ان أعلى مستويات الأوزون في الصيف واقلها في الشتاء. غير أن ذلك غير صحيح حيث أن أعلى مستويات الأوزون متواجدة في القطبين الشمالي والجنوبي كما تكون أعلى في فصل الربيع وليس في الصيف, واقلها في فصل الخريف وليس الشتاء. خلال فصل الشتاء, تزداد سماكة طبقة الاوزون. تم تفسير هذه الأحجية من خلال دورة الرياح في طبقة الستراتوسفير والمعروفة بدورة بروير-دوبسون (). معظم الأوزون يتم إنتاجه فوق القطبين وتقوم دورة الرياح في طبقة الستراتوسفير من عند القطبين بإتجاه وبالعكس إلى ارتفاع اقل في طبقة الستراتوسفير.
دورة بروير - دوبسون في طبقة الاوزون
طيقة الأوزون أكثر ارتفاعاً عند خط الاستواء وأقل انخفاضاً عند الابتعاد عن خط الاستواء, خصوصاً عند منطقة القطبين. تنوع الارتفاع في الأوزون سببه بطئ دورة الهواء التي ترفع الأوزون من طبقة الترابوسفير إلى الستراتوسفير.
كلما ابتعدنا عن خط الاستواء زادت سماكة الأوزون بإتجاه القطبين, بشكل عام كمية الأوزون الموجودة في القطب الشمالي أكثر منها في الجنوبي. بالإضافة إلى ذلك, تكون سماكة الأوزون في القطب الشمالي أكبر في فصل الربيع (مارس - أبريل) منها في القطب الجنوبي بينما تكون في القطب الجنوبي أكبر في فصل الخريف (سبتمبر - أكتوبر) منها في القطب الشمالي في نفس الفترة. في الواقع أكبر كميات الأوزون في جميع أنحاء العالم توجد في القطب الشمالي خلال فترة الربيع وفي خلال الفترة نفسها تكون أقل كميات الأوزون في جميع أنحاء العالم توجد في القطب الجنوبي خلال فترة الربيع بالقطب الجنوبي بشهري سبتمبر وأكتوبر وذلك بسبب ظاهرة ثقب الأوزون.
استنزاف الأوزون[عدل]من الممكن استنزاف طبقة الأو هيدروكسيل (OH), غاز الكلور (Cl) وغاز البرومين (Br). حيث يوجد مصادر طبيعية لجميع العناصر المذكورة, إلا أن تركيز غاز الكلور وغاز البرومين قد ارتفع بشكل ملحوظ في السنوات الأخيرة وذلك بسبب إنتاج البشر لبعض المواد المركبة خصوصاً كلوروفلوروكربون (chlorofluorocarbon) والتي تعرف اختصاراً باسم (CFCs) وأيضاً بروموفلوروكربون.
هذه المركبات المستقرة كيميائية تستطيع ان تصل إلى طبقة الستراتوسفير حيث تعمل الأشعة فوق البنفسجية على تفكيك كل من الكلور والفلور.. يبدأ كل منهم بتحفيز سلسلة من التفاعل القادرة على تفكيك أكثر من 100,000 جزئ أوزون. الاوزون في الجزء الشمالي من الكرة الأرضية في انخفاض 4% كل عقد. تقريباً أكثر من 5% من سطح الأرض حول القطب الشمالي والقطب الجنوبي, أكثر (لكن بشكل موسمي) قد ينخفض; وهذا ما يسمى بـ ثقب الأوزون.
مـا هـي الحلـول المقترحـة للتقليل من استنزاف الأوزون[عدل]السويد هي أول دولة تمنع استخدام الرشاشات (مثل المبيدات الحشرية) التي تقضي علي الحشرات ولكنها تحتوي على كلوروفلوروكربون (CFC) الذي يعمل علي تاكل طبقة الاوزون في 23 يناير, 1978. تلتها بعض الدول مثل الولايات المتحدة الأمريكية, كندا والنرويج. وقد منعت المجموعة الأوروبية اقتراح مشابه. حتى في الولايات المتحدة, ما زال غاز كلوروفلوروكربون يستخدم في أماكن أخرى مثل الثلاجات والمنظفات الصناعية حتى بعد اكتشاف ثقب طبقة الأوزون بالقطب الجنوبي في سنة 1985. بعد محادثات ومعاهدة دولية (بروتوكول مونتريال), تم وقف إنتاج كلوروفلوروكربون (CFC) بشكل كبير ابتداً من 1987 وبشكل كامل في عام 1996.
في 2 اغسطس 2003, قام العلماء بالإعلان ان استنزاف طبقة الأوزون قد بدأ يتباطأ بعد حظر استخدام الكلوروفلوروكربون (CFC).
ثلاث أقمار اصطناعية وثلاث محطات ارضية اثبتت بطئ استنزاف طبقة الأوزون العليا بشكل كبير خلال العقد الماضي. تمت الدراسة من خلال منظمة الإتحاد الجيوفيزيائي الأمريكي (American Geophysical Union). بعض الانحلال ما زال قائم في طبقة الأوزون بسبب عدم قيام بعض الدول بمنع استخدام الكلوروفلوروكربون (CFC) بالإضافة إلى وجوده مسبقاً في طبقة الستراتوسفير قبل منع استخدامه, حيث له فترة انحلال طويلة من 50 إلى أكثر من 100 سنة, ولذلك تحتاج طبقة الأوزون لرجوعها بشكل كامل لعدة عقود.
حالياً يتم تركيب مكونات تحتوي على (C-H) لتحل كبديل لاستخدام الكلوروفلوروكربون (CFC) مثل هايدروكوروفلوروكربون (HCFC), حيث ان هذه المركبات أكثر نشاط ولحسن الحظ لا تبقى فترة كافية في الغلاف الجوي لتصل إلى طبقة الستراتوسفير حيث تؤثر على طبقة الأوزون.http://ar.wikipedia.org/wiki/%D8%B7%D8%A8%D9%82%D8%A9_%D8%A7%D9%84%D8%A3%D9%88%D8%B2%D9%88%D9%86
malaak jabr
صورة توضح دورة حياة الأوزون والأكسجين في طبقة الأوزون
طبقة الأوزون (Ozone layer) أو (Ozonsphere layer) هي جزء من الغلاف الجوي لكوكب الأرض والذي يحتوي بشكل مكثف غاز الأوزون. وهي متمركزة بشكل كبير في الجزء السفلي من طبقة الستراتوسفير من الغلاف الجوي للأرض وهي ذات لون أزرق.
يتحول فيها جزء من غاز الأوكسجين إلى غاز الأوزون بفعل الأشعة فوق البنفسجية القوية التي تصدرها الشمس وتؤثر في هذا الجزء من الغلاف الجوي نظرا لعدم وجود طبقات سميكة من الهواء فوقه لوقايته. ولهذه الطبقة أهمية حيوية بالنسبة لنا فهي تحول دون وصول الموجات فوق البنفسجية القصيرة بتركيز كبير إلى سطح الأرض.
اكتشف كل من شارل فابري وهنري بويسون طبقة الأوزون في 1913 وتم معرفة التفاصيل عنها من خلال غوردون دوبسون الذي قام بتطوير جهاز لقياس الأوزون الموجود في طبقة الستراتوسفير من سطح الأرض.
بين سنة 1928 و1958 قام دوبسون بعمل شبكة عالمية لمراقبة الأوزون والتي ما زالت تعمل حتى وقتنا هذا. وحدة قياس دوبسون, هي وحدة لقياس مجموع الأوزون في العامود، تم تسميتها تكريماً له.
الأشعة الفوق بنفسجية والأوزون[عدل]
رسم بياني يوضح مستويات الأوزون عند ارتفاعات مختلفة ومنع الأشعة فوق البنفسجية
دور طبقــة الأوزون: على الرغم من أن تركيز الأوزون في طبقة الأوزون قليل, إلا انه مهم بشكل كبير للحياة على الأرض, حيث انها تتسرب الأشعة فوق البنفسجية الضارة (UV) التي تطلقها الشمس. تم تصنيفها على حسب طول موجاتها إلى UV-A و UV-B و UV-C حيث تعتبر الأخيرة خطيرة جداً على البشر ويتم تنقيتها بشكل كامل من خلال الأوزون على ارتفاع 35 كيلومتر. مع ذلك يعتبر غاز الأوزون سام على ارتفاعات منخفضة حيث يسبب النزيف وغيرها.
من الممكن ان يؤدي تعرض الجلد لأشعة UV-B لاحتراقه (يظهر على شكل احمرار شديد); والتعرض الشديد له قد يؤدي إلى تغير في الشفرة الوراثية والتي تنتج عنها سرطان الجلد. مع ان طبقة الأوزون تمنع وصول الأشعة UV-B الا انه يصل بعضاً منها لسطح الأرض. معظم أشعة UV-A تصل الأرض وهي لا تضر بشكل كبير إلا انها من الممكن ان تسبب تغيير في الشفرة الوراثية أيضاً.
استنزاف طبقة الأوزون يسمح للأشعة فوق البنفسجية وتحديداً الأشعة ذات الموجات الأكثر ضررا أن تصل إلى سطح الأرض مما يؤدي إلى زيادة في احتمال حدوث تغييرات بالجينات الوراثية للأحياء على الأرض.
حساسية الحمض النووي للأشعة فوق البنفسجية[عدل]
مستويات طاقة الأشعة فوق البنفسجية عند ارتفاعات مختلفة, الخط الأزرق يوضح حساسية الحمض النووي (DNA). اللون الأحمر يوضح مستوى الطاقة عند انخفاض 10% بنسبة الاوزون
لتقدير أهمية الوقاية من الأشعة فوق البنفسجية, نستطيع خصائص الضرر من التعرض للإشعاع في طيف ضوئي (action spectrum), حيث يبين لنا تأثير الإشعاع البيولوجي حسب طول الموجات. من الممكن ان يكون التأثير حروق الجلد, تغير في نمو النبات أو تغيير في الحمض النووي (DNA). يتغير الضرر من التعرض للإشعاع على حسب طول الموجات. لحسن الحظ, يتغير تركيب الحمض النووي (DNA) بالموجات الأقل من 290 نانومتر والتي تقوم طبقة الأوزون بحجبها بشكل كبير. وفي الموجات الأطول التي يحجبها الاوزون بشكل بسيط لا يتضرر الحمض النووي بشكل كبير. لو قل الأوزون بنسبة 10%, سيتم التغيير بنسبة 22% في الحمض النووي من تأثير الأشعة الفوق بنفسجية. للعلم التغيير في الحمض النووي يؤدي الى أمراض مثل سرطان الجلد, وهذا يوضح أهمية طبقة الاوزون على حياتنا.
أيــن يتوزع الأوزون[عدل]
المتوسط الشهري العالمي لكمية الأوزون الإجمالية
سماكة الأوزون هي الكمية الإجمالية في عامود رأسي من الهواء وهي تختلف لأسباب كثيرة, حيث تكون اقل عند خط الاستواء وأكبر مع المرور عند القطبين. وهي تختلف أيضاً في المواسم, حيث تكون أكثر سماكة في فصل الربيع وأقل سماكة في فصل الخريف. والأسباب لذلك معقدة, يتضمن ذلك دورة الغلاف الجوي وقوة الشمس.
بما أن الأوزون الموجود في طبقة الستراتوسفير تنتج بسبب الأشعة الفوق البنفسجية الصادرة من اشعة الشمس, لذلك من المتوقع ان تكون أعلى مستويات الأوزون عند خط الاستواء وأقلها عن القطبين ولنفس السبب من الممكن الاستنتاج ان أعلى مستويات الأوزون في الصيف واقلها في الشتاء. غير أن ذلك غير صحيح حيث أن أعلى مستويات الأوزون متواجدة في القطبين الشمالي والجنوبي كما تكون أعلى في فصل الربيع وليس في الصيف, واقلها في فصل الخريف وليس الشتاء. خلال فصل الشتاء, تزداد سماكة طبقة الاوزون. تم تفسير هذه الأحجية من خلال دورة الرياح في طبقة الستراتوسفير والمعروفة بدورة بروير-دوبسون (). معظم الأوزون يتم إنتاجه فوق القطبين وتقوم دورة الرياح في طبقة الستراتوسفير من عند القطبين بإتجاه وبالعكس إلى ارتفاع اقل في طبقة الستراتوسفير.
دورة بروير - دوبسون في طبقة الاوزون
طيقة الأوزون أكثر ارتفاعاً عند خط الاستواء وأقل انخفاضاً عند الابتعاد عن خط الاستواء, خصوصاً عند منطقة القطبين. تنوع الارتفاع في الأوزون سببه بطئ دورة الهواء التي ترفع الأوزون من طبقة الترابوسفير إلى الستراتوسفير.
كلما ابتعدنا عن خط الاستواء زادت سماكة الأوزون بإتجاه القطبين, بشكل عام كمية الأوزون الموجودة في القطب الشمالي أكثر منها في الجنوبي. بالإضافة إلى ذلك, تكون سماكة الأوزون في القطب الشمالي أكبر في فصل الربيع (مارس - أبريل) منها في القطب الجنوبي بينما تكون في القطب الجنوبي أكبر في فصل الخريف (سبتمبر - أكتوبر) منها في القطب الشمالي في نفس الفترة. في الواقع أكبر كميات الأوزون في جميع أنحاء العالم توجد في القطب الشمالي خلال فترة الربيع وفي خلال الفترة نفسها تكون أقل كميات الأوزون في جميع أنحاء العالم توجد في القطب الجنوبي خلال فترة الربيع بالقطب الجنوبي بشهري سبتمبر وأكتوبر وذلك بسبب ظاهرة ثقب الأوزون.
استنزاف الأوزون[عدل]من الممكن استنزاف طبقة الأو هيدروكسيل (OH), غاز الكلور (Cl) وغاز البرومين (Br). حيث يوجد مصادر طبيعية لجميع العناصر المذكورة, إلا أن تركيز غاز الكلور وغاز البرومين قد ارتفع بشكل ملحوظ في السنوات الأخيرة وذلك بسبب إنتاج البشر لبعض المواد المركبة خصوصاً كلوروفلوروكربون (chlorofluorocarbon) والتي تعرف اختصاراً باسم (CFCs) وأيضاً بروموفلوروكربون.
هذه المركبات المستقرة كيميائية تستطيع ان تصل إلى طبقة الستراتوسفير حيث تعمل الأشعة فوق البنفسجية على تفكيك كل من الكلور والفلور.. يبدأ كل منهم بتحفيز سلسلة من التفاعل القادرة على تفكيك أكثر من 100,000 جزئ أوزون. الاوزون في الجزء الشمالي من الكرة الأرضية في انخفاض 4% كل عقد. تقريباً أكثر من 5% من سطح الأرض حول القطب الشمالي والقطب الجنوبي, أكثر (لكن بشكل موسمي) قد ينخفض; وهذا ما يسمى بـ ثقب الأوزون.
مـا هـي الحلـول المقترحـة للتقليل من استنزاف الأوزون[عدل]السويد هي أول دولة تمنع استخدام الرشاشات (مثل المبيدات الحشرية) التي تقضي علي الحشرات ولكنها تحتوي على كلوروفلوروكربون (CFC) الذي يعمل علي تاكل طبقة الاوزون في 23 يناير, 1978. تلتها بعض الدول مثل الولايات المتحدة الأمريكية, كندا والنرويج. وقد منعت المجموعة الأوروبية اقتراح مشابه. حتى في الولايات المتحدة, ما زال غاز كلوروفلوروكربون يستخدم في أماكن أخرى مثل الثلاجات والمنظفات الصناعية حتى بعد اكتشاف ثقب طبقة الأوزون بالقطب الجنوبي في سنة 1985. بعد محادثات ومعاهدة دولية (بروتوكول مونتريال), تم وقف إنتاج كلوروفلوروكربون (CFC) بشكل كبير ابتداً من 1987 وبشكل كامل في عام 1996.
في 2 اغسطس 2003, قام العلماء بالإعلان ان استنزاف طبقة الأوزون قد بدأ يتباطأ بعد حظر استخدام الكلوروفلوروكربون (CFC).
ثلاث أقمار اصطناعية وثلاث محطات ارضية اثبتت بطئ استنزاف طبقة الأوزون العليا بشكل كبير خلال العقد الماضي. تمت الدراسة من خلال منظمة الإتحاد الجيوفيزيائي الأمريكي (American Geophysical Union). بعض الانحلال ما زال قائم في طبقة الأوزون بسبب عدم قيام بعض الدول بمنع استخدام الكلوروفلوروكربون (CFC) بالإضافة إلى وجوده مسبقاً في طبقة الستراتوسفير قبل منع استخدامه, حيث له فترة انحلال طويلة من 50 إلى أكثر من 100 سنة, ولذلك تحتاج طبقة الأوزون لرجوعها بشكل كامل لعدة عقود.
حالياً يتم تركيب مكونات تحتوي على (C-H) لتحل كبديل لاستخدام الكلوروفلوروكربون (CFC) مثل هايدروكوروفلوروكربون (HCFC), حيث ان هذه المركبات أكثر نشاط ولحسن الحظ لا تبقى فترة كافية في الغلاف الجوي لتصل إلى طبقة الستراتوسفير حيث تؤثر على طبقة الأوزون.http://ar.wikipedia.org/wiki/%D8%B7%D8%A8%D9%82%D8%A9_%D8%A7%D9%84%D8%A3%D9%88%D8%B2%D9%88%D9%86
malaak jabr
#bassant
الطريقة العلمية في البحث "
تمكّن المتعلّمين من امتلاك أداة قويّة وفاعلة لخوض غمار دراسة الكيمياء . تُعرّف " الطريقة العلمية في البحث " بأنّها نظرة منظّمة أو منحى منظّم للبحث (A systematic approach to research ) ويتمّ فيها معالجة منطقية لمشكلة تواجه المتعلّم عبر ثلاث خطوات رئيسة :
الأولى : لاحظ المشكلة .
الثانية : ضع افتراضات لحلّ المشكلة .
الثالثة : اختبر هذه الافتراضات وتوصّل إلى الحلّ .
يُقصد بالمشكلة هنا الظاهرة أو موضوع البحث وليس بالضرورة أن تكون مشكلة بالمعنى المتعارف عليه . ويبدوا للوهلة الأولى أنّ القيام بعملية الملاحظة ( Observations ) أمرٌ سهل ، والحقيقة غيرُ ذلك ، فالملاحظة العلمية تتطلّب توفّر مجموعة من المهارات لدى المتعلّم ، فهي إمّا أن تكون ملاحظة عشوائية أو منظمّة ، مقصودة أو غير مقصودة ، كيفية أو كمّية ، وبالطبع فإنّ الملاحظة التي نحتاجها في طريقة البحث العلمي هي الملاحظة المنظّمة المقصودة والمخطط لها .
وتتبع الملاحظة في الخطوة الثانية عملية افتراض الفرضيات ( Hypothesis ) وهي عبارة عن تفسيرات تجريبية لمجموعة الملاحظات والتي يمكن صياغتها على شكل عبارات تقريرية أو تساؤلات . وفي الثالثة تأتي مرحلة اختبار هذه الفرضيات ( Experiment to Test Hypothesis )للوصول إلى نتيجة كحلّ نهائي للمشكلة .
لنضرب مثالاً على ذلك :
الملاحظة : المحلّ ( أ) لبيع القهوة قهوته أجود وألذّ من القهوة في المحلّ ( ب ) ، ولكن المحلّ ( ب ) أرخص سعراً من المحلّ ( أ ) ، وبالرغم من أنّ طلاّب الجامعة يفضلّون القهوة التي في المحلّ ( أ ) إلاّ أنّهم يحتسون القهوة في المحل ( ب ) أكثر. الافتراض : كلفة القهوة أكثر أهمّية من جودتها ومذاقها لدى معظم طلاّب الجامعة . التجريب : نخفّض سعر القهوة في المحل ( أ ) وننظر هل يتجّه طلاّب الجامعة إليه أكثر . لو تحوّل طلاّب الجامعة إلى المحلّ ( أ ) بأعداد أكبرفمعنى هذا أنّ الافتراض صحيح .
.طبقة الأوزون
هي جزء من الغلاف الجوي لكوكب الأرض والذي يحتوي بشكل مكثف غاز الأوزون. وهي متمركزة بشكل كبير في الجزء السفلي من طبقة الستراتوسفير من الغلاف الجوي للأرض وهي ذات لون أزرق.
يتحول فيها جزء من غاز الأوكسجين إلى غاز الأوزون بفعل الأشعة فوق البنفسجية القوية التي تصدرها الشمس وتؤثر في هذا الجزء من الغلاف الجوي نظرا لعدم وجود طبقات سميكة من الهواء فوقه لوقايته. ولهذه الطبقة أهمية حيوية بالنسبة لنا فهي تحول دون وصول الموجات فوق البنفسجية القصيرة بتركيز كبير إلى سطح الأرض.
اكتشف كل من شارل فابري وهنري بويسون طبقة الأوزون في 1913 وتم معرفة التفاصيل عنها من خلال غوردون دوبسون الذي قام بتطوير جهاز لقياس الأوزون الموجود في طبقة الستراتوسفير من سطح الأرض.
بين سنة 1928 و1958 قام دوبسون بعمل شبكة عالمية لمراقبة الأوزون والتي ما زالت تعمل حتى وقتنا هذا. وحدة قياس دوبسون, هي وحدة لقياس مجموع
الأوزون في العامود، تم تسميتها تكريماً له.
razan madi
هي جزء من الغلاف الجوي لكوكب الأرض والذي يحتوي بشكل مكثف غاز الأوزون. وهي متمركزة بشكل كبير في الجزء السفلي من طبقة الستراتوسفير من الغلاف الجوي للأرض وهي ذات لون أزرق.
يتحول فيها جزء من غاز الأوكسجين إلى غاز الأوزون بفعل الأشعة فوق البنفسجية القوية التي تصدرها الشمس وتؤثر في هذا الجزء من الغلاف الجوي نظرا لعدم وجود طبقات سميكة من الهواء فوقه لوقايته. ولهذه الطبقة أهمية حيوية بالنسبة لنا فهي تحول دون وصول الموجات فوق البنفسجية القصيرة بتركيز كبير إلى سطح الأرض.
اكتشف كل من شارل فابري وهنري بويسون طبقة الأوزون في 1913 وتم معرفة التفاصيل عنها من خلال غوردون دوبسون الذي قام بتطوير جهاز لقياس الأوزون الموجود في طبقة الستراتوسفير من سطح الأرض.
بين سنة 1928 و1958 قام دوبسون بعمل شبكة عالمية لمراقبة الأوزون والتي ما زالت تعمل حتى وقتنا هذا. وحدة قياس دوبسون, هي وحدة لقياس مجموع
الأوزون في العامود، تم تسميتها تكريماً له.
razan madi
إكتشاف الأوزون
تم اكتشاف غاز الأوزون و قياس كميته في أواخر القرن التاسع عشر و قد أثار اهتمام العلماء فهو يتكون فوق خط الاستواء لأن أشعة الشمس عمودية و قوية هناك ثم يتحرك حول الأرض بفعل تيارات الهواء في الستراتوسفير لذا يعد مؤشرا مناسبا يساعدنا على تتبع حركة الرياح في طبقة الستراتوسفير
SALMA MUSADDI
تم اكتشاف غاز الأوزون و قياس كميته في أواخر القرن التاسع عشر و قد أثار اهتمام العلماء فهو يتكون فوق خط الاستواء لأن أشعة الشمس عمودية و قوية هناك ثم يتحرك حول الأرض بفعل تيارات الهواء في الستراتوسفير لذا يعد مؤشرا مناسبا يساعدنا على تتبع حركة الرياح في طبقة الستراتوسفير
SALMA MUSADDI
النظريات القديمة للمادة
هناك نظريات قديمه للماده وبدياتها كانت من فلاسفة الاغريق واشهر هؤلاء العلماء هم
دمقريطس والذي عاش بين (370-460) قبل الميلاد وكان يعتقد ان الماده: 1-ان الماده مكونه من اجزاء صغيره وتسمى الذرات 2-ان الماده صلبه، متجانسه، غير قابله للانقسام 3-الأنواع المختلفه من الذرات لها احجام واشكال مختلفة 4-حجم الذرات وشكلها وحركتها يحدد خواص الماده
ولكن أرسطو الذي عاش بين (322-384) قبل الميلاد انتقد ورفض فكرة الذرات لانها لاتتوفق مع افكاره حول الطبيعه وكانت أهم انتقاداته تتعلق بفكرة ان الذرات تتحرك بالفراغ
وكان اعتقاد أرسطو هو: 1-لاوجو للفراغ 2-الماده مكونه من ما، تراب، هواء,نار
أما جون دالتون الذي عاش بين (1766-1844)م كان لديه ستة نظريات أربع منها صحيحة وهي: 1-تتكون المادة منأجزاء صغيرة جداً تسمى الذرات. 2-تختلف ذرات أي عنصر من ذرات العناصر الأخرى. 3-الذرات المختلفة تتحد بنسبة عددية بسيطة لتكوين المركبات. 4-في التفاعلات الكيميائية:تنفصل الذرات,أو تتحد,أو يعاد ترتيبها. وإثنتان منها خاطئة وهي: 1-أن الذرات لا يمكن تجزئتهاوالسبب في أنها خاطئة أنه يمكن تجزئة الذرات إلى جسيمات ذرية. 2-أن جميع الذرات المكون للعنصر لها خواص متماثلة,والخطأ في هذه النظرية أن ذرات العنصر الواحد يمكن أن تختلف بشكل بسيط في كتلتها
razan madi.
هناك نظريات قديمه للماده وبدياتها كانت من فلاسفة الاغريق واشهر هؤلاء العلماء هم
دمقريطس والذي عاش بين (370-460) قبل الميلاد وكان يعتقد ان الماده: 1-ان الماده مكونه من اجزاء صغيره وتسمى الذرات 2-ان الماده صلبه، متجانسه، غير قابله للانقسام 3-الأنواع المختلفه من الذرات لها احجام واشكال مختلفة 4-حجم الذرات وشكلها وحركتها يحدد خواص الماده
ولكن أرسطو الذي عاش بين (322-384) قبل الميلاد انتقد ورفض فكرة الذرات لانها لاتتوفق مع افكاره حول الطبيعه وكانت أهم انتقاداته تتعلق بفكرة ان الذرات تتحرك بالفراغ
وكان اعتقاد أرسطو هو: 1-لاوجو للفراغ 2-الماده مكونه من ما، تراب، هواء,نار
أما جون دالتون الذي عاش بين (1766-1844)م كان لديه ستة نظريات أربع منها صحيحة وهي: 1-تتكون المادة منأجزاء صغيرة جداً تسمى الذرات. 2-تختلف ذرات أي عنصر من ذرات العناصر الأخرى. 3-الذرات المختلفة تتحد بنسبة عددية بسيطة لتكوين المركبات. 4-في التفاعلات الكيميائية:تنفصل الذرات,أو تتحد,أو يعاد ترتيبها. وإثنتان منها خاطئة وهي: 1-أن الذرات لا يمكن تجزئتهاوالسبب في أنها خاطئة أنه يمكن تجزئة الذرات إلى جسيمات ذرية. 2-أن جميع الذرات المكون للعنصر لها خواص متماثلة,والخطأ في هذه النظرية أن ذرات العنصر الواحد يمكن أن تختلف بشكل بسيط في كتلتها
razan madi.
تغيرات المادة
خواص المادة وتغيراتها
يستغل الكيميائيون الخواص التي تميز المواد للتفريق بينها، فيمكن التفريق بين مجموعات المادة الواحدة بواسطة هذه الخواص. ويمكن استخدامها أيضا لتصنيف مادة مجهولة ضمن مجموعة من المواد. هناك خواص تعتمد على كمية المادة الموجودة كخواص الحجم والكتلة وكمية الطاقة، بينما هناك خواص لا تعتمد على كمية المادة الموجودة كدرجة الانصهار والغليان والكثافة والقدرة على توصيل الكهرباء والحرارة.
الخواص والتغيرات الفيزيائية للمادة
الخواص الفيزيائية هي صفات التي ترى وتقاس دون أن يحدث تغيير في هوية المادة، أي انها الصفات التي تتصف بها المادة نفسها وليس كيفية تحولها إلى مواد أخرى. التغيير الفيزيائي يكون في خواص المادة الفيزيائية دون أن يحولها إلى مادة أخرى، أي لا تغير في هوية المادة، إذ تبقى المادة كما هي. التغير في الحالة هو تغير فيزيائي يجعل المادة تتحول من حالة إلى أخرى.
الحالات الشائعة للمادة:
1. الحالة الصلبة.
2. الحالة السائلة.
3. الحالة الغازية.
الحالة الصلبة: الجسيمات التي تكونها تكون قريبة من بعضها مما يجعلها تتسم بحجم وشكل محددين. وبينما السبب الذي يجعلها ثابتة و تتذبذب فقط حول نقطة ثابتة هو أن قوى تجاذب الجسيمات قوية جدا
الحالة السائلة: تتسم فيها المادة بحجم محدد لكنها تفتقر إلى شكل محدد حيث أنها تتخذ شكل الوعاء إلى توضع فيه، وتتصف المادة السائلة بهذه الخواص لأن الجسيمات التي تكونها متقاربة، لكنها أكثر حركة من جسيمات المادة الصلبة.
الحالة الغازية: تفتقر المادة إلى شكل أو حجم محددين. وتتصف المادة بهذه الخواص نظرا إلى تباعد جسيمات حيث أن قوى التجاذب ضعيفة جدا.
أما الحالة الرابعة للمادة فهي البلازما: وهي الحالة الفيزيائية التي تنتج عن درجات الحرارة العالية، حيث تفقد الذرات إلكتروناتها.
shooq
يستغل الكيميائيون الخواص التي تميز المواد للتفريق بينها، فيمكن التفريق بين مجموعات المادة الواحدة بواسطة هذه الخواص. ويمكن استخدامها أيضا لتصنيف مادة مجهولة ضمن مجموعة من المواد. هناك خواص تعتمد على كمية المادة الموجودة كخواص الحجم والكتلة وكمية الطاقة، بينما هناك خواص لا تعتمد على كمية المادة الموجودة كدرجة الانصهار والغليان والكثافة والقدرة على توصيل الكهرباء والحرارة.
الخواص والتغيرات الفيزيائية للمادة
الخواص الفيزيائية هي صفات التي ترى وتقاس دون أن يحدث تغيير في هوية المادة، أي انها الصفات التي تتصف بها المادة نفسها وليس كيفية تحولها إلى مواد أخرى. التغيير الفيزيائي يكون في خواص المادة الفيزيائية دون أن يحولها إلى مادة أخرى، أي لا تغير في هوية المادة، إذ تبقى المادة كما هي. التغير في الحالة هو تغير فيزيائي يجعل المادة تتحول من حالة إلى أخرى.
الحالات الشائعة للمادة:
1. الحالة الصلبة.
2. الحالة السائلة.
3. الحالة الغازية.
الحالة الصلبة: الجسيمات التي تكونها تكون قريبة من بعضها مما يجعلها تتسم بحجم وشكل محددين. وبينما السبب الذي يجعلها ثابتة و تتذبذب فقط حول نقطة ثابتة هو أن قوى تجاذب الجسيمات قوية جدا
الحالة السائلة: تتسم فيها المادة بحجم محدد لكنها تفتقر إلى شكل محدد حيث أنها تتخذ شكل الوعاء إلى توضع فيه، وتتصف المادة السائلة بهذه الخواص لأن الجسيمات التي تكونها متقاربة، لكنها أكثر حركة من جسيمات المادة الصلبة.
الحالة الغازية: تفتقر المادة إلى شكل أو حجم محددين. وتتصف المادة بهذه الخواص نظرا إلى تباعد جسيمات حيث أن قوى التجاذب ضعيفة جدا.
أما الحالة الرابعة للمادة فهي البلازما: وهي الحالة الفيزيائية التي تنتج عن درجات الحرارة العالية، حيث تفقد الذرات إلكتروناتها.
shooq
ذرة
الذرة هي أصغر جزء من العنصر الكيميائي الذي يحتفظ بالخصائص الكيميائية لذلك العنصر. يرجع أصل الكلمة الإنجليزية (بالإنجليزية
: Atom) إلى الكلمة الإغريقيةأتوموس، وتعني غير القابل للانقسام؛ إذ كان يعتقد أنه ليس ثمة ما هو أصغر من الذرة. تتكون الذرة من سحابة من الشحنات السالبة (الإلكترونات) تحوم حول نواة موجبة الشحنة صغيرة جدا في الوسط. تتكون النواة الموجبة هذه من بروتونات موجبة الشحنة، ونيوترونات متعادلة. الذرة هي أصغر جزء من العنصر يمكن أن يتميز به عن بقية العناصر؛ إذ كلما غصنا أكثر في المادة لنلاقي البنى الأصغر لن يعود هناك فرق بين عنصر وآخر. فمثلاً، لا فرق بين بروتون في ذرة حديد وبروتون آخر في ذرة يورانيوم مثلاً، أو ذرة أي عنصر آخر. الذرة، بما تحمله من خصائص؛ عدد بروتوناتها، كتلتها، توزيعها الإلكتروني...، تصنع الفروقات بين العناصر المختلفة، وبين الصور المختلفة للعنصر نفسه (المسماة بالنظائر)، وحتى بين كون هذا العنصر قادراً على خوض تفاعل كيميائي ما أم لا.
ظل تركيب الذرة وما يجري في هذا العالم البالغ الصغر، ظل وما زال يشغل العلماء ويدفعهم إلى اكتشاف المزيد. ومن هنا أخذت تظهر فروع جديدة في العلم حاملة معها مبادئها ونظرياتها الخاصة بها، بدءاً بمبدأ عدم التأكد (اللاثقة)، مروراً بنظريات التوحيد الكبرى، وانتهاءً بنظرية الأوتار الفائقة.
: Atom) إلى الكلمة الإغريقيةأتوموس، وتعني غير القابل للانقسام؛ إذ كان يعتقد أنه ليس ثمة ما هو أصغر من الذرة. تتكون الذرة من سحابة من الشحنات السالبة (الإلكترونات) تحوم حول نواة موجبة الشحنة صغيرة جدا في الوسط. تتكون النواة الموجبة هذه من بروتونات موجبة الشحنة، ونيوترونات متعادلة. الذرة هي أصغر جزء من العنصر يمكن أن يتميز به عن بقية العناصر؛ إذ كلما غصنا أكثر في المادة لنلاقي البنى الأصغر لن يعود هناك فرق بين عنصر وآخر. فمثلاً، لا فرق بين بروتون في ذرة حديد وبروتون آخر في ذرة يورانيوم مثلاً، أو ذرة أي عنصر آخر. الذرة، بما تحمله من خصائص؛ عدد بروتوناتها، كتلتها، توزيعها الإلكتروني...، تصنع الفروقات بين العناصر المختلفة، وبين الصور المختلفة للعنصر نفسه (المسماة بالنظائر)، وحتى بين كون هذا العنصر قادراً على خوض تفاعل كيميائي ما أم لا.
ظل تركيب الذرة وما يجري في هذا العالم البالغ الصغر، ظل وما زال يشغل العلماء ويدفعهم إلى اكتشاف المزيد. ومن هنا أخذت تظهر فروع جديدة في العلم حاملة معها مبادئها ونظرياتها الخاصة بها، بدءاً بمبدأ عدم التأكد (اللاثقة)، مروراً بنظريات التوحيد الكبرى، وانتهاءً بنظرية الأوتار الفائقة.
رسم توضيحي لذرة الهيليوم, يصور النواة (بالوردي) وتوزيع السحابة الإلكترونية (بالأسود). النواة (أعلى اليمين) في الهليوم-4 في الواقع متماثلة كرويًا وتشبه إلى حد كبير السحابة الإلكترونية، على الرغم من أن الأنوية أكثر تعقيدًا وهذا ليس الحال دائما. الشريط الأسود هو أنغستروم واحد (10−10 مأو 100 بيكومتر).
تعريف أصغر قسم معترف به من العنصر الكيميائي
الخصائص
الوزن الشامل:1.67×10−27 إلى 4.52×10−25 كغم
الشحنة الكهربية:صفر (طبيعية), أو شحنة أيون
نطاقالقطر:62 بيكومتر
(He) إلى 520 بيكومتر (Cs) (صفحة بيانات)ا
لمكونات:إلكترونات وما يوافقها في النواة من البروتوناتإلى جانب النيوترونات
النظرية الذرية
النظرية الذرية تهتم بدراسة طبيعة المادة، وتنص على أن كل المواد تتكون من ذرات. -الاكتشافات اليونانية في عام 430 ق.م توصل الفيلسوف اليونانى (ديموقريطس) إلى مفهوم أو فكرة في كل الأشياء مصنوعة من ذرات أو بالمعنى الحرفى كل الأشياء مكونة من ذرات غير قابلة للانقسام. واعتقد هذا الفيلسوف أن كل الذرات متماثلة وصلبة وغير قابلة للانضغاط إلى جانب أنها غير قابلة للإنقسام ، وأن الذرات تتحرك بأعداد لا حصر لها في فضاء فارغ.وأن الاختلاف في الشكل والحجم الذرى يحدد الخصائص المختلفة لكل مادة. وطبقاً لفلسفة (ديموقريطس) فإن الذرات ليست المكون الأساسي للمواد فقط ولكنها تكون أيضاً خصائص النفس الإنسانية. فعلى سبيل المثال فإن الآلام تسببها "الذرات الشريرة" وذلك لأن هذه الذرات تكون على شكل (إبر) بينما يتكون اللون الفاتح من الذرات المسطحة ذات الملمس الناعم ، وقد اعتقد ديمقريطس واعتقد معه الناس أفكار هي بلا شك تثير تهكمنا الآن ولكنها كانت منذ قرون "العلم الذي لا يبارى". إن النظرية اليونانية عن الذرة لها مدلول تاريخي وفلسفى بالغ الأهمية ، إلا أنها ليست ذات قيمة علمية، ذلك أنها لم تقم على أساس ملاحظة الطبيعة أو القياس أو الاختبارات أو التجارب
الرمز النمطي للذرة
تعريف أصغر قسم معترف به من العنصر الكيميائي
الخصائص
الوزن الشامل:1.67×10−27 إلى 4.52×10−25 كغم
الشحنة الكهربية:صفر (طبيعية), أو شحنة أيون
نطاقالقطر:62 بيكومتر
(He) إلى 520 بيكومتر (Cs) (صفحة بيانات)ا
لمكونات:إلكترونات وما يوافقها في النواة من البروتوناتإلى جانب النيوترونات
النظرية الذرية
النظرية الذرية تهتم بدراسة طبيعة المادة، وتنص على أن كل المواد تتكون من ذرات. -الاكتشافات اليونانية في عام 430 ق.م توصل الفيلسوف اليونانى (ديموقريطس) إلى مفهوم أو فكرة في كل الأشياء مصنوعة من ذرات أو بالمعنى الحرفى كل الأشياء مكونة من ذرات غير قابلة للانقسام. واعتقد هذا الفيلسوف أن كل الذرات متماثلة وصلبة وغير قابلة للانضغاط إلى جانب أنها غير قابلة للإنقسام ، وأن الذرات تتحرك بأعداد لا حصر لها في فضاء فارغ.وأن الاختلاف في الشكل والحجم الذرى يحدد الخصائص المختلفة لكل مادة. وطبقاً لفلسفة (ديموقريطس) فإن الذرات ليست المكون الأساسي للمواد فقط ولكنها تكون أيضاً خصائص النفس الإنسانية. فعلى سبيل المثال فإن الآلام تسببها "الذرات الشريرة" وذلك لأن هذه الذرات تكون على شكل (إبر) بينما يتكون اللون الفاتح من الذرات المسطحة ذات الملمس الناعم ، وقد اعتقد ديمقريطس واعتقد معه الناس أفكار هي بلا شك تثير تهكمنا الآن ولكنها كانت منذ قرون "العلم الذي لا يبارى". إن النظرية اليونانية عن الذرة لها مدلول تاريخي وفلسفى بالغ الأهمية ، إلا أنها ليست ذات قيمة علمية، ذلك أنها لم تقم على أساس ملاحظة الطبيعة أو القياس أو الاختبارات أو التجارب
الرمز النمطي للذرة
نموذج دالتون[عدل]وجاءت نظرية دالتون بشكل مختلف عما سبق ذلك كونها تعتمد على قوانين بقاء الكتلة والنسب الثابتة والتي اشتقت من العديد من الاستنتاجات المباشرة.
يمكن التعبير عن النظرية التي اقترحها بالاتي :
تفسر هذه النظرية (قانون النسب الثابتة) : افترض دالتون ان مادة ما تتكون من عنصرين A و B. وان أي جزيئي من هذه المادة يتكون من ذرة واحدة من A وذرة واحدة من B يعرف الجزيء بأنه مجموعة ذرات مترابطة مع بعضها بقوة تسمح لها بالتصرف أو اعادة التنظيم كجسيم واحد. افترض أيضا ان كتلة الذرة A تكون ضعف كتلة الذرة B وبالتالى فان الذرة A تساهم بضعف الكتلة التي تساهم بها الذرة B في تكوين جزيء واحد من هذه المادة الأمر الذي يعني ان نسبة كتلة الذرة Aالى الذرة B هي 2/1. في مركب الماء نسبة الهيدروجين إلى الأكسجين دائماً ثابتة :
2.00g H /16.00g O=1.00g H / 8.00g O
لقد تنبأت نظرية دالتون بقانون النسب المتضاعفة (قانون النسب المتعددة): عندما تتحدد ذرة ما مع أخرى وتشكل أكثر من مركب فإن نسبة الأوزان لتلك الذرة التي تتحد مع واحد جرام من الذرة الأخرى يجب أن يكون نسبة بسيطة.
مثال: الأكسجين يتحد مع الكربون ويشكل أكثر من مركب (CO1 ، CO2)، وزن الأكسجين الذي يتحد مع واحد جرام من الكربون في المركبين هو 2.66g للمركب الأول و 1.33g للمركب الثاني ، نسبة هذه الأوزان هي :
2 = 2.66g 1 1.3
وكان دالتون أول من حسب أوزان ذرات عدد من العناصر.
نموذج فاراداي
[توصّل فاراداي إلى أن الذرات تحتوي على جسيمات مكهربة تدعى إلكترونات وقام بتجارب تحليل أملاح إلا أنه لم يضع أي نموذج ذري
نموذج طومسون]
نموذج تومسون، الشحنة الموجبة موزعة بالتساوي على كل الحجم المشغول بالإلكترونات
في عام 1896م أجرى أبحاثاً حول أشعة الكاثود. وفي عام 30 أبريل 1897م، أدهش الأوساط العلمية بإعلانه عن أن الجسيمات المكونة لأشعة الكاثود هي أصغر حجماً بكثير من الذرات، وقد سميت هذه الجسيمات بالإلكترونات.
وفى عام 1897م أظهر اكتشاف الالكترون للعالم "طومسون" أن المفهوم القديم عن الذرة منذ ألفى عام، والذي ينطوى عليها على أنها جسيم غير قابل للإنقسام كان مفهوماً خاطئاً، كما أظهر أيضاً أن للذرة - في الواقع- ترتيب معقد غير أنهم لم يغيروا مصطلح "الذرة" أو الغير قابله للتجزئة إلى "اللا ذرة" وأدى اكتشاف "طومسون" عن الالكترون ذو الشحنة السالبة إلى إثارة الإشكاليات النظرية لدى الفيزيائيين لأن الذرات ككل - تحمل شحنات كهربائية متعادلة فأين الشحنة الإيجابية التي تعادل شحنة الإلكترون.
وفى الفترة ما بين عامى (1903 - 1907) حاول - "طومسون" أن يحل هذا اللغز السابق الذي ذكره عن طريق تكييف نموذج للذرة والتي اقترحها في المقام الأول "اللورد كيلفن" في عام 1902، وطبقاً لهذا النموذج والذي يشار إليه غالباً بنموذج "كرة معجونة وبها بعض حبوب الزبيب" فإن الذرة غالباً هنا عبارة عن كرة ذات شحنة موجبة متماثلة أما الشحنات السالبة فإنها منتشرة على الإلكترونات مثل الزبيب المدفون في كرة معجونة.
وترجع أفضلية نظرية " طومسون" عن الذرة في أنها ثابتة، فإذا لم توضع الإلكترونات في مكانها الصحيح فستحاول أن تعود إلى مواضعها الأصلية ثانية. وفى نموذج معاصر أيضاً نظر العلماء إلى الذرة على أنها مثل النظام الشمسى أو مثل كوكب "زحل" ذو حلقات من الإلكترونات محيطة بالشحنة الكهربية الإيجابية المركزة.
حيث توصل طومسون إلى أن
نموذج رذرفورد[عدل]اكتشف رذرفورد من خلال تجاربه بأن الشحنة الموجبة للذرة تتركز في مركزها في نواة صغيرة مكثفة وتراصة وعلى أساس ذلك وضع نموذجه الذري الذي عرف بالنموذج النووي. افترض راذرفورد عام 1911م النموذج النووي للذرة معتبراً أن الذرة تتكون من كتلة صغيرة جداً وكثيفة جداً ذات شحنة موجبة تسمى النواة وتحتل مركز الذرة وتحتوي نواة الذرة على جميع البروتونات ولذا فان كتلة الذرة هي تعبير عن مجموع كتل البروتونات في نواتها (حيث أن قيمة كتل الإلكترونات صغيرة جداً…. فهي قيم مهملة). كما أن شحنة النواة الموجبة ترجع إلى تمركز البروتونات الموجبة بها. وتتوزع الالكترونات في الذرة حول النواة بنفس الطريقة التي تتوزع بها الأجرام السماوية حول الشمس. وبما أن الذرة متعادلة لذا فعدد الاليكترونات السيارة يساوي عدد البروتونات بالنواة.
قام العالم راذرفورد بإجراء بعض من أبرز التجارب للوصول إلى حقائق تركيب الذرة. وقد اعتمد في تجارية على استخدام جسيمات ألفا المنطلقة من مادة مشعة وفي اعتقاده أن المادة المشعة تطلق إشعاعاتها في كافة الاتجاهات وبلا حدود وهي تتكون من جسيمات ألفا (œ-particles) الموجبة الشحنة وجسيمات بيتا (ß-particles) السالبة الشحنة وأشعة جاما (y-rays) المتعادلة الشحنة. ويمكن اعتبار جسيمات ألفا تحمل على أنها ذرات للهليوم فقد منها إليكترونين ولذا فان جسيمات ألفا تحمل شحنتين موجبتين ولها كتلة تساوي أربعة مرات كتلة ذرة الهيدروجين. وقد ساعد "رذر فورد" على تنمية معرفتنا بالذرة ،عندما قام مع "هانز جيجر" بإجراء تجارب رقائق الذهب الشهيرة والتي أظهرت أن للذرة نواة صغيرة ولكنها تحتوى على كل الكتلة تقريباً. فقد قام بإطلاق جسيمات "ألفا" خلال الرقائق الذهبية ثم استقبلت هذه الجسيمات كومضات ضوئية.
لقد سمح راذرفورد بإطلاق حزمة رقيقة للغاية من جسيمات ألفا من مصدر مشع كعنصر البولونيوم بالمرور في اتجاه صفيحة معدنية رقيقة من الفضة أو الذهب ،وبعد اختراق تلك الجسيمات الصفيحة المعدنية استقبلها على لوح من كبرتيد الخارصين موضوع خلفها وكانت النتائج : قام روذرفورد عمليا بإطلاق جسيمات "ألفا" خلال الرقائق الذهبية تصل سماكة الرقيقة الذهبية الواحدة إلى حوالى 0.00004 سنتيمتر فقط، ثم استقبل هذه الجسيمات كومضات ضوئية على شاشة الاستقبال ومرت معظم الجزئيات مباشرة عبر الرقائق في حين انحرفت واحدة فقط من عشرين ألف جزئ (ألفا) إلى حوالى 45ْ م أو أكثر. هذه التجربة شكلت ثورة علمية في المفهوم الذري وقتها وكانت الطريقة الوحيدة لقبول واستيعاب نتائج هذه التجربة هي فيما استطاع روذرفورد تفسيره على أن كامل كتلة الذرة تقريبا مجتمعة في المركز وتمتلك هذه النواة حجما صغيراً جداً مقارنة بحجم الذرة الكلية وقد توصل روذرفورد نتيجة ذلك إلى القول ((من خلال التفكير والدراسة أدركت أن هذا الارتداد المتفرق هي نتيجة حتمية للتصادم الفردى فعندما قمت بالعد وجدت أنه من المستحيل أن أحصل على أي نتيجة ولهذا العدد الضخم، إلا إذا أخذت نظام يكون الجزء الأكبر من الكتلة من الذرة فيه مركزا بالنواة الدقيقة. وبعد كل هذا التحليل أستطيع القول بأننى قد توصلت إلى وجود ذرة ذات مركز دقيق جداً به أغلب الكتلة ويحمل شحنة موجبة تعادل شحنة الإلكترون.)). إن الطريقة الوحيدة التي مكنت راذرفورد من تفسير نتائج تجربته المدهشة وقدرة الجسيمات على المرور والانحراف ضمن الذرة هي الاستنتاجات بأن :
أولاً : وجود فراغ كبير في الذرة دليل على عدم الانحراف الكلي للجسيمات.
ثانياً : احتواء الذرة بعض الجسيمات الثقيلة والمشحونة بشحنات موجبة وبالتالي فإن اقتراب جسيمات ألفا من هذه الجسيمات الموجبة قد تسبب في تنافر بسيط معها ، وبالتالي كان سببا في انحراف بعض جسيمات ألفا.
ثالثاً: تمركز الجسيمات الموجبة الشحنة بالذرة في وسطها مما سبب الانحراف الكلى لجسيمات ألفا (قليلة العدد نظراً لصغر حجم الفراغ الذي تشغله النواة) المارة بمركز النواة. مما سبب الانحراف الكبير لهذه الجسيمات.
نموذج الذرة التي توصل إليها روذرفورد (النموذج النووي):
اولاً : الذرة ليست متزنة ميكانيكياً حيث أن النواة الموجبة تقوم بجذب الالكترونات السالبة وتلتحم وتتعادل بفرض أن الالكترونات سالبة. إذا كانت الالكترونات تدور حول النواة في مسار دائري تنشأ قوة مركزية تساوي (ك ع2 / نق) وبالتالي يتحرك الالكترون بتسارع مركزي ويكون مع النواة ثنائي متذبذب فيشع أمواجاً كهرومغناطيسية ويدور في مسار حلزوني إلى أن يسقط في النواة.
ثانياً : بما أن الالكترون يدور حول النواة ويكون معها زوجا متذبذباً إذاً الذرة تشع طيف مستمر متغير في التردد والطول الموجي وتتناقص طاقته تدريجيا وهذا يناقض مع التجارب العملية التي أثبتت أن الذرات تشع طيفاً خطياً له طول موجي محدد بدقــة.
#BASSANT
يمكن التعبير عن النظرية التي اقترحها بالاتي :
- الأشياء (المواد) تتكون من العديد من الجسيمات الغير قابلة للتجزئة(ذرات) ذات حجم صغير جداً.
- ذرات نفس العنصر متشابهة في الخواص (الشكل ، الحجم ، الكتلة)، وتختلف تماماً عن ذرات العناصر الأخرى.
- الذرة مصمتة متناهية الصغر،غير قابلة للتجزئة
- يمكن لذرات العناصر المختلفة أن تتحد مع بعضها بنسب عددية بسيطة مكونة المواد.
- الاتحاد الكيميائي عبارة عن تغيير في توزيع الذرات.
تفسر هذه النظرية (قانون النسب الثابتة) : افترض دالتون ان مادة ما تتكون من عنصرين A و B. وان أي جزيئي من هذه المادة يتكون من ذرة واحدة من A وذرة واحدة من B يعرف الجزيء بأنه مجموعة ذرات مترابطة مع بعضها بقوة تسمح لها بالتصرف أو اعادة التنظيم كجسيم واحد. افترض أيضا ان كتلة الذرة A تكون ضعف كتلة الذرة B وبالتالى فان الذرة A تساهم بضعف الكتلة التي تساهم بها الذرة B في تكوين جزيء واحد من هذه المادة الأمر الذي يعني ان نسبة كتلة الذرة Aالى الذرة B هي 2/1. في مركب الماء نسبة الهيدروجين إلى الأكسجين دائماً ثابتة :
2.00g H /16.00g O=1.00g H / 8.00g O
لقد تنبأت نظرية دالتون بقانون النسب المتضاعفة (قانون النسب المتعددة): عندما تتحدد ذرة ما مع أخرى وتشكل أكثر من مركب فإن نسبة الأوزان لتلك الذرة التي تتحد مع واحد جرام من الذرة الأخرى يجب أن يكون نسبة بسيطة.
مثال: الأكسجين يتحد مع الكربون ويشكل أكثر من مركب (CO1 ، CO2)، وزن الأكسجين الذي يتحد مع واحد جرام من الكربون في المركبين هو 2.66g للمركب الأول و 1.33g للمركب الثاني ، نسبة هذه الأوزان هي :
2 = 2.66g 1 1.3
وكان دالتون أول من حسب أوزان ذرات عدد من العناصر.
نموذج فاراداي
[توصّل فاراداي إلى أن الذرات تحتوي على جسيمات مكهربة تدعى إلكترونات وقام بتجارب تحليل أملاح إلا أنه لم يضع أي نموذج ذري
نموذج طومسون]
نموذج تومسون، الشحنة الموجبة موزعة بالتساوي على كل الحجم المشغول بالإلكترونات
في عام 1896م أجرى أبحاثاً حول أشعة الكاثود. وفي عام 30 أبريل 1897م، أدهش الأوساط العلمية بإعلانه عن أن الجسيمات المكونة لأشعة الكاثود هي أصغر حجماً بكثير من الذرات، وقد سميت هذه الجسيمات بالإلكترونات.
وفى عام 1897م أظهر اكتشاف الالكترون للعالم "طومسون" أن المفهوم القديم عن الذرة منذ ألفى عام، والذي ينطوى عليها على أنها جسيم غير قابل للإنقسام كان مفهوماً خاطئاً، كما أظهر أيضاً أن للذرة - في الواقع- ترتيب معقد غير أنهم لم يغيروا مصطلح "الذرة" أو الغير قابله للتجزئة إلى "اللا ذرة" وأدى اكتشاف "طومسون" عن الالكترون ذو الشحنة السالبة إلى إثارة الإشكاليات النظرية لدى الفيزيائيين لأن الذرات ككل - تحمل شحنات كهربائية متعادلة فأين الشحنة الإيجابية التي تعادل شحنة الإلكترون.
وفى الفترة ما بين عامى (1903 - 1907) حاول - "طومسون" أن يحل هذا اللغز السابق الذي ذكره عن طريق تكييف نموذج للذرة والتي اقترحها في المقام الأول "اللورد كيلفن" في عام 1902، وطبقاً لهذا النموذج والذي يشار إليه غالباً بنموذج "كرة معجونة وبها بعض حبوب الزبيب" فإن الذرة غالباً هنا عبارة عن كرة ذات شحنة موجبة متماثلة أما الشحنات السالبة فإنها منتشرة على الإلكترونات مثل الزبيب المدفون في كرة معجونة.
وترجع أفضلية نظرية " طومسون" عن الذرة في أنها ثابتة، فإذا لم توضع الإلكترونات في مكانها الصحيح فستحاول أن تعود إلى مواضعها الأصلية ثانية. وفى نموذج معاصر أيضاً نظر العلماء إلى الذرة على أنها مثل النظام الشمسى أو مثل كوكب "زحل" ذو حلقات من الإلكترونات محيطة بالشحنة الكهربية الإيجابية المركزة.
حيث توصل طومسون إلى أن
- الذرة كرة مصمتة موجبة الشحنة.
- تتخلل الالكترونات السالبة الذرة (كما تتخلل البذور ثمرة البرتقال).
- الذرة متعادلة كهربائياً.
نموذج رذرفورد[عدل]اكتشف رذرفورد من خلال تجاربه بأن الشحنة الموجبة للذرة تتركز في مركزها في نواة صغيرة مكثفة وتراصة وعلى أساس ذلك وضع نموذجه الذري الذي عرف بالنموذج النووي. افترض راذرفورد عام 1911م النموذج النووي للذرة معتبراً أن الذرة تتكون من كتلة صغيرة جداً وكثيفة جداً ذات شحنة موجبة تسمى النواة وتحتل مركز الذرة وتحتوي نواة الذرة على جميع البروتونات ولذا فان كتلة الذرة هي تعبير عن مجموع كتل البروتونات في نواتها (حيث أن قيمة كتل الإلكترونات صغيرة جداً…. فهي قيم مهملة). كما أن شحنة النواة الموجبة ترجع إلى تمركز البروتونات الموجبة بها. وتتوزع الالكترونات في الذرة حول النواة بنفس الطريقة التي تتوزع بها الأجرام السماوية حول الشمس. وبما أن الذرة متعادلة لذا فعدد الاليكترونات السيارة يساوي عدد البروتونات بالنواة.
قام العالم راذرفورد بإجراء بعض من أبرز التجارب للوصول إلى حقائق تركيب الذرة. وقد اعتمد في تجارية على استخدام جسيمات ألفا المنطلقة من مادة مشعة وفي اعتقاده أن المادة المشعة تطلق إشعاعاتها في كافة الاتجاهات وبلا حدود وهي تتكون من جسيمات ألفا (œ-particles) الموجبة الشحنة وجسيمات بيتا (ß-particles) السالبة الشحنة وأشعة جاما (y-rays) المتعادلة الشحنة. ويمكن اعتبار جسيمات ألفا تحمل على أنها ذرات للهليوم فقد منها إليكترونين ولذا فان جسيمات ألفا تحمل شحنتين موجبتين ولها كتلة تساوي أربعة مرات كتلة ذرة الهيدروجين. وقد ساعد "رذر فورد" على تنمية معرفتنا بالذرة ،عندما قام مع "هانز جيجر" بإجراء تجارب رقائق الذهب الشهيرة والتي أظهرت أن للذرة نواة صغيرة ولكنها تحتوى على كل الكتلة تقريباً. فقد قام بإطلاق جسيمات "ألفا" خلال الرقائق الذهبية ثم استقبلت هذه الجسيمات كومضات ضوئية.
لقد سمح راذرفورد بإطلاق حزمة رقيقة للغاية من جسيمات ألفا من مصدر مشع كعنصر البولونيوم بالمرور في اتجاه صفيحة معدنية رقيقة من الفضة أو الذهب ،وبعد اختراق تلك الجسيمات الصفيحة المعدنية استقبلها على لوح من كبرتيد الخارصين موضوع خلفها وكانت النتائج : قام روذرفورد عمليا بإطلاق جسيمات "ألفا" خلال الرقائق الذهبية تصل سماكة الرقيقة الذهبية الواحدة إلى حوالى 0.00004 سنتيمتر فقط، ثم استقبل هذه الجسيمات كومضات ضوئية على شاشة الاستقبال ومرت معظم الجزئيات مباشرة عبر الرقائق في حين انحرفت واحدة فقط من عشرين ألف جزئ (ألفا) إلى حوالى 45ْ م أو أكثر. هذه التجربة شكلت ثورة علمية في المفهوم الذري وقتها وكانت الطريقة الوحيدة لقبول واستيعاب نتائج هذه التجربة هي فيما استطاع روذرفورد تفسيره على أن كامل كتلة الذرة تقريبا مجتمعة في المركز وتمتلك هذه النواة حجما صغيراً جداً مقارنة بحجم الذرة الكلية وقد توصل روذرفورد نتيجة ذلك إلى القول ((من خلال التفكير والدراسة أدركت أن هذا الارتداد المتفرق هي نتيجة حتمية للتصادم الفردى فعندما قمت بالعد وجدت أنه من المستحيل أن أحصل على أي نتيجة ولهذا العدد الضخم، إلا إذا أخذت نظام يكون الجزء الأكبر من الكتلة من الذرة فيه مركزا بالنواة الدقيقة. وبعد كل هذا التحليل أستطيع القول بأننى قد توصلت إلى وجود ذرة ذات مركز دقيق جداً به أغلب الكتلة ويحمل شحنة موجبة تعادل شحنة الإلكترون.)). إن الطريقة الوحيدة التي مكنت راذرفورد من تفسير نتائج تجربته المدهشة وقدرة الجسيمات على المرور والانحراف ضمن الذرة هي الاستنتاجات بأن :
أولاً : وجود فراغ كبير في الذرة دليل على عدم الانحراف الكلي للجسيمات.
ثانياً : احتواء الذرة بعض الجسيمات الثقيلة والمشحونة بشحنات موجبة وبالتالي فإن اقتراب جسيمات ألفا من هذه الجسيمات الموجبة قد تسبب في تنافر بسيط معها ، وبالتالي كان سببا في انحراف بعض جسيمات ألفا.
ثالثاً: تمركز الجسيمات الموجبة الشحنة بالذرة في وسطها مما سبب الانحراف الكلى لجسيمات ألفا (قليلة العدد نظراً لصغر حجم الفراغ الذي تشغله النواة) المارة بمركز النواة. مما سبب الانحراف الكبير لهذه الجسيمات.
نموذج الذرة التي توصل إليها روذرفورد (النموذج النووي):
- الذرة تشبه المجموعة الشمسية (نواة مركزية يدور حولها على مسافات شاسعة الالكترونات سالبة الشحنة)
- الذرة معظمها فراغ (لأن الذرة ليست مصمتة وحجم النواة صغير جدا بالنسبة لحجم الذرة)
- تتركز كتلة الذرة في النواة (لأن كتلة الالكترونات صغيرة جدا مقارنة بكتلة مكونات النواة من البروتونات والنيوترونات)
- يوجد بالذرة نوعان من الشحنة (شحنة موجبة بالنواة وشحنات سالبة على الالكترونات
- الذرة متعادلة كهربيا لأن عدد الشحنات الموجبة (البروتونات) يساوي عدد الشحنات السالبة (الالكترونات)
- تدور الالكترونات حول النواة في مدارات خاصة.
- يرجع ثبات الذرة إلى وقوع الالكترونات تحت تأثير قوتين متضادتين في الاتجاه متساويتين في المقدار هما قوة جذب النواة للالكترونات وقوة الطرد المركزي الناشئة عن دوران الالكترونات حول النواة.
اولاً : الذرة ليست متزنة ميكانيكياً حيث أن النواة الموجبة تقوم بجذب الالكترونات السالبة وتلتحم وتتعادل بفرض أن الالكترونات سالبة. إذا كانت الالكترونات تدور حول النواة في مسار دائري تنشأ قوة مركزية تساوي (ك ع2 / نق) وبالتالي يتحرك الالكترون بتسارع مركزي ويكون مع النواة ثنائي متذبذب فيشع أمواجاً كهرومغناطيسية ويدور في مسار حلزوني إلى أن يسقط في النواة.
ثانياً : بما أن الالكترون يدور حول النواة ويكون معها زوجا متذبذباً إذاً الذرة تشع طيف مستمر متغير في التردد والطول الموجي وتتناقص طاقته تدريجيا وهذا يناقض مع التجارب العملية التي أثبتت أن الذرات تشع طيفاً خطياً له طول موجي محدد بدقــة.
#BASSANT
نموذج بور
في عام 1913م اقترح الفيزيائي الدنماركي نيلز بور نموذجًا للذرة تنتظم فيه الإلكترونات في مدارات متوالية الاتساع حول نواة صغيرة تتكون من البروتونات والنيوترونات. ويقترح بور أن الإلكترونات تدور حول النواة في مسارات دائرية وبمدارات محددة ، وطالما أنها في مداراتها فإنها تمتلك طاقة محددة وثابتة ، وتفقد جزء من طاقتها على شكل إشعاع ضوئي عند الانتقال من مدار أبعد إلى مار أقرب عن النواة ، والعكس صحيح ، فعند إعطاء الإلكترون كمية من الطاقة كالتسخين مثلا ، عندئذ يمكن أن ينتقل من مدار أقرب إلى مدار أبعد عن النواة بسبب امتصاصه هذه الطاقة. واعتقد بور بأن العديد من خواص العنصر تعتمد على(عدد) الإلكترونات الموجودة في المدار الخارجي لذرة ذلك العنصر. ولقد ساعد نموذج بور للذرة على تفسير الكيفية التي تتفاعل بها الذرات مع الضوء والأشكال الأخرى للإشعاع. فقد افترض بور أن امتصاص وابتعاث (إطلاق) الضوء بوساطة الذرة يستلزم تغييرًا في وضع وطاقة الإلكترون فيقفز من مدار لآخر. وقد استطاع الكيميائيون الحصول على الكثير من المعلومات حول تركيب الجزيئات عن طريق قياس كمية الإشعاع التي تمتصها والتي تنبعث منها. افتراضات نيلز بور في نموذجه الذري : 1- الإلكترونات تدور حول النواة في مسارات دئرية الشكل وضمن مدارات محددة ولها طاقات ثابتة ومحددة. 2- كل مدار له طاقة محددة وثابتة يعبر عنها بأرقام صحيحة من 1-7 سميت بالأعداد الكمية الرئيسية. 3- لا يفقد الإلكترون طاقة ما دام في مداره وإذا صعد لمدار أعلى فإنه يكتسب طاقة تسمى طيف امتصاص. وإذا نزل لمدار أدنى فإنه يفقد طاقة ضوئية تسمى طيف انبعاث.
في عام 1913م اقترح الفيزيائي الدنماركي نيلز بور نموذجًا للذرة تنتظم فيه الإلكترونات في مدارات متوالية الاتساع حول نواة صغيرة تتكون من البروتونات والنيوترونات. ويقترح بور أن الإلكترونات تدور حول النواة في مسارات دائرية وبمدارات محددة ، وطالما أنها في مداراتها فإنها تمتلك طاقة محددة وثابتة ، وتفقد جزء من طاقتها على شكل إشعاع ضوئي عند الانتقال من مدار أبعد إلى مار أقرب عن النواة ، والعكس صحيح ، فعند إعطاء الإلكترون كمية من الطاقة كالتسخين مثلا ، عندئذ يمكن أن ينتقل من مدار أقرب إلى مدار أبعد عن النواة بسبب امتصاصه هذه الطاقة. واعتقد بور بأن العديد من خواص العنصر تعتمد على(عدد) الإلكترونات الموجودة في المدار الخارجي لذرة ذلك العنصر. ولقد ساعد نموذج بور للذرة على تفسير الكيفية التي تتفاعل بها الذرات مع الضوء والأشكال الأخرى للإشعاع. فقد افترض بور أن امتصاص وابتعاث (إطلاق) الضوء بوساطة الذرة يستلزم تغييرًا في وضع وطاقة الإلكترون فيقفز من مدار لآخر. وقد استطاع الكيميائيون الحصول على الكثير من المعلومات حول تركيب الجزيئات عن طريق قياس كمية الإشعاع التي تمتصها والتي تنبعث منها. افتراضات نيلز بور في نموذجه الذري : 1- الإلكترونات تدور حول النواة في مسارات دئرية الشكل وضمن مدارات محددة ولها طاقات ثابتة ومحددة. 2- كل مدار له طاقة محددة وثابتة يعبر عنها بأرقام صحيحة من 1-7 سميت بالأعداد الكمية الرئيسية. 3- لا يفقد الإلكترون طاقة ما دام في مداره وإذا صعد لمدار أعلى فإنه يكتسب طاقة تسمى طيف امتصاص. وإذا نزل لمدار أدنى فإنه يفقد طاقة ضوئية تسمى طيف انبعاث.
النمـوذج الـذري الحديث
تتكون الذرة من نواة تحتوي على الشحنة الموجبة (بروتونات) تتركز فيها معظم الكتلة محاطة بإلكترونات سالبة الشحنة تتحرك بسرعة كبيرة ولها خواص الموجات بموجب معادلة رياضية وموجودة في فراغ حول النواة يكون احتمال وجودها فيه أكثر من 90% تسمى المجالات الإلكترونية.
مكونات الذرة ونظرية الكم
تتكون الذرة من سحابة من الشحنات السالبة (الإلكترونات) تحوم حول نواة موجبة الشحنة صغيرة جدا في الوسط. تتكون النواة الموجبة هذه من بروتونات موجبة الشحنة، ونيوترونات متعادلة. الذرة هي أصغر جزء من العنصر يمكن أن يتميز به عن بقية العناصر؛ إذ كلما غصنا أكثر في المادة لنلاقي البنى الأصغر لن يعود هناك فرق بين عنصر وآخر. فمثلاً، لا فرق بين بروتون في ذرة حديد وبروتون آخر في ذرة يورانيوم مثلاً، أو ذرة أي عنصر آخر. الذرة، بما تحمله من خصائص؛ عدد بروتوناتها، كتلتها، توزيعها الإلكتروني...، تصنع الفروقات بين العناصر المختلفة، وبين الصور المختلفة للعنصر نفسه (المسماة بالنظائر)، وحتى بين كون هذا العنصر قادراً على خوض تفاعل كيميائي ما أم لا. ظل تركيب الذرة وما يجري في هذا العالم البالغ الصغر، ظل وما زال يشغل العلماء ويدفعهم إلى اكتشاف المزيد. ومن هنا أخذت تظهر فروع جديدة في العلم حاملة معها مبادئها ونظرياتها الخاصة بها، بدءاً بمبدأ الشك (اللاثقة)، مروراً بنظريات التوحيد الكبرى، وانتهاءً بنظرية الأوتار الفائقة أكثر النظريات التي لاقت قبولا لتفسير تركيب الذرة هي النظرية الموجية. وهذا التصور مبني على تصور بوهر مع الأخذ في الاعتبار الاكتشافات الحديثة والتطويرات في ميكانيكا الكم. و التي تنص على :
:-خصائص الذرة
اول خاصية هي العدد الذري وهو عدد البروتونات بالذرة
:-الذرة في العلم
ظلت الذرة محل أنظار تركيز العلماء لعقود. وكان للنظرية الذرية تأثير كبير على كثير من فروع العلم، مثل الفيزياء النووية، الطيف وكل فروع الكيمياء تقريبا. ويتم دراسة الذرة هذه الأيام في مجال ميكانيكا الكم والجسيمات تحت-الذرية.
و قد تمت دراسة الذرة بدون قصد مباشر في القرن 19 والقرن 20 وفى السنين الحالية، وبظهور تقنيات جديدة أصبحت دراسة الذرة أسهل وأدق. فعن استخدام الميكروسكوب الإلكتروني الذي تم اكتشافه في عام 1931 تم تصوير ذرات مفردة. كما تم استحداث طرق جديدة للتعرف على الذرات والمركبات. فمثلا يتم استخدام مطياف الكتلة لتحديد الذرات والمركبات. كما يتم استخدام جي سي إم إس " كروماتوجرافى الغاز ومطياف الكتلة " لمعرفة المواد. وأيضا التأكد من وجود ذرات أو جزيئات معينة عن طريق أشعة إكس كريستالوجرافى.
الذرة في الصناعة
تقوم الذرة بدور غاية في الأهمية في الصناعة، يتضمن ذلك الصناعات النووية، علم المواد الصناعية، وأيضا في الصناعات الكيميائية.
#BASSANT
تتكون الذرة من نواة تحتوي على الشحنة الموجبة (بروتونات) تتركز فيها معظم الكتلة محاطة بإلكترونات سالبة الشحنة تتحرك بسرعة كبيرة ولها خواص الموجات بموجب معادلة رياضية وموجودة في فراغ حول النواة يكون احتمال وجودها فيه أكثر من 90% تسمى المجالات الإلكترونية.
مكونات الذرة ونظرية الكم
تتكون الذرة من سحابة من الشحنات السالبة (الإلكترونات) تحوم حول نواة موجبة الشحنة صغيرة جدا في الوسط. تتكون النواة الموجبة هذه من بروتونات موجبة الشحنة، ونيوترونات متعادلة. الذرة هي أصغر جزء من العنصر يمكن أن يتميز به عن بقية العناصر؛ إذ كلما غصنا أكثر في المادة لنلاقي البنى الأصغر لن يعود هناك فرق بين عنصر وآخر. فمثلاً، لا فرق بين بروتون في ذرة حديد وبروتون آخر في ذرة يورانيوم مثلاً، أو ذرة أي عنصر آخر. الذرة، بما تحمله من خصائص؛ عدد بروتوناتها، كتلتها، توزيعها الإلكتروني...، تصنع الفروقات بين العناصر المختلفة، وبين الصور المختلفة للعنصر نفسه (المسماة بالنظائر)، وحتى بين كون هذا العنصر قادراً على خوض تفاعل كيميائي ما أم لا. ظل تركيب الذرة وما يجري في هذا العالم البالغ الصغر، ظل وما زال يشغل العلماء ويدفعهم إلى اكتشاف المزيد. ومن هنا أخذت تظهر فروع جديدة في العلم حاملة معها مبادئها ونظرياتها الخاصة بها، بدءاً بمبدأ الشك (اللاثقة)، مروراً بنظريات التوحيد الكبرى، وانتهاءً بنظرية الأوتار الفائقة أكثر النظريات التي لاقت قبولا لتفسير تركيب الذرة هي النظرية الموجية. وهذا التصور مبني على تصور بوهر مع الأخذ في الاعتبار الاكتشافات الحديثة والتطويرات في ميكانيكا الكم. و التي تنص على :
- تتكون الذرة من جسيمات تحت ذرية (البروتونات ،الإلكترونات ،النيوترونات).
- مع العلم بأن معظم حجم الذرة يحتوى على فراغ.
- في مركز الذرة توجد نواة موجبة الشحنة تتكون من البروتونات ،النيوترونات (ويعرفوا على أنهم نويات)
- النواة أصغر 100,000 مرة من الذرة. فلو أننا تخيلنا أن الذرة بإتساع مطار هيثرو فإن النواة ستكون في حجم كرة الجولف
- معظم الفراغ الذري يتم شغله بالمدارات التي تحتوى على الإلكترونات في شكل إلكترونى محدد.
- كل مدار يمكن أن يتسع لعدد 2 إلكترون ، محكومين بثلاث أرقام للكم ، عدد الكم الرئيسي ، عدد الكم الثانوي ، عدد الكم المغناطيسي.
- كل إلكترون في أي من المدارات له قيمة واحدة لعدد الكم الرابع والذي يسمى عدد الكم المغناطيسي.
- المدارات ليست ثابتة ومحددة في الاتجاه وإنما هي تمثل احتمالية تواجد 2 إلكترون لهم نفس الثلاث أعداد الأولى للكم ، وتكون آخر حدود هذا المدار هو المناطق التي يقل تواجد الإلكترون فيها عن 90%.
- عند انضمام الإلكترون إلى الذرة فإنها تشغل أقل مستويات الطاقة ، والذي تكون المدارات فيه قريبة للنواة (مستوى الطاقة الأول). وتكون الإلكترونات الموجودة في المدارات الخارجية (مدار التكافؤ) هي المسئولة عن الترابط بين الذرات. لمزيد من التفاصيل راجع "التكافؤ والترابط
:-خصائص الذرة
اول خاصية هي العدد الذري وهو عدد البروتونات بالذرة
:-الذرة في العلم
ظلت الذرة محل أنظار تركيز العلماء لعقود. وكان للنظرية الذرية تأثير كبير على كثير من فروع العلم، مثل الفيزياء النووية، الطيف وكل فروع الكيمياء تقريبا. ويتم دراسة الذرة هذه الأيام في مجال ميكانيكا الكم والجسيمات تحت-الذرية.
و قد تمت دراسة الذرة بدون قصد مباشر في القرن 19 والقرن 20 وفى السنين الحالية، وبظهور تقنيات جديدة أصبحت دراسة الذرة أسهل وأدق. فعن استخدام الميكروسكوب الإلكتروني الذي تم اكتشافه في عام 1931 تم تصوير ذرات مفردة. كما تم استحداث طرق جديدة للتعرف على الذرات والمركبات. فمثلا يتم استخدام مطياف الكتلة لتحديد الذرات والمركبات. كما يتم استخدام جي سي إم إس " كروماتوجرافى الغاز ومطياف الكتلة " لمعرفة المواد. وأيضا التأكد من وجود ذرات أو جزيئات معينة عن طريق أشعة إكس كريستالوجرافى.
الذرة في الصناعة
تقوم الذرة بدور غاية في الأهمية في الصناعة، يتضمن ذلك الصناعات النووية، علم المواد الصناعية، وأيضا في الصناعات الكيميائية.
#BASSANT
مزيج
المزيج أو المخلوط هو مادة كيميائية متجانسة أو غير متجانسة ممتزجة بدون روابط كيميائية بين العناصر الكيميائية أو المركبات الكيميائية فيها والتي قد تكون موجودة بنسب مختلفة ، وبالتالي يحتفظ كل بخواصه وشكله، ويمكن فصل المخاليط بالطرق الكيميائية والفزيائية.
لا يوجد تغييرات كيميائية في المزائج ، أى أن كل مادة موجودة في المزيج تحتفظ بخواصها الفردية وشكلها السابق قبل وضعها في المخلوط . ولكن الخواص الفيزيائية قد تتغير قليلا ، قمثلا تتغير درجة الانصهار للمخلوط عن درجات حرارة مكوناته الفردية .
المزيج المتجانس هي المزائج التي لها تركيب وخواص محددة ، أى أن أى كمية من المخلوط لها نفس التركيب والخواص . مثال لذلك المحاليل وبعض السبائك ( ولكن ليس كلها ).
المزيج اللا متجانس هي المزائج التي لا يكون لها تركيب محدد ، مثال الجرانيت . وتكون البيتزا مثال جيد للمزائج اللا متجانسة . ويقال على المزائج اللا متجانسة أن لها حالات عديدة ( ولا يجب الخلط بين ذلك وبين حالة المادة ), أى أنه يمكن فصل أجزاء من المزيج بالطرق الكيميائية.
#BASSANT
.
لا يوجد تغييرات كيميائية في المزائج ، أى أن كل مادة موجودة في المزيج تحتفظ بخواصها الفردية وشكلها السابق قبل وضعها في المخلوط . ولكن الخواص الفيزيائية قد تتغير قليلا ، قمثلا تتغير درجة الانصهار للمخلوط عن درجات حرارة مكوناته الفردية .
المزيج المتجانس هي المزائج التي لها تركيب وخواص محددة ، أى أن أى كمية من المخلوط لها نفس التركيب والخواص . مثال لذلك المحاليل وبعض السبائك ( ولكن ليس كلها ).
المزيج اللا متجانس هي المزائج التي لا يكون لها تركيب محدد ، مثال الجرانيت . وتكون البيتزا مثال جيد للمزائج اللا متجانسة . ويقال على المزائج اللا متجانسة أن لها حالات عديدة ( ولا يجب الخلط بين ذلك وبين حالة المادة ), أى أنه يمكن فصل أجزاء من المزيج بالطرق الكيميائية.
#BASSANT
.
احببت ان اريكم الفرق بين المركبات والمخاليط
نبدأ بالمخاليط
ما هي المخاليط ؟
المخاليط هي : مزيج مكون من مادتين نقيتين او اكثر مع
احتفاظ كل من هذي المواد بخواصها الاصليه.
وتنقسم المخاليط الى قسمين هما :-
1-المخلوط الغير متجانس . مثال:-
سلطة الخضار والماء مع التراب و الملح مع السكر
ويمكن فصلها بطرقه سهله.
2-المخاليط المتجانسه . مثال:-
الشاهي و السكر في الماء و ملح الطعام في الماء
----------------------------------------------
باختصار
المخاليط الغير متجانسه:-
لا تذوب في المحلول بل تضهر على شكلها الاصلي ولا تفقد خواصها
المخاليط المتجانسه
تذوب وتختفي في الملحول لكنها لا تفقد خواصها بل تحتفظ بها
---------------------------------------------
فصل المخاليط ؟
هل يمكن فصل المخاليط ؟
نعم يمكن وبعدة طرق وهي
1-الترشيح
2-التقطير
3-التبلور
4-التسامي
5-الكروماتوجرافيا
سنشرحها في موضوع مستقل ^^
انتهينا من المخاليط .
نبدأ في المركبات
ما هي المركبات ؟
المركب هو عباره عن عنصرين او اكثر متحدين معا اتحادا كيميائياً
من خواص المركبات
1- تختلف خواص العنصر عند اتحاده مع عنصر اخر مثال:-
ملح الطعام بكون من كلوريد وهي ماده سامه + الصوديوم وهي ايضا ماده سامه
وكونت ملح الطعام ماده نقيه ليست سامه مثل عناصرها
2-يصعب فصل العناصر المركبه الا بالطرق كيميائيه صعبه سنشرحها في موضوع مستقل
عذرا على الاطاله
نتمنى ان استفدتم من الموضوع لانه متعوب عليه
كتبته بيدي ليس منقولا لكي يكون واضحا ومختصرا
تحياتي
#BASSANT
نبدأ بالمخاليط
ما هي المخاليط ؟
المخاليط هي : مزيج مكون من مادتين نقيتين او اكثر مع
احتفاظ كل من هذي المواد بخواصها الاصليه.
وتنقسم المخاليط الى قسمين هما :-
1-المخلوط الغير متجانس . مثال:-
سلطة الخضار والماء مع التراب و الملح مع السكر
ويمكن فصلها بطرقه سهله.
2-المخاليط المتجانسه . مثال:-
الشاهي و السكر في الماء و ملح الطعام في الماء
----------------------------------------------
باختصار
المخاليط الغير متجانسه:-
لا تذوب في المحلول بل تضهر على شكلها الاصلي ولا تفقد خواصها
المخاليط المتجانسه
تذوب وتختفي في الملحول لكنها لا تفقد خواصها بل تحتفظ بها
---------------------------------------------
فصل المخاليط ؟
هل يمكن فصل المخاليط ؟
نعم يمكن وبعدة طرق وهي
1-الترشيح
2-التقطير
3-التبلور
4-التسامي
5-الكروماتوجرافيا
سنشرحها في موضوع مستقل ^^
انتهينا من المخاليط .
نبدأ في المركبات
ما هي المركبات ؟
المركب هو عباره عن عنصرين او اكثر متحدين معا اتحادا كيميائياً
من خواص المركبات
1- تختلف خواص العنصر عند اتحاده مع عنصر اخر مثال:-
ملح الطعام بكون من كلوريد وهي ماده سامه + الصوديوم وهي ايضا ماده سامه
وكونت ملح الطعام ماده نقيه ليست سامه مثل عناصرها
2-يصعب فصل العناصر المركبه الا بالطرق كيميائيه صعبه سنشرحها في موضوع مستقل
عذرا على الاطاله
نتمنى ان استفدتم من الموضوع لانه متعوب عليه
كتبته بيدي ليس منقولا لكي يكون واضحا ومختصرا
تحياتي
#BASSANT
انواع المواد ~مدخل الي العناصر و المركبات و المخاليط ..
سؤال : لماذا قلنا ثمانين عنصراً ولم نقل المائة كلها ؟
أشرنا في المقدمة إلى أن كل شيء في الكون يكاد يكون مخلوطاً بسيطاً أو معقداً ، فالبكتيريا المجهرية والكائنات الحية الكبيرة والمعقدة ، والأرض والنجوم والمجرات كلها مخاليط .
يمكن أن نسمي هذه المخاليط باسم المخاليط الطبيعية ، ومن بعض هذه المخاليط الطبيعية يأخذ الإنسان حاجته من المواد وينقيها إذا احتاجت إلى تنقية ، وفوق هذا كله يقوم بنفسه بعمل الكثير من المخلوطات حسب ما يحتاجه ، فيعمل العجين ، والخرسانة ، والفولاذ ، والأدوات الكهربائية والسيارات والطائرات ... يمكن أن نطلق على هذه المخلوطات اسم المخلوطات الصناعية تمييزاً لها عن المخلوطات الطبيعية التي لا يتدخل الإنسان في صنعها .
تصنف المخاليط بطريقة أخرى اعتماداً على مظهرها في فئتين هما :
1. المخاليط غير المتجانسة :
وهي مخاليط يمكن مشاهدة بعض أو كل مكوناتها بالعين المجردة أو بعدسة مكبرة أو بمجهر عادي ومن الأمثلة على هذه المخاليط : مخلوط البزر والفستق ، وصخر الغرانيت ، وورق الشجر ، والكرتون ، والحليب ، والدم .
للمناقشة : أي الأمثلة أعلاه تظهر متجانسة بالعين المجردة !
2. المخاليط المتجانسة :
وهي مخاليط لا يمكن مشاهدة أحد مكوناتها متميزاً عن المكونات الأخرى حتى بالمجهر الإلكتروني ونحن نسمي هذه الفئة من المخاليط باسم المحاليل الحقيقية أو باختصار المحاليل ومن أمثلتها : الهواء وهو محلول غازي ، ومحلول ملح الطعام في الماء وهو محلول سائل وقطع النقود المعدنية وهي محاليل صلبة تتكون الواحدة منها من عدة فلزات ممتزجة مع بعضها . جزيئات هذه المخاليط متجانسة على الرغم من وجود عدة أنواع منها ( أي من الجزيئات ) في المخلوط الواحد .
تدريبات :
1. صنف المواد التالية إلى مخاليط متجانسة ومخاليط غير متجانسة :ورقة بيضاء ـ خميرة العجين ـ سكر مذاب في الماء ـ الزعتر مع الزيت ـ محلول حمض الكبريتيك ـ اللبن ـ الفولاذ ـ خرسانة مسلحة ، ذهب عيار 21 ـ العدس الحب مع الأرز ـ كحول وماء ـ السلطة ـ الكرة الأرضية ـ العطر ـ قطعة البرونز .
2. اضرب ثلاثة أمثلة لمخاليط يتغير تركيبها حسب الظروف .
3. اضرب خمسة أمثلة لمخاليط يتحكم الإنسان بنسب المواد المكونة لها .
4. سعر لتر الكحول 96% هو (2) دينار ، وسعر لتر من الكحول المطلق ( نسبته حوالي 99.95 % ) هو (15) ديناراً ، ما سبب هذا الفرق في السعر ؟؟؟
المركبات الكيميائية :
العناصر المعروفة حتى الآن حوالي المائة ، والشائع والمستخدم منها في الحياة العملية حوالي النصف ، فمن أين يأتي هذا العدد الهائل من المواد والذي يقدر بالملايين ؟ وأنت لو حاولت أن تعد المواد التي تعرفها لوجدت أنه قائمتك تحتوي على الآلاف منها .
الجواب عن تساؤلنا عن عدد المواد الكبير يكمن في أن العناصر ترتبط مع بعضها بعلاقات مختلفة مكونة عدداً هائلاً من المركبات ومنها ما هو معروف ومألوف لديك كالماء وثاني أوكسيد الكربون ، وملح الطعام ... الخ.
يتكون المركب من اتحاد عنصرين أو أكثر بنسب وزنية ثابتة .
المركبات هي النوع الثاني من أنواع المادة وهي تتكون من جزيئات متشابهة ، إلا أن هذه الجزيئات قابلة للتحليل ، فإذا حللنا الماء حصلنا على جزيئات الهيدروجين وجزيئات الأوكسيجين وتحليل ملح الطعام يعطينا جزيئات مكونيه وهما عنصر الصوديوم والكلور .
سؤال :
ـ ما الفرق بين جزيئات العناصر وجزيئات المركبات ؟
ـ ما أوجه الشبه بين جزيئات العناصر وجزيئات المركبات ؟
لكن أمر المواد لا يتوقف عند العناصر والمركبات ، فالعناصر والمركبات قد ترتبط مع بعضها بنسب وزينة غير ثابتة منتجة مواد من نوع جديد نسميها المخاليط ، بل إن العناصر والمركبات والمخاليط تمتزج لتكون مخاليط جديدة ، ومن المخاليط ذات الأهمية الهواء وماء البحر والصخور.
لا شك أنك أدركت الآن أن ملايين المواد من مركبات ومخاليط منشؤها في الأساس هو حوالي ثمانين عنصراً من العناصر المائة المعروفة .
مقارنة بين أنواع المواد وبين اللغة بحروفها وكلماتها :
يوجد الكثير من المركبات المختلفة التي تتكون من نفس العناصر ، فمثلاً الكربون يكون باتحاده مع عدد قليل من العناصر المعروفة ملايين المركبات ، تسمى هذه المركبات باسم المركبات العضوية ، وهناك فرع من فروع الكيمياء يدرس هذه المركبات وخواصها وعلاقاتها اسمه الكيمياء العضوية . المركبات العضوية ذات أهمية بالغة للحياة من أمثلتها الهرمونات والفيتامينات والأنزيمات والبروتينات والسكاكر والنشويات وهي مواد ضرورية للحياة ومعظمها يصنعها النبات ومنذ حوالي القرن بدأ الإنسان يستخرج ويصنع بعض المواد العضوية من البترول ومشتقاته ومن الغاز الطبيعي لأن البترول والغاز الطبيعي غنية بالمواد العضوية ، وتسمى هذه الصناعات باسم عام هو البتروكيماويات أي الصناعات الكيميائية المعتمدة على النفط وينتج عنها في أيامنا هذه على سبيل المثال : الأقمشة بأنواعها ، والسجاد بأنواعه ،والبلاط الصناعي ، والبلاستيك ، وقطع السيارات وهياكلها ، وهياكل الأدوات الكهربائية كالثلاجات والغسالات والمسجلات ، والعلاجات الطبية ، والأغذية الصناعية والمواد المضادة للحريق ... والقائمة تطول ويصعب حصرها .
للمناقشة :
يوجد ملايين المركبات تتكون من الهيدروجين والكربون فقط وتعرف باسم الفحوم الهيدروجينية ( الهيدروكربونات ) . ويتزعم هذه الطائفة مركب معروف هو الميثان ، سؤال : ما صيغة الميثان ؟ ما العناصر التي يتكون منها ؟
ويوجد الكثير الكثير من المركبات التي تتكون من ثلاث عناصر هي الكربون والهيدروجين والأوكسيجين نذكر لك منها : السكر بأنواعه ، النشاء بأنواعه ، والسيلولوز ، والمركب الأساسي في زيت الزيتون وأنواع الزيوت والدهون والخل ، والكحول والأسيتون وقائمة أخرى طويلة، كيف تفسر ذلك ؟
#BASSANT
أشرنا في المقدمة إلى أن كل شيء في الكون يكاد يكون مخلوطاً بسيطاً أو معقداً ، فالبكتيريا المجهرية والكائنات الحية الكبيرة والمعقدة ، والأرض والنجوم والمجرات كلها مخاليط .
يمكن أن نسمي هذه المخاليط باسم المخاليط الطبيعية ، ومن بعض هذه المخاليط الطبيعية يأخذ الإنسان حاجته من المواد وينقيها إذا احتاجت إلى تنقية ، وفوق هذا كله يقوم بنفسه بعمل الكثير من المخلوطات حسب ما يحتاجه ، فيعمل العجين ، والخرسانة ، والفولاذ ، والأدوات الكهربائية والسيارات والطائرات ... يمكن أن نطلق على هذه المخلوطات اسم المخلوطات الصناعية تمييزاً لها عن المخلوطات الطبيعية التي لا يتدخل الإنسان في صنعها .
تصنف المخاليط بطريقة أخرى اعتماداً على مظهرها في فئتين هما :
1. المخاليط غير المتجانسة :
وهي مخاليط يمكن مشاهدة بعض أو كل مكوناتها بالعين المجردة أو بعدسة مكبرة أو بمجهر عادي ومن الأمثلة على هذه المخاليط : مخلوط البزر والفستق ، وصخر الغرانيت ، وورق الشجر ، والكرتون ، والحليب ، والدم .
للمناقشة : أي الأمثلة أعلاه تظهر متجانسة بالعين المجردة !
2. المخاليط المتجانسة :
وهي مخاليط لا يمكن مشاهدة أحد مكوناتها متميزاً عن المكونات الأخرى حتى بالمجهر الإلكتروني ونحن نسمي هذه الفئة من المخاليط باسم المحاليل الحقيقية أو باختصار المحاليل ومن أمثلتها : الهواء وهو محلول غازي ، ومحلول ملح الطعام في الماء وهو محلول سائل وقطع النقود المعدنية وهي محاليل صلبة تتكون الواحدة منها من عدة فلزات ممتزجة مع بعضها . جزيئات هذه المخاليط متجانسة على الرغم من وجود عدة أنواع منها ( أي من الجزيئات ) في المخلوط الواحد .
تدريبات :
1. صنف المواد التالية إلى مخاليط متجانسة ومخاليط غير متجانسة :ورقة بيضاء ـ خميرة العجين ـ سكر مذاب في الماء ـ الزعتر مع الزيت ـ محلول حمض الكبريتيك ـ اللبن ـ الفولاذ ـ خرسانة مسلحة ، ذهب عيار 21 ـ العدس الحب مع الأرز ـ كحول وماء ـ السلطة ـ الكرة الأرضية ـ العطر ـ قطعة البرونز .
2. اضرب ثلاثة أمثلة لمخاليط يتغير تركيبها حسب الظروف .
3. اضرب خمسة أمثلة لمخاليط يتحكم الإنسان بنسب المواد المكونة لها .
4. سعر لتر الكحول 96% هو (2) دينار ، وسعر لتر من الكحول المطلق ( نسبته حوالي 99.95 % ) هو (15) ديناراً ، ما سبب هذا الفرق في السعر ؟؟؟
المركبات الكيميائية :
العناصر المعروفة حتى الآن حوالي المائة ، والشائع والمستخدم منها في الحياة العملية حوالي النصف ، فمن أين يأتي هذا العدد الهائل من المواد والذي يقدر بالملايين ؟ وأنت لو حاولت أن تعد المواد التي تعرفها لوجدت أنه قائمتك تحتوي على الآلاف منها .
الجواب عن تساؤلنا عن عدد المواد الكبير يكمن في أن العناصر ترتبط مع بعضها بعلاقات مختلفة مكونة عدداً هائلاً من المركبات ومنها ما هو معروف ومألوف لديك كالماء وثاني أوكسيد الكربون ، وملح الطعام ... الخ.
يتكون المركب من اتحاد عنصرين أو أكثر بنسب وزنية ثابتة .
المركبات هي النوع الثاني من أنواع المادة وهي تتكون من جزيئات متشابهة ، إلا أن هذه الجزيئات قابلة للتحليل ، فإذا حللنا الماء حصلنا على جزيئات الهيدروجين وجزيئات الأوكسيجين وتحليل ملح الطعام يعطينا جزيئات مكونيه وهما عنصر الصوديوم والكلور .
سؤال :
ـ ما الفرق بين جزيئات العناصر وجزيئات المركبات ؟
ـ ما أوجه الشبه بين جزيئات العناصر وجزيئات المركبات ؟
لكن أمر المواد لا يتوقف عند العناصر والمركبات ، فالعناصر والمركبات قد ترتبط مع بعضها بنسب وزينة غير ثابتة منتجة مواد من نوع جديد نسميها المخاليط ، بل إن العناصر والمركبات والمخاليط تمتزج لتكون مخاليط جديدة ، ومن المخاليط ذات الأهمية الهواء وماء البحر والصخور.
لا شك أنك أدركت الآن أن ملايين المواد من مركبات ومخاليط منشؤها في الأساس هو حوالي ثمانين عنصراً من العناصر المائة المعروفة .
مقارنة بين أنواع المواد وبين اللغة بحروفها وكلماتها :
يوجد الكثير من المركبات المختلفة التي تتكون من نفس العناصر ، فمثلاً الكربون يكون باتحاده مع عدد قليل من العناصر المعروفة ملايين المركبات ، تسمى هذه المركبات باسم المركبات العضوية ، وهناك فرع من فروع الكيمياء يدرس هذه المركبات وخواصها وعلاقاتها اسمه الكيمياء العضوية . المركبات العضوية ذات أهمية بالغة للحياة من أمثلتها الهرمونات والفيتامينات والأنزيمات والبروتينات والسكاكر والنشويات وهي مواد ضرورية للحياة ومعظمها يصنعها النبات ومنذ حوالي القرن بدأ الإنسان يستخرج ويصنع بعض المواد العضوية من البترول ومشتقاته ومن الغاز الطبيعي لأن البترول والغاز الطبيعي غنية بالمواد العضوية ، وتسمى هذه الصناعات باسم عام هو البتروكيماويات أي الصناعات الكيميائية المعتمدة على النفط وينتج عنها في أيامنا هذه على سبيل المثال : الأقمشة بأنواعها ، والسجاد بأنواعه ،والبلاط الصناعي ، والبلاستيك ، وقطع السيارات وهياكلها ، وهياكل الأدوات الكهربائية كالثلاجات والغسالات والمسجلات ، والعلاجات الطبية ، والأغذية الصناعية والمواد المضادة للحريق ... والقائمة تطول ويصعب حصرها .
للمناقشة :
يوجد ملايين المركبات تتكون من الهيدروجين والكربون فقط وتعرف باسم الفحوم الهيدروجينية ( الهيدروكربونات ) . ويتزعم هذه الطائفة مركب معروف هو الميثان ، سؤال : ما صيغة الميثان ؟ ما العناصر التي يتكون منها ؟
ويوجد الكثير الكثير من المركبات التي تتكون من ثلاث عناصر هي الكربون والهيدروجين والأوكسيجين نذكر لك منها : السكر بأنواعه ، النشاء بأنواعه ، والسيلولوز ، والمركب الأساسي في زيت الزيتون وأنواع الزيوت والدهون والخل ، والكحول والأسيتون وقائمة أخرى طويلة، كيف تفسر ذلك ؟
#BASSANT
يمكن إعطاء تفسير وتقريبه من أذهان الدارسين إذا عقدنا مقارنة بين اللغة العربية من جهة والكيمياء من جهة أخرى .
الكيمياء
اللغة العربية
عدد العناصر حوالي مئة والشائع والنشط منها والذي يكون المركبات حوالي ثمانين .
عدد الحروف 28 حرفاً.
تتحد العناصر مع بعضها طبيعياً وبدون تدخل الإنسان وصناعياً يتدخل الإنسان وتكون عدداً كبيراً من المركبات يقدر حتى الآن ببضعة ملايين .
نستخدم حروف الهجاء في تكوين الكلمات وينتج عن ذلك عدد لا يحصى من الكلمات : وهي تقدر بالملايين .
يوجد مركبان لهما نفس الصيغة البسيطة C2H6O أحدهما الكحول المعروف والمستخدم للتعقيم . يوجد ثلاث مركبات مختلفة تجمعها الصيغة C5H12
تتغير الكلمات بتغير ترتيب حروفها مثل :جَمَعَ ، عَجَمَ ، سفيرة ، فريسة ، تفسير ، تسفير ... الخ .
كثير من المركبات لها نفس الصيغة ونفس الربط ولكنها تختلف في شكلها الفراغي تماماً كالكلمات التي تغير معانيها بتغيير الحركات أو حتى ببقائها على حركاتها كما هي .
تتغير الكلمات بتغيير حركة بعض الحروف مثل :
قَرْبَ ، قِرَب ، قُرْب .
جَمال ، جِمال ، عَلَم ، عِلْم ، عَلِمَ .
وقد يكون للكلمة الواحدة أكثر من معنى مثل :حمل ، البيان ، رقّ .
يكون الحديد مع الأوكسيجين ثلاثة أكاسيد هي :FeO , Fe2O3 , Fe3O4
أما الكربون والهيدروجين فتكون مجموعة كبيرة من المركبات تسمى الفحوم الهيدروجينية ( الهيدروكربونات ) مثل :CH4 , C2H6 , C3H8 , C4H10,C5H12,…
تتغير الكلمات بتغير الحركات وترتيب الحروف وعددها مثل : رِماح ، رَمّاح .
أقسام ، قسّام .
جمّال ، جَمال ، جِمال .
تجتمع العناصر والمركبات والمخاليط مع بعضها لتكون مخاليط ،مثلاً نمزج الحديد والنحاس والفضة لتحصل على عملة معدنية . الصخور مخاليط طبيعية مكونة من عدة مركبات .
تجتمع الحروف والكلمات لتكون جملاً مختلفة .
اجتمع الرياضيون في الساحة وقاموا بالألعاب .
وخلاصة القول :
حروف الهجاء في اللغة تقابل العناصر في الكيمياء .
تتكون ملايين المركبات من عدد محدود من حروف الهجاء ( الـ 28) ،وملايين المركبات تنتج المخاليط عن اتحاد عدد قليل من العناصر
( المائة ) .
الكلمات في اللغة تقابل المركبات في الكيمياء
#BASSANT
قانون النسب الثابتة
قانون النسب الثابتة أو التركيب المحدد ويسمى بالإنجليزية (Law of composition or Definite proportions)أكمل الفرنسي (بروست)دراسات أنطوان لافوازييه بعد وفاته وتبين له’ أن المركبات تحتوي على نسب ثابتة من العناصر المكونة لها’ ولاتتغير هذه النسب مهما اختلفت طرق تحضير المركب.فمثلا ملح الطعام النقي سواء حصلنا عليه من مياه البحار أو تم تحضيره من تفاعل كميائي’ فإنه يحتوي دائما على 39,3% من كتلته الصوديوم و60,7% من كتلته كلور ومن خلاصة أبحاث متعددة توصل بروست إلى القانون الذي ينص على أنه: يتألف كل مركب كميائي نقي من نسب وزنية ثابتة للعناصر المكونة له مهما اختلفت طرق تحضيره و هذا الأمر يتم حسابه عبر الكتلة الذرية الموجودة في الجدول الدوري A.G.R
#BASSANT
قانون النسب الثابتة أو التركيب المحدد ويسمى بالإنجليزية (Law of composition or Definite proportions)أكمل الفرنسي (بروست)دراسات أنطوان لافوازييه بعد وفاته وتبين له’ أن المركبات تحتوي على نسب ثابتة من العناصر المكونة لها’ ولاتتغير هذه النسب مهما اختلفت طرق تحضير المركب.فمثلا ملح الطعام النقي سواء حصلنا عليه من مياه البحار أو تم تحضيره من تفاعل كميائي’ فإنه يحتوي دائما على 39,3% من كتلته الصوديوم و60,7% من كتلته كلور ومن خلاصة أبحاث متعددة توصل بروست إلى القانون الذي ينص على أنه: يتألف كل مركب كميائي نقي من نسب وزنية ثابتة للعناصر المكونة له مهما اختلفت طرق تحضيره و هذا الأمر يتم حسابه عبر الكتلة الذرية الموجودة في الجدول الدوري A.G.R
#BASSANT
جون دالتون
حياته
ولد عالم الكيمياء جون دالتون في قرية إنكليزية صغيرة تدعى (ايكزفيلد كمبرلاند) نشأ في اسرة فقيرة كان أبوه نساجا وتوفي اثنان من اخوته جوعا وبردا، لمع منذ اعوامه الدراسية الأولى في الرياضيات وحل مسائل رياضية معقدة وفي الخامسة عشرة من عمره أصبح استاذا في مدرسة القرية ثم تركها وانتقل إلى كندال العام 1781 حيث عمل مدرساً أيضا.
جند دالتون مرصدا صغيرا لمراقبة الأحوال الجوية ووضع جداول لتسجيل المعطيات اليومية لكل من الضغط الجوي وكمية المطر والرطوبة والرياح وغيرها.
تعلم دالتون على يد العلامة الضرير جون هوف اللغة اليونانية واللاتينية والفرنسية والرياضيات ونال اعجابه وتقدير زملائه وسكان المدينة. قام بكتابة مقالات في مجلة لتبسيط العلوم ودرس المذهب الطبيعي في الفلسفة في الكلية الجديدة في مانشستر وكندال في آن واحد معا. ثم انتقل كليا إلى مانشستر العام 1793.
الوسام الذهبي
زار دالتون لندن سنة 1809 والتقى بكبار العلماء فيها، فعرضوا عليه دخول الجمعية الملكية لكنه رفض لتعلقه بمانشستر، عينته أكاديمية العلوم الفرنسية عضوا مراسلا وأصبح رئيسا للجمعية الادبية والفلسفية من مانشستر العام 1817 وفي العام 1822 سافر بعدها إلى باريس والتقى جميع العلماء لاسيما بالعالم غي لوساك. ثم عاد إلى مانشستر ووضع جدولا للاوزان الذرية لمعظم العناصر وكان يقوم بتجديده دائما وفي سنة 1826 منحته الحكومة الإنكليزية وساما ذهبيا تقديرا لاكتشافاته في الكيمياء والفيزياء ومنحته بلدية مانشستر لقب مواطن شرف واقامت له تمثالا في أكبر قاعاتها Town-Hall.
النظرية الذرية
يعتبر دالتون أبا للكيمياء الحديثة وذلك بعد أن اقترح النظرية الذرية للمادة حوالي العام 1803 ان نظرية دالتون تعتمد على قوانين بقاء الكتلة والنسب الثابتة والتي اشتقت من العديد من الاستنتاجات المباشرة، تتكون المادة من العديد من الجسيمات الغير قابلة للتجزئة تسمى الذرات، اما محتوى نظرية دالتون هو ان المادة تتكون من العديد من الجسيمات غير القابلة للتجزئة تسمى الذرات إضافة إلى ان كل ذرات العنصر تتميز بنفس الخواص (الحجم - الشكل - الكتلة) والتي تختلف باختلاف العناصر. كما أن التفاعل الكيميائي يحدث عند تبديل وضعية الذرات وتحويلها من منظومة لأخرى.
لقد اثبت نجاح نظرية دالتون عبر تفسيرها لبعض الحقائق القائمة في ذلك الوقت كما أنها استطاعت أيضا التنبؤ ببعض القوانين غير المكتشفة.
1- تضمنت هذه النظرية قانون حفظ الكتلة حيث ان التفاعل الكيميائي لايفعل شيئا سوى اعادة توزيع الذرات ولم تفقد اي ذرة في هذه المنظومة وبالتالي تظل الكتلة ثابتة عند حدوث التفاعل.
2- فسرت نظرية دالتون قانون النسب الثابتة بافتراضها ان المادة تتكون من عنصرين B,A وان اي جزيء من هذه المادة يتكون من ذرة واحدة من A وذرة واحدة من B (يعرف من الجزيء بانه مجموعة ذرات مترابطة مع بعضها بقوة تسمح لها بالتصرف أو اعادة التنظيم كجسيم واحد كما افترض أيضا ان كتلة الذرة A تكون ضعف كتلة الذرة B وبالتالي فان الذرة A تساهم بضعف الكتلة التي تساهم بها الذرة B في تكوين جزيئي واحد من هذه المادة الامر الذي يعني ان نسبة كتلة الذرة A إلى الذرة B هي ½. اما إذا اخذنا مجموعة كبيرة من جزيئات هذه المادة فاننا نجد دائما ان عدد ذرات A مساو لعدد ذرات B الامر الذي يعني انه بغض النظر عن حجم العينة فاننا نحصل دائماً على نسبة كتلة B-A تساوي ½ وبالمثل إذا فاعلنا A مع B لنحصل على هذا الجزيئي سنجد ان اي ذرة من A تتحد مع ذرة واحدة من B اما إذا خلطنا 100 ذرة من A مع 110 ذرة من B نجد انه قد تبقت 10 ذرات من B غير متفاعلة بعد اكتمال التفاعل.
تنبأت نظرية دالتون بقانون النسب المتضاعفة: عند تكوين مركبين مختلفين من نفس العنصرين فان كتلتي أحد العنصرين اللتين تتفاعلان مع كتلة ثابتة من العنصر الاخر تكونان في شكل نسبة عددين بسيطين وصحيحين.
انجازاته العلمية
حياته
ولد عالم الكيمياء جون دالتون في قرية إنكليزية صغيرة تدعى (ايكزفيلد كمبرلاند) نشأ في اسرة فقيرة كان أبوه نساجا وتوفي اثنان من اخوته جوعا وبردا، لمع منذ اعوامه الدراسية الأولى في الرياضيات وحل مسائل رياضية معقدة وفي الخامسة عشرة من عمره أصبح استاذا في مدرسة القرية ثم تركها وانتقل إلى كندال العام 1781 حيث عمل مدرساً أيضا.
جند دالتون مرصدا صغيرا لمراقبة الأحوال الجوية ووضع جداول لتسجيل المعطيات اليومية لكل من الضغط الجوي وكمية المطر والرطوبة والرياح وغيرها.
تعلم دالتون على يد العلامة الضرير جون هوف اللغة اليونانية واللاتينية والفرنسية والرياضيات ونال اعجابه وتقدير زملائه وسكان المدينة. قام بكتابة مقالات في مجلة لتبسيط العلوم ودرس المذهب الطبيعي في الفلسفة في الكلية الجديدة في مانشستر وكندال في آن واحد معا. ثم انتقل كليا إلى مانشستر العام 1793.
الوسام الذهبي
زار دالتون لندن سنة 1809 والتقى بكبار العلماء فيها، فعرضوا عليه دخول الجمعية الملكية لكنه رفض لتعلقه بمانشستر، عينته أكاديمية العلوم الفرنسية عضوا مراسلا وأصبح رئيسا للجمعية الادبية والفلسفية من مانشستر العام 1817 وفي العام 1822 سافر بعدها إلى باريس والتقى جميع العلماء لاسيما بالعالم غي لوساك. ثم عاد إلى مانشستر ووضع جدولا للاوزان الذرية لمعظم العناصر وكان يقوم بتجديده دائما وفي سنة 1826 منحته الحكومة الإنكليزية وساما ذهبيا تقديرا لاكتشافاته في الكيمياء والفيزياء ومنحته بلدية مانشستر لقب مواطن شرف واقامت له تمثالا في أكبر قاعاتها Town-Hall.
النظرية الذرية
يعتبر دالتون أبا للكيمياء الحديثة وذلك بعد أن اقترح النظرية الذرية للمادة حوالي العام 1803 ان نظرية دالتون تعتمد على قوانين بقاء الكتلة والنسب الثابتة والتي اشتقت من العديد من الاستنتاجات المباشرة، تتكون المادة من العديد من الجسيمات الغير قابلة للتجزئة تسمى الذرات، اما محتوى نظرية دالتون هو ان المادة تتكون من العديد من الجسيمات غير القابلة للتجزئة تسمى الذرات إضافة إلى ان كل ذرات العنصر تتميز بنفس الخواص (الحجم - الشكل - الكتلة) والتي تختلف باختلاف العناصر. كما أن التفاعل الكيميائي يحدث عند تبديل وضعية الذرات وتحويلها من منظومة لأخرى.
لقد اثبت نجاح نظرية دالتون عبر تفسيرها لبعض الحقائق القائمة في ذلك الوقت كما أنها استطاعت أيضا التنبؤ ببعض القوانين غير المكتشفة.
1- تضمنت هذه النظرية قانون حفظ الكتلة حيث ان التفاعل الكيميائي لايفعل شيئا سوى اعادة توزيع الذرات ولم تفقد اي ذرة في هذه المنظومة وبالتالي تظل الكتلة ثابتة عند حدوث التفاعل.
2- فسرت نظرية دالتون قانون النسب الثابتة بافتراضها ان المادة تتكون من عنصرين B,A وان اي جزيء من هذه المادة يتكون من ذرة واحدة من A وذرة واحدة من B (يعرف من الجزيء بانه مجموعة ذرات مترابطة مع بعضها بقوة تسمح لها بالتصرف أو اعادة التنظيم كجسيم واحد كما افترض أيضا ان كتلة الذرة A تكون ضعف كتلة الذرة B وبالتالي فان الذرة A تساهم بضعف الكتلة التي تساهم بها الذرة B في تكوين جزيئي واحد من هذه المادة الامر الذي يعني ان نسبة كتلة الذرة A إلى الذرة B هي ½. اما إذا اخذنا مجموعة كبيرة من جزيئات هذه المادة فاننا نجد دائما ان عدد ذرات A مساو لعدد ذرات B الامر الذي يعني انه بغض النظر عن حجم العينة فاننا نحصل دائماً على نسبة كتلة B-A تساوي ½ وبالمثل إذا فاعلنا A مع B لنحصل على هذا الجزيئي سنجد ان اي ذرة من A تتحد مع ذرة واحدة من B اما إذا خلطنا 100 ذرة من A مع 110 ذرة من B نجد انه قد تبقت 10 ذرات من B غير متفاعلة بعد اكتمال التفاعل.
تنبأت نظرية دالتون بقانون النسب المتضاعفة: عند تكوين مركبين مختلفين من نفس العنصرين فان كتلتي أحد العنصرين اللتين تتفاعلان مع كتلة ثابتة من العنصر الاخر تكونان في شكل نسبة عددين بسيطين وصحيحين.
انجازاته العلمية
- نشر عدداً من الأبحاث في تفنيد السيمياء (الكيمياء القديمة).
- النظرية الذرية في الكيمياء.
- محاضرات في عمى الألوان.
- من أهم مؤلفاته نظام جديد للفلسفة الكيميائية سنة 1808.
- #BASSANT
جوزيف جون طومسون
جوزيف جون طومسون (18 ديسمبر 1856 - 30 أغسطس 1940)، عالم إنجليزي ولد بالقرب من مدينة مانشستر الإنجليزية، وتفوق في دراسته منذ الصغر حتى أنه التحق بكلية الهندسة بجامعة فيكتوريا مانشستر وهو في الرابعة عشر من عمره، ثم حصل على منحة من جامعة كامبريدج حيث تخصص في حقل الفيزياء النظرية.
ثم اتجه طومسون للعمل في معمل كافندش العريق، وفي عام 1884 م تم تعيينه رئيساً لمعمل كافندش وهو في الثامنة والعشرين من عمره، وقد ترأس المعمل لمدة 34 عاما حتى خلفه تلميذه النيوزلندي ارنست رذرفورد.
يعتبر اكتشافه للإلكترون أفضل بحوثه على الإطلاق وأكثرها شهرةً وتأثيراً، حيث قادته تجاربه على أشعة المهبط (أو أشعة الكاثود) إلى اكتشاف الخواص الأساسيةللإلكترون. حيث قام بتعريض غاز مخلخل لتيار كهربائي فرق جهده حوالي 10,000 فولت تحت ضغط منخفض يتراوح من 0.0001 إلى 0.01 مم/زئبق فلاحظ انطلاق أشعة من الكاثود (مهبط) إلي الآنود (مصعد) وهي أشعة غير منظورة لكنها تحدث توهجاً على جدار أنبوبة التفريغ، وأثبت أن أشعة المهبط ليست أشعة ولكنها سيل متصل من الجسيمات سالبة الشحنة تتأثر بالمجال الكهربي والمجال المغناطيسي وتنحرف طبقاً لشدة مجال كل منهما، كما تمكن من حساب سرعة تلك الجسيمات، لذا فقد اشتهر بلقب ""أبو الإلكترون"".
حصل طومسون على جائزة نوبل عام 1906 م لاكتشافه الإلكترون، ثم ترك العمل في معمل كافندش قرب نهاية الحرب العالمية الأولى وترأس كلية ترينيتي فيكامبريدج، وظل هناك حتى توفي 1940 م عن عمر يناهز الرابعة والثمانين.
#BASSANT
جوزيف جون طومسون (18 ديسمبر 1856 - 30 أغسطس 1940)، عالم إنجليزي ولد بالقرب من مدينة مانشستر الإنجليزية، وتفوق في دراسته منذ الصغر حتى أنه التحق بكلية الهندسة بجامعة فيكتوريا مانشستر وهو في الرابعة عشر من عمره، ثم حصل على منحة من جامعة كامبريدج حيث تخصص في حقل الفيزياء النظرية.
ثم اتجه طومسون للعمل في معمل كافندش العريق، وفي عام 1884 م تم تعيينه رئيساً لمعمل كافندش وهو في الثامنة والعشرين من عمره، وقد ترأس المعمل لمدة 34 عاما حتى خلفه تلميذه النيوزلندي ارنست رذرفورد.
يعتبر اكتشافه للإلكترون أفضل بحوثه على الإطلاق وأكثرها شهرةً وتأثيراً، حيث قادته تجاربه على أشعة المهبط (أو أشعة الكاثود) إلى اكتشاف الخواص الأساسيةللإلكترون. حيث قام بتعريض غاز مخلخل لتيار كهربائي فرق جهده حوالي 10,000 فولت تحت ضغط منخفض يتراوح من 0.0001 إلى 0.01 مم/زئبق فلاحظ انطلاق أشعة من الكاثود (مهبط) إلي الآنود (مصعد) وهي أشعة غير منظورة لكنها تحدث توهجاً على جدار أنبوبة التفريغ، وأثبت أن أشعة المهبط ليست أشعة ولكنها سيل متصل من الجسيمات سالبة الشحنة تتأثر بالمجال الكهربي والمجال المغناطيسي وتنحرف طبقاً لشدة مجال كل منهما، كما تمكن من حساب سرعة تلك الجسيمات، لذا فقد اشتهر بلقب ""أبو الإلكترون"".
حصل طومسون على جائزة نوبل عام 1906 م لاكتشافه الإلكترون، ثم ترك العمل في معمل كافندش قرب نهاية الحرب العالمية الأولى وترأس كلية ترينيتي فيكامبريدج، وظل هناك حتى توفي 1940 م عن عمر يناهز الرابعة والثمانين.
#BASSANT
ذرة
الذرة هي أصغر جزء من العنصر الكيميائي الذي يحتفظ بالخصائص الكيميائية لذلك العنصر. يرجع أصل الكلمة الإنجليزية (بالإنجليزية: Atom) إلى الكلمة الإغريقية أتوموس، وتعني غير القابل للانقسام؛ إذ كان يعتقد أنه ليس ثمة ما هو أصغر من الذرة. تتكون الذرة من سحابة من الشحنات السالبة (الإلكترونات) تحوم حول نواة موجبة الشحنة صغيرة جدا في الوسط. تتكون النواة الموجبة هذه من بروتونات موجبة الشحنة، ونيوترونات متعادلة. الذرة هي أصغر جزء من العنصر يمكن أن يتميز به عن بقية العناصر؛ إذ كلما غصنا أكثر في المادة لنلاقي البنى الأصغر لن يعود هناك فرق بين عنصر وآخر. فمثلاً، لا فرق بين بروتون في ذرة حديد وبروتون آخر في ذرة يورانيوم مثلاً، أو ذرة أي عنصر آخر. الذرة، بما تحمله من خصائص؛ عدد بروتوناتها، كتلتها، توزيعها الإلكتروني...، تصنع الفروقات بين العناصر المختلفة، وبين الصور المختلفة للعنصر نفسه (المسماة بالنظائر)، وحتى بين كون هذا العنصر قادراً على خوض تفاعل كيميائي ما أم لا.
ظل تركيب الذرة وما يجري في هذا العالم البالغ الصغر، ظل وما زال يشغل العلماء ويدفعهم إلى اكتشاف المزيد. ومن هنا أخذت تظهر فروع جديدة في العلم حاملة معها مبادئها ونظرياتها الخاصة بها، بدءاً بمبدأ عدم التأكد (اللاثقة)، مروراً بنظريات التوحيد الكبرى، وانتهاءً بنظرية الأوتار الفائقة.
razan madi
الذرة هي أصغر جزء من العنصر الكيميائي الذي يحتفظ بالخصائص الكيميائية لذلك العنصر. يرجع أصل الكلمة الإنجليزية (بالإنجليزية: Atom) إلى الكلمة الإغريقية أتوموس، وتعني غير القابل للانقسام؛ إذ كان يعتقد أنه ليس ثمة ما هو أصغر من الذرة. تتكون الذرة من سحابة من الشحنات السالبة (الإلكترونات) تحوم حول نواة موجبة الشحنة صغيرة جدا في الوسط. تتكون النواة الموجبة هذه من بروتونات موجبة الشحنة، ونيوترونات متعادلة. الذرة هي أصغر جزء من العنصر يمكن أن يتميز به عن بقية العناصر؛ إذ كلما غصنا أكثر في المادة لنلاقي البنى الأصغر لن يعود هناك فرق بين عنصر وآخر. فمثلاً، لا فرق بين بروتون في ذرة حديد وبروتون آخر في ذرة يورانيوم مثلاً، أو ذرة أي عنصر آخر. الذرة، بما تحمله من خصائص؛ عدد بروتوناتها، كتلتها، توزيعها الإلكتروني...، تصنع الفروقات بين العناصر المختلفة، وبين الصور المختلفة للعنصر نفسه (المسماة بالنظائر)، وحتى بين كون هذا العنصر قادراً على خوض تفاعل كيميائي ما أم لا.
ظل تركيب الذرة وما يجري في هذا العالم البالغ الصغر، ظل وما زال يشغل العلماء ويدفعهم إلى اكتشاف المزيد. ومن هنا أخذت تظهر فروع جديدة في العلم حاملة معها مبادئها ونظرياتها الخاصة بها، بدءاً بمبدأ عدم التأكد (اللاثقة)، مروراً بنظريات التوحيد الكبرى، وانتهاءً بنظرية الأوتار الفائقة.
razan madi
النظريات القديمة
للمادة
هناك نظريات قديمه للماده وبدياتها كانت من فلاسفة الاغريق واشهر هؤلاء العلماء هم
دمقريطس والذي عاش بين (370-460) قبل الميلاد وكان يعتقد ان الماده: 1-ان الماده مكونه من اجزاء صغيره وتسمى الذرات 2-ان الماده صلبه، متجانسه، غير قابله للانقسام 3-الأنواع المختلفه من الذرات لها احجام واشكال مختلفة 4-حجم الذرات وشكلها وحركتها يحدد خواص الماده
ولكن أرسطو الذي عاش بين (322-384) قبل الميلاد انتقد ورفض فكرة الذرات لانها لاتتوفق مع افكاره حول الطبيعه وكانت أهم انتقاداته تتعلق بفكرة ان الذرات تتحرك بالفراغ
وكان اعتقاد أرسطو هو: 1-لاوجو للفراغ 2-الماده مكونه من ما، تراب، هواء,نار
أما جون دالتون الذي عاش بين (1766-1844)م كان لديه ستة نظريات أربع منها صحيحة وهي: 1-تتكون المادة منأجزاء صغيرة جداً تسمى الذرات. 2-تختلف ذرات أي عنصر من ذرات العناصر الأخرى. 3-الذرات المختلفة تتحد بنسبة عددية بسيطة لتكوين المركبات. 4-في التفاعلات الكيميائية:تنفصل الذرات,أو تتحد,أو يعاد ترتيبها. وإثنتان منها خاطئة وهي: 1-أن الذرات لا يمكن تجزئتهاوالسبب في أنها خاطئة أنه يمكن تجزئة الذرات إلى جسيمات ذرية. 2-أن جميع الذرات المكون للعنصر لها خواص متماثلة,والخطأ في هذه النظرية أن ذرات العنصر الواحد يمكن أن تختلف بشكل بسيط في كتلتها.
razan madi
هناك نظريات قديمه للماده وبدياتها كانت من فلاسفة الاغريق واشهر هؤلاء العلماء هم
دمقريطس والذي عاش بين (370-460) قبل الميلاد وكان يعتقد ان الماده: 1-ان الماده مكونه من اجزاء صغيره وتسمى الذرات 2-ان الماده صلبه، متجانسه، غير قابله للانقسام 3-الأنواع المختلفه من الذرات لها احجام واشكال مختلفة 4-حجم الذرات وشكلها وحركتها يحدد خواص الماده
ولكن أرسطو الذي عاش بين (322-384) قبل الميلاد انتقد ورفض فكرة الذرات لانها لاتتوفق مع افكاره حول الطبيعه وكانت أهم انتقاداته تتعلق بفكرة ان الذرات تتحرك بالفراغ
وكان اعتقاد أرسطو هو: 1-لاوجو للفراغ 2-الماده مكونه من ما، تراب، هواء,نار
أما جون دالتون الذي عاش بين (1766-1844)م كان لديه ستة نظريات أربع منها صحيحة وهي: 1-تتكون المادة منأجزاء صغيرة جداً تسمى الذرات. 2-تختلف ذرات أي عنصر من ذرات العناصر الأخرى. 3-الذرات المختلفة تتحد بنسبة عددية بسيطة لتكوين المركبات. 4-في التفاعلات الكيميائية:تنفصل الذرات,أو تتحد,أو يعاد ترتيبها. وإثنتان منها خاطئة وهي: 1-أن الذرات لا يمكن تجزئتهاوالسبب في أنها خاطئة أنه يمكن تجزئة الذرات إلى جسيمات ذرية. 2-أن جميع الذرات المكون للعنصر لها خواص متماثلة,والخطأ في هذه النظرية أن ذرات العنصر الواحد يمكن أن تختلف بشكل بسيط في كتلتها.
razan madi
خواص المواد
خواص المادة هي سمات مميزة لكل مادة، وتعرف بأنها غير مقدارية (لا تختلف باختلاف مقدار المادة) ويمكن غالبا وصفها كميا، وذلك من خلال وحدات للقياس تمكننا من المقارنة بين المواد وترتيبها حسب كل خاصية مما يساعد في اختيار المادة حسب المواصفات المطلوبة.فمثلا الكثافة ووحدتها كيلوجرام/مترمكعب هي خاصية غير مقدارية للمادة حيث أنها ثابتة أينما أخذنا العينة من المادة الموجودة . وكذلك حرارة نوعية ووحدتها جول/مول أيضا خاصية غير مقدارية حيث أنها تنطبق على أي مول من المادة . تسمى تلك الخاصيتان وأشباههما في الترموديناميكا "خاصية مكثفة".
وقد تكون خواص المادة رقما ثابتا وقد تتغير حسب متغير (مثل الحرارة) أو أكثر من متغير. وقد تتغير قيمة خواص المادة تبعا لاتجاه القياس وهو ما يعرف بـ تباينية الخواص. مثال على ذلك أن مغناطيسية بلورة في اتجاه المحور السيني قد تختلف عن مغناطيسيتها في اتجاه المحور الصادي.
وبالنسبة للخواص التي تربط بين ظاهرتين طبيعيتين فهي تتغير بشكل خطي أو شبه خطي خلال نطاق معين، فهي تعتبر قيمة ثابتة خلال هذا النطاق
razan madi
خواص المادة هي سمات مميزة لكل مادة، وتعرف بأنها غير مقدارية (لا تختلف باختلاف مقدار المادة) ويمكن غالبا وصفها كميا، وذلك من خلال وحدات للقياس تمكننا من المقارنة بين المواد وترتيبها حسب كل خاصية مما يساعد في اختيار المادة حسب المواصفات المطلوبة.فمثلا الكثافة ووحدتها كيلوجرام/مترمكعب هي خاصية غير مقدارية للمادة حيث أنها ثابتة أينما أخذنا العينة من المادة الموجودة . وكذلك حرارة نوعية ووحدتها جول/مول أيضا خاصية غير مقدارية حيث أنها تنطبق على أي مول من المادة . تسمى تلك الخاصيتان وأشباههما في الترموديناميكا "خاصية مكثفة".
وقد تكون خواص المادة رقما ثابتا وقد تتغير حسب متغير (مثل الحرارة) أو أكثر من متغير. وقد تتغير قيمة خواص المادة تبعا لاتجاه القياس وهو ما يعرف بـ تباينية الخواص. مثال على ذلك أن مغناطيسية بلورة في اتجاه المحور السيني قد تختلف عن مغناطيسيتها في اتجاه المحور الصادي.
وبالنسبة للخواص التي تربط بين ظاهرتين طبيعيتين فهي تتغير بشكل خطي أو شبه خطي خلال نطاق معين، فهي تعتبر قيمة ثابتة خلال هذا النطاق
razan madi
مزيج
قطرة ماء تطفو على سطح زيت. الماء لا يمتزج
بالزيوت.
المزيج أو المخلوط هو مادة كيميائية متجانسة أو غير متجانسة ممتزجة بدون روابط كيميائية بين العناصر الكيميائية أو المركبات الكيميائية فيها والتي قد تكون موجودة بنسب مختلفة ، وبالتالي يحتفظ كل بخواصه وشكله، ويمكن فصل المخاليط بالطرق الكيميائية والفزيائية.
لا يوجد تغييرات كيميائية في المزائج ، أى أن كل مادة موجودة في المزيج تحتفظ بخواصها الفردية وشكلها السابق قبل وضعها في المخلوط . ولكن الخواص الفيزيائية قد تتغير قليلا ، قمثلا تتغير درجة الانصهار للمخلوط عن درجات حرارة مكوناته الفردية .
المزيج المتجانس هي المزائج التي لها تركيب وخواص محددة ، أى أن أى كمية من المخلوط لها نفس التركيب والخواص . مثال لذلك المحاليل وبعض السبائك ( ولكن ليس كلها ).
المزيج اللا متجانس هي المزائج التي لا يكون لها تركيب محدد ، مثال الجرانيت . وتكون البيتزا مثال جيد للمزائج اللا متجانسة . ويقال على المزائج اللا متجانسة أن لها حالات عديدة ( ولا يجب الخلط بين ذلك وبين حالة المادة ), أى أنه يمكن فصل أجزاء من المزيج بالطرق الكيميائية
razan madi
المزيج أو المخلوط هو مادة كيميائية متجانسة أو غير متجانسة ممتزجة بدون روابط كيميائية بين العناصر الكيميائية أو المركبات الكيميائية فيها والتي قد تكون موجودة بنسب مختلفة ، وبالتالي يحتفظ كل بخواصه وشكله، ويمكن فصل المخاليط بالطرق الكيميائية والفزيائية.
لا يوجد تغييرات كيميائية في المزائج ، أى أن كل مادة موجودة في المزيج تحتفظ بخواصها الفردية وشكلها السابق قبل وضعها في المخلوط . ولكن الخواص الفيزيائية قد تتغير قليلا ، قمثلا تتغير درجة الانصهار للمخلوط عن درجات حرارة مكوناته الفردية .
المزيج المتجانس هي المزائج التي لها تركيب وخواص محددة ، أى أن أى كمية من المخلوط لها نفس التركيب والخواص . مثال لذلك المحاليل وبعض السبائك ( ولكن ليس كلها ).
المزيج اللا متجانس هي المزائج التي لا يكون لها تركيب محدد ، مثال الجرانيت . وتكون البيتزا مثال جيد للمزائج اللا متجانسة . ويقال على المزائج اللا متجانسة أن لها حالات عديدة ( ولا يجب الخلط بين ذلك وبين حالة المادة ), أى أنه يمكن فصل أجزاء من المزيج بالطرق الكيميائية
razan madi
مركب كيميائي
المُركب الكيميائي هو مادة كيميائية تكونت من عنصرين أو أكثر، [1][2][3] بنسبة ثابتة تحدد تركيبه، فمثلا الماء (H2O) مركب يتكون من الهيدروجين والأكسجين بنسبة 1:2، وبصفة عامة فإن هذه النسبة يجب
أن تكون ثابتة لبعض الاعتبارات الفيزيائية، وليس طبقا للاختيارات البشرية، ولهذا
السبب فإن المواد مثل النحاس الأصفر تعتبر سبيكة وليست مركب. ومن الخواص المميزة للمركب أن له بنية كيميائية مميزة يعبر عنها عن طريق صيغة جزيئية، تصف هذه الصيغ نسبة الذرات الموجودة به،
وعدد الذرات الموجودة في جزيء واحد من المادة، وعلى هذا فيكون شكل الإيثان C2H4 وليس CH2)، ويمكن عن طريق معرفة تلك الصيغ حساب الكتلة المولية للمركب، توجد عدة معرفات لتمييز المركبات
الكيميائية منها رقم CAS (رقم لتعريف كل المركبات).
ويمكن للمركبات أن يكون لها حالات عديدة. معظم المركبات توجد في هيئة صلبة. كما أن المركبات الجزيئية يمكن أن توجد أيضا في حالة سائلة أو غازية.
مقارنة المركبات والخلائط الخواص الفيزيائية والكيميائية للمركب تختلف عن خواص العناصر المكونة لها وهذه إحدى الطرق للتمييز خلائط العناصرأومواد أخرى لانه مزيج من الخصائص بشكل عام ترتبط ببعضها ارتباطا وثيقا وتعتمد على خصائص المكونات.
يتميز الخليط عن المركب أنه يمكن فصل مكوناته بسهولة بطرق ميكانيكية سواء الترسيب أو التبخر أو باستخدام القوة المغناطيسية لكن لايمكن فصل مكونات المركب إلا بالتفاعل الكيميائي.
يمكن تكوين الخليط بطريقة ميكانيكية بينما يتكون المركب (من عنصر أو مركبات أخرى أو مزيج منهما) عن طريق التفاعل الكيميائي.
بعض الخلائط ترتبط ارتبطا وثيقا بالمركبات ولها نفس الخصائص ومن السهل عدم التفريق بينهم ومثال ذلك السبائك
تصنع السبائك بطريقة ميكانيكية حيث يسخن المعدن إلى أن يتحول إلى الحالة السائلة ويخلط جيدا وتعتبر هذه الطريقة أكثر شيوعا ثم يبرد الخليط مع التحريك بسرعة بحيث تكون المكونات بالأسفل مكونة قاعدة معدنية وامثلة أخرى للمركبات كالخلائط تشمل سبائك المعادن والفلزات القلوية المحلولة في الأمونيا السائل.
razan madi
ويمكن للمركبات أن يكون لها حالات عديدة. معظم المركبات توجد في هيئة صلبة. كما أن المركبات الجزيئية يمكن أن توجد أيضا في حالة سائلة أو غازية.
مقارنة المركبات والخلائط الخواص الفيزيائية والكيميائية للمركب تختلف عن خواص العناصر المكونة لها وهذه إحدى الطرق للتمييز خلائط العناصرأومواد أخرى لانه مزيج من الخصائص بشكل عام ترتبط ببعضها ارتباطا وثيقا وتعتمد على خصائص المكونات.
يتميز الخليط عن المركب أنه يمكن فصل مكوناته بسهولة بطرق ميكانيكية سواء الترسيب أو التبخر أو باستخدام القوة المغناطيسية لكن لايمكن فصل مكونات المركب إلا بالتفاعل الكيميائي.
يمكن تكوين الخليط بطريقة ميكانيكية بينما يتكون المركب (من عنصر أو مركبات أخرى أو مزيج منهما) عن طريق التفاعل الكيميائي.
بعض الخلائط ترتبط ارتبطا وثيقا بالمركبات ولها نفس الخصائص ومن السهل عدم التفريق بينهم ومثال ذلك السبائك
تصنع السبائك بطريقة ميكانيكية حيث يسخن المعدن إلى أن يتحول إلى الحالة السائلة ويخلط جيدا وتعتبر هذه الطريقة أكثر شيوعا ثم يبرد الخليط مع التحريك بسرعة بحيث تكون المكونات بالأسفل مكونة قاعدة معدنية وامثلة أخرى للمركبات كالخلائط تشمل سبائك المعادن والفلزات القلوية المحلولة في الأمونيا السائل.
razan madi